「エスクレチン」の版間の差分
表示
削除された内容 追加された内容
| 53行目: | 53行目: | ||
エスクレチンは、植物に含まれる青色蛍光化合物である<ref>{{cite journal|title = Fluorescence emission spectra of plant leaves and plant constituents|author1 = Lang, M.|author2 = Stober, F.|author3 = Lichtenthaler, H. K.|journal = Radiation And Environmental Biophysics|year = 1991|volume = 30|issue = 4|pages = 333-347|doi = 10.1007/BF01210517}}</ref>。エスクレチンの[[グルコシド]]である[[エスクリン]]は、長波長の[[紫外線]](360nm)で[[蛍光]]を発するが、エスクリンが[[加水分解]]されると蛍光は失われる。また、エスクレチンは[[ウシ血清アルブミン]]の蛍光を消す能力を持つ<ref>{{cite journal|title = Interaction between natural pharmaceutical homologues of coumarin and bovine serum albumin|last1 = Liu|first1 = X.-F.|last2 = Xia|first2 = Y.-M.|last3 = Fang|first3 = Y.|last4 = Zou|first4 = L.|last5 = Liu|first5 = L.-L.|journal = Huaxue xuebao|year = 2004|volume = 62|issue = 16|pages = 1484-1490}}</ref>。 |
エスクレチンは、植物に含まれる青色蛍光化合物である<ref>{{cite journal|title = Fluorescence emission spectra of plant leaves and plant constituents|author1 = Lang, M.|author2 = Stober, F.|author3 = Lichtenthaler, H. K.|journal = Radiation And Environmental Biophysics|year = 1991|volume = 30|issue = 4|pages = 333-347|doi = 10.1007/BF01210517}}</ref>。エスクレチンの[[グルコシド]]である[[エスクリン]]は、長波長の[[紫外線]](360nm)で[[蛍光]]を発するが、エスクリンが[[加水分解]]されると蛍光は失われる。また、エスクレチンは[[ウシ血清アルブミン]]の蛍光を消す能力を持つ<ref>{{cite journal|title = Interaction between natural pharmaceutical homologues of coumarin and bovine serum albumin|last1 = Liu|first1 = X.-F.|last2 = Xia|first2 = Y.-M.|last3 = Fang|first3 = Y.|last4 = Zou|first4 = L.|last5 = Liu|first5 = L.-L.|journal = Huaxue xuebao|year = 2004|volume = 62|issue = 16|pages = 1484-1490}}</ref>。 |
||
エスクレチンは、[[ラット]]の[[肝臓]]の[[カテコール-O-メチルトランスフェラーゼ]]とともに培養することによって、[[スコポレチン]](7-ヒドロキシ-6-メトキシクマリン)や[[イソスコポレチン]](6-ヒドロキシ-7-メトキシクマリン)に変化しうる<ref>{{cite journal|title = 6.7-Dihydroxycoumarin (Aesculetin) as a substrate for catechol-''o''-methyltransferase|journal = Z. Naturforsch. C|year = 1976|issue = 5-6|volume = 31|pages = 280-284|author1 = Müller-Enoch, D.|author2 = Seidl, E.|author3 = Thomas, H.| |
エスクレチンは、[[ラット]]の[[肝臓]]の[[カテコール-O-メチルトランスフェラーゼ]]とともに培養することによって、[[スコポレチン]](7-ヒドロキシ-6-メトキシクマリン)や[[イソスコポレチン]](6-ヒドロキシ-7-メトキシクマリン)に変化しうる<ref>{{cite journal|title = 6.7-Dihydroxycoumarin (Aesculetin) as a substrate for catechol-''o''-methyltransferase|journal = Z. Naturforsch. C|year = 1976|issue = 5-6|volume = 31|pages = 280-284|author1 = Müller-Enoch, D.|author2 = Seidl, E.|author3 = Thomas, H.|pmid = 134569|language = German}}</ref>。 |
||
==関連項目== |
==関連項目== |
||
2020年1月25日 (土) 14:21時点における版
| エスクレチン[1] | |
|---|---|
| |
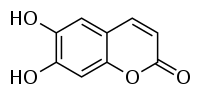
6,7-dihydroxy-2-chromenone | |
別称 esculetin cichorigenin 6,7-dihydroxycoumarin | |
| 識別情報 | |
| CAS登録番号 | 305-01-1 |
| PubChem | 5281416 |
| ChemSpider | 4444764 |
| KEGG | C09263 |
| ChEBI | |
| ChEMBL | CHEMBL244743 |
| |
| |
| 特性 | |
| 化学式 | C9H6O4 |
| モル質量 | 178.14 g mol−1 |
| 精密質量 | 178.026609 u |
| 外観 | white or light yellow powder |
| 特記なき場合、データは常温 (25 °C)・常圧 (100 kPa) におけるものである。 | |
エスクレチン(Aesculetin)は、クマリンの誘導体である。天然のラクトンで、ケイ皮酸誘導体の分子間環化によって生成される。
配糖体またはコーヒー酸複合体の形で、多くの毒性植物、薬草に含まれる[2]。
エスクレチンを含む試料は、抗凝固薬の作用を持ち、ワルファリン等の抗凝固薬と相互作用すると考えられている。
この化合物は、日焼け止め剤にも用いられているが、DNA損傷の光線感作物質として働くという証拠も得られている[3]。メチル誘導体のナトリウム塩は、静脈瘤の治療に用いられる[4]。
エスクレチンは、植物に含まれる青色蛍光化合物である[5]。エスクレチンのグルコシドであるエスクリンは、長波長の紫外線(360nm)で蛍光を発するが、エスクリンが加水分解されると蛍光は失われる。また、エスクレチンはウシ血清アルブミンの蛍光を消す能力を持つ[6]。
エスクレチンは、ラットの肝臓のカテコール-O-メチルトランスフェラーゼとともに培養することによって、スコポレチン(7-ヒドロキシ-6-メトキシクマリン)やイソスコポレチン(6-ヒドロキシ-7-メトキシクマリン)に変化しうる[7]。
関連項目
出典
- ^ “Aesculetin”. Sigma-Aldrich. 2013年1月29日閲覧。
- ^ Dey, P. M.; Harborne, J. B., eds (1997). Plant Biochemistry. Academic Press. ISBN 9780122146749
- ^ Hausen, B. M.; Schmieder, M. (September 1986). “The sensitizing capacity of coumarins (I)”. Contact Dermatitis 15 (3): 157–163. doi:10.1111/j.1600-0536.1986.tb01317.x. PMID 3780217.
- ^ “"Permethol" Data Sheet”. 2013年1月29日閲覧。
- ^ Lang, M.; Stober, F.; Lichtenthaler, H. K. (1991). “Fluorescence emission spectra of plant leaves and plant constituents”. Radiation And Environmental Biophysics 30 (4): 333-347. doi:10.1007/BF01210517.
- ^ Liu, X.-F.; Xia, Y.-M.; Fang, Y.; Zou, L.; Liu, L.-L. (2004). “Interaction between natural pharmaceutical homologues of coumarin and bovine serum albumin”. Huaxue xuebao 62 (16): 1484-1490.
- ^ Müller-Enoch, D.; Seidl, E.; Thomas, H. (1976). “6.7-Dihydroxycoumarin (Aesculetin) as a substrate for catechol-o-methyltransferase” (German). Z. Naturforsch. C 31 (5-6): 280-284. PMID 134569.
