「トリシクロヘキシルホスフィン」の版間の差分
表示
削除された内容 追加された内容
m 基礎情報のテンプレートへの移動 |
|||
| 45行目: | 45行目: | ||
==特長== |
==特長== |
||
特長として、高い[[塩基性]]([[塩基解離定数|{{pKa}} ]]= 9.7)<ref>{{cite journal|first=C. A.|last=Streuli|title=Determination of Basicity of Substituted Phosphines by Nonaqueous Titrimetry|journal=Analyt. Chem.|date=1960|volume=32|page=985–987| |
特長として、高い[[塩基性]]([[塩基解離定数|{{pKa}} ]]= 9.7)<ref>{{cite journal|first=C. A.|last=Streuli|title=Determination of Basicity of Substituted Phosphines by Nonaqueous Titrimetry|journal=Analyt. Chem.|date=1960|volume=32|page=985–987|doi=10.1021/ac60164a027}}</ref> と大きな[[配位子円錐角]](170°)がある<ref>{{cite journal | first1 = R. C. | last1 = Bush | first2 = R. J. | last2 = Angelici | title = Phosphine basicities as determined by enthalpies of protonation | year = 1988 | journal = [[Inorg. Chem.]] | volume = 27 | issue = 4 | pages = 681–686 | doi = 10.1021/ic00277a022}}</ref><ref>{{cite journal | last = Immirzi | first = A. | last2 = Musco | first2 = A. | title = A Method to Measure the Size of Phosphorus Ligands in Coordination Complexes | doi = 10.1016/S0020-1693(00)95635-4 | year = 1977 | journal = Inorg. Chim. Acta | volume = 25 | pages = L41–42}}</ref>。 |
||
==用途== |
==用途== |
||
2020年1月25日 (土) 16:06時点における最新版
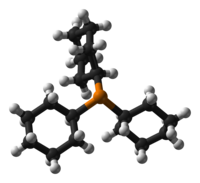
| トリシクロヘキシルホスフィン | |
|---|---|

| |
| |

| |
Tricyclohexylphosphane | |
別称 P(Cy)3 PCy3 | |
| 識別情報 | |
| CAS登録番号 | 2622-14-2 |
| PubChem | 75806 |
| ChemSpider | 68315 |
| |
| |
| 特性 | |
| 化学式 | C18H33P |
| モル質量 | 280.43 g mol−1 |
| 示性式 | P(C6H11)3 |
| 外観 | 白色個体 |
| 融点 |
82 °C, 355 K, 180 °F |
| 水への溶解度 | 有機溶媒 |
| 危険性 | |
| 主な危険性 | 毒性 |
| 特記なき場合、データは常温 (25 °C)・常圧 (100 kPa) におけるものである。 | |
トリシクロヘキシルホスフィン(英語:Tricyclohexylphosphine)は、リンに3個のシクロヘキサンが結合した三級ホスフィンである。多くの場合、Cyはシクロヘキシル基を表すことからPCy3と略記される。 一般的に、有機金属化学における配位子として使用される。
特長[編集]
特長として、高い塩基性(pKa = 9.7)[1] と大きな配位子円錐角(170°)がある[2][3]。
用途[編集]
P(Cy)3錯体として有名な物に、2005年ノーベル化学賞に選ばれたメタセシス反応に使用されるグラブス触媒や、均一系水素添加触媒のクラブトリー触媒がある。
-
第一世代グラブス触媒
-
クラブトリー触媒
出典[編集]
- ^ Streuli, C. A. (1960). “Determination of Basicity of Substituted Phosphines by Nonaqueous Titrimetry”. Analyt. Chem. 32: 985–987. doi:10.1021/ac60164a027.
- ^ Bush, R. C.; Angelici, R. J. (1988). “Phosphine basicities as determined by enthalpies of protonation”. Inorg. Chem. 27 (4): 681–686. doi:10.1021/ic00277a022.
- ^ Immirzi, A.; Musco, A. (1977). “A Method to Measure the Size of Phosphorus Ligands in Coordination Complexes”. Inorg. Chim. Acta 25: L41–42. doi:10.1016/S0020-1693(00)95635-4.


