「酸化プルトニウム(IV)」の版間の差分
閉じられてないspanタグについて、意図不明なため一旦除去。 |
|||
| 49行目: | 49行目: | ||
== 合成 == |
== 合成 == |
||
金属プルトニウムは空気中の酸素によって容易に酸化されて酸化プルトニウム(IV)となる。酸化プルトニウム(IV)は[[再処理工場|核燃料再処理工程]]において抽出されるシュウ酸プルトニウム六水和物((Pu(C<sub>2</sub>O<sub>4</sub>)<sub>2</sub>·6H<sub>2</sub>O)を300℃で[[ |
金属プルトニウムは空気中の酸素によって容易に酸化されて酸化プルトニウム(IV)となる。酸化プルトニウム(IV)は[[再処理工場|核燃料再処理工程]]において抽出されるシュウ酸プルトニウム六水和物((Pu(C<sub>2</sub>O<sub>4</sub>)<sub>2</sub>·6H<sub>2</sub>O)を300℃で[[煆焼]]することで得られる{{要出典|date=December 2012}}。酸化プルトニウム(IV)は[[溶融塩原子炉]]の燃料からウランを六フッ化ウランとして取り除いた後、炭酸ナトリウムを加えることでも得られる。 |
||
== 用途 == |
== 用途 == |
||
2020年7月14日 (火) 19:54時点における最新版
| 酸化プルトニウム(IV) | |
|---|---|
| |
酸化プルトニウム(IV) | |
Plutonium(4+) oxide | |
別称 二酸化プルトニウム Plutonium dioxide | |
| 識別情報 | |
| CAS登録番号 | 12059-95-9 |
| ChemSpider | 10617028 |
| |
| 特性 | |
| 化学式 | O2Pu |
| モル質量 | 276.06 g mol−1 |
| 外観 | 暗黄色結晶 |
| 密度 | 11.5 g cm−3 |
| 融点 |
2390 °C, 2663 K, 4334 °F |
| 沸点 |
2800 °C, 3073 K, 5072 °F |
| 構造 | |
| 結晶構造 | 蛍石 (cubic), cF12 |
| 空間群 | Fm3m, No. 225 |
| 配位構造 | 四面体 (O2−); 立方体 (PuIV) |
| 危険性 | |
| 主な危険性 | Radioactive |
| 特記なき場合、データは常温 (25 °C)・常圧 (100 kPa) におけるものである。 | |
酸化プルトニウム(IV) は化学式 PuO2 で表されるプルトニウムの酸化物である。高融点の固体で主要なプルトニウム化合物である。粒径や温度、製法により黄色やオリーブグリーンなどの様々な色調を呈する[1]。
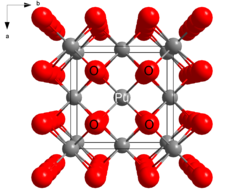
構造
[編集]酸化プルトニウム(IV)は蛍石型結晶で、Pu4+ は面心立方格子の中央に位置し、酸化物イオンは四面体の頂点に位置する[2]。
酸化プルトニウム(IV)の結晶には八面体状に格子欠陥があり、ここに核分裂生成物が入り込むため、実用的な核燃料として利用できる。
核分裂の際に、プルトニウム原子が2つに分裂する。八面体状の格子欠陥に核分裂生成物が入り込むことで元々の酸化プルトニウムの結晶格子が維持されるため、結晶構造が安定するためである[要出典]。
性質
[編集]酸化プルトニウム(IV)は水に極めて溶けにくく高融点(2,390°C)の安定したセラミックである[3]。
プルトニウムのアルファ崩壊により、酸化プルトニウム(IV)の塊に触れると温かさを感じる。他のプルトニウム化合物と同様に、核拡散防止条約の監視対象物質である。
合成
[編集]金属プルトニウムは空気中の酸素によって容易に酸化されて酸化プルトニウム(IV)となる。酸化プルトニウム(IV)は核燃料再処理工程において抽出されるシュウ酸プルトニウム六水和物((Pu(C2O4)2·6H2O)を300℃で煆焼することで得られる[要出典]。酸化プルトニウム(IV)は溶融塩原子炉の燃料からウランを六フッ化ウランとして取り除いた後、炭酸ナトリウムを加えることでも得られる。
用途
[編集]
酸化プルトニウム(IV)は酸化ウラン(IV)と混合して原子炉のMOX燃料に用いられる。プルトニウム238酸化物は深宇宙探査機ニュー・ホライズンズや火星探査機マーズ・サイエンス・ラボラトリーの探査ローバー、キュリオシティーの電源に利用された。これはアルファ崩壊の際に発生する熱を利用している(放射性同位体熱電気転換器を参照)。これらの宇宙機が事故により大気圏に再突入して大きく損傷した場合、プルトニウムが地表や上層大気に撒き散らされると懸念されていた。
物理学者ピーター・ツィンマーマンは、セオドア・ブリュースター・テイラーの提案を元に低威力(1キロトン級)核兵器は酸化プルトニウムから比較的容易に作ることができることを実証した[4]。
毒性
[編集]体内における酸化プルトニウム(IV)の挙動は摂取経路によって変わってくる。酸化プルトニウム(IV)は不溶性であり、経口摂取した場合はその大部分が排泄される[5]。一方、10マイクロメートル(0.01 mm)[3]以下の微粒子を吸入した場合にはアルファ線による内部被曝が問題となる[6]。
関連項目
[編集]脚注
[編集]- ^ “Nitric acid processing”. Los Alamos Laboratory
- ^ Greenwood, Norman N.; Earnshaw, A. (1984), Chemistry of the Elements, Oxford: Pergamon, p. 1471, ISBN 0-08-022057-6
- ^ a b World Nuclear Society, Plutonium (accessed Nov 29 2013)
- ^ Michael Singer, David Weir, and Barbara Newman Canfield (Nov 26, 1979). “Nuclear Nightmare: America's Worst Fear Come True”. New York Magazine
- ^ United States Nuclear Regulatory Commission, Fact sheet on plutonium (accessed Nov 29 2013)
- ^ “Toxicological Profile For Plutonium”. U.S. Department of Health and Human Services (2007年9月27日). 2009年4月23日閲覧。
