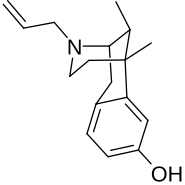
アラゾシン
 | |
| IUPAC命名法による物質名 | |
|---|---|
| |
| データベースID | |
| CAS番号 |
825594-24-9 34061-23-9 (HCl) 14198-28-8 ((–)-isomer) 58640-82-7 ((+)-isomer) 74957-58-7 ((–)-isomer HCl) 133005-41-1 ((+)-isomer HCl) |
| ATCコード | None |
| PubChem | CID: 1235 |
| ChemSpider |
1198 |
| ChEMBL |
CHEMBL274099 |
| 別名 | SKF-10047; WIN-19631; N-Allylnormetazocine; NANM; NAN; ANMC; 2'-Hydroxy-5,9-dimethyl-2-allyl-6,7-benzomorphan |
| 化学的データ | |
| 化学式 | C17H23NO |
| 分子量 | 257.38 g·mol−1 |
| |
アラゾシン(英: alazocine、開発コード: SKF-10047)は、メタゾシンと関連したベンゾモルファン系の合成オピオイド鎮痛剤であり、市販されたことはない[1][2][3]。N-アリルノルメタゾシン(N-allylnormetazocine、NANM)の名称でも一般的に知られる。オピオイド活性に加えて、σ受容体のアゴニストでもあり、この受容体の研究に広く利用されている[4][5]。アラゾシンは強力な鎮痛剤、精神異常発現薬、幻覚剤、モルヒネ様物質、オピオイド拮抗薬として記載されている[2]。さらに、エナンチオマーの1つはσ1受容体を選択的に標識することが発見された最初の化合物であり、この受容体の発見と特徴づけを導いた[4][5]。
薬理作用
[編集]薬物動態
[編集]アラゾシンの薬物動態には立体選択性がみられる[6]。(–)-エナンチオマーは、μ、κ、δオピオイド受容体に対する非選択的高親和性リガンドであり(ラット脳膜標品においてそれぞれKi = 3.0、4.7、15 nM)、一方σ1受容体に対する親和性は非常に低い(Ki = 1,800–4,657 nM)[6][7]。
(±)-アラゾシンはκ-オピオイド受容体に対しては中等度の効力のパーシャルアゴニストとして(HEK293細胞にトランスフェクションしたマウス受容体に対してKi = 0.4 nM、EC50 = 24 nM、Emax= 66%)[8]、一方μ-オピオイド受容体に対してはアンタゴニストとして(Ki = 1.15 nM)作用する[9]。また、δ-オピオイド受容体に対してもはるかに弱い効力でアゴニストとして作用する(Ki: 未報告、IC50 = 184 nM、Imax = 68%)[10]。
(+)-エナンチオマーはオピオイド受容体に対する親和性はほとんどなく(ラット脳膜標品においてμ、κ、δオピオイド受容体に対してそれぞれKi = 1,900、1,600、19,000 nM)、代わりにσ1受容体に対して選択的な高親和性アゴニストとして作用する(Ki = 48–66 nM)[6][7]。しかしながら、(+)-エナンチオマーはNMDA受容体のジゾシルピン(MK-801)やフェンサイクリジン(PCP)結合部位に対しても中等度の親和性を示し(Ki = 587 nM、σ1受容体に対しては45 nM)、高濃度では非競合的NMDA受容体アンタゴニストとしても作用する[11]。そのため、(+)-アラゾシンのσ1受容体に対する選択性は中等度である[11]。
アラゾシンのどちらのエナンチオマーもσ2受容体に対する親和性は非常に低い(ラット脳膜標本またはラットPC12細胞において、Ki = 13,694 nM (+)、4,581 nM (–))[5][7][11]。そのため、(+)-アラゾシンは、放射性リガンド結合アッセイなどで、σ受容体の2つのサブタイプを区別するために利用することができる[5][11]。
まとめると、(–)-アラゾシンは、κオピオイド受容体の選択的パーシャルアゴニスト、μオピオイド受容体のアンタゴニスト、そしてはるかに弱い効力でδオピオイド受容体のアゴニストとして作用し[8][9][10]、σ受容体に対する親和性は非常に低い。一方、(+)-アラゾシンは、σ1受容体に対する選択的アゴニスト、そしてより弱い効力(約10倍)でNMDA受容体に対するアンタゴニストであり、オピオイド受容体やσ2受容体に対する親和性は低い[5][6][7][11]。
歴史
[編集]アラゾシンは初期に研究が行われたベンゾモルファン系オピオイド鎮痛剤の1つである[1]。アラゾシンは1961年に初めて学術文献に記載された[12]。アラゾシンの開発は、1950年代半ばに登場したナロルフィン(N-アリルノルモルヒネ)という類似した薬理作用を持つ強力な鎮痛剤かつオピオイドアンタゴニストに由来する[1]。アラゾシンはヒトで強い精神異常発現作用を示すことが判明し、臨床使用のためのさらなる開発は行われなかった[1][13]。その後、ペンタゾシン(N-ジメチルアリルベンゾモルファン)、シクラゾシン(N-シクロプロピルメチルベンゾモルファン)、フェナゾシン(N-フェニルエチルベンゾモルファン)など、他のベンゾモルファンが開発され、その一部は鎮痛剤として市販されている[1]。
1976年にσ1受容体が命名され、(+)-アラゾシンがその典型的なリガンドとされた[13][14][15]。σ1受容体は当初はオピオイド受容体と考えられ、その後しばらくはNMDA受容体と混同されていたが、最終的には両者から区別された[5][13][14]。アラゾシンや他のベンゾモルファンの精神異常発現作用は、当初はσ1受容体の作動によるものと誤って認識されていたが、その後の研究により、実際にはκ-オピオイド受容体の作動またはNMDA受容体に対する拮抗作用によって引き起こされていることが判明した[5][13]。σ2受容体は1990年に発見と命名が行われたが、この受容体に対するアラゾシンの親和性がσ1受容体と比べて劇的に低いことがこの受容体の同定につながった要因の1つである(ハロペリドール、ジトリルグアニジン、(+)-3-PPPなどの非選択的リガンドは、双方のサブタイプに同等の親和性を示す)[7]。
出典
[編集]- ^ a b c d e A.F. Casy; R.T. Parfitt (29 June 2013). Opioid Analgesics: Chemistry and Receptors. Springer Science & Business Media. pp. 176–178, 420–421. ISBN 978-1-4899-0585-7
- ^ a b Keats, Arthur S.; Telford, Jane (1964). “Narcotic Antagonists as Analgesics”. Molecular Modification in Drug Design. Advances in Chemistry. 45. pp. 170–176. doi:10.1021/ba-1964-0045.ch014. ISBN 0-8412-0046-7. ISSN 0065-2393
- ^ “Pharmacologic effects of N-allylnormetazocine (SKF-10047)”. NIDA Research Monograph 34: 82–8. (February 1981). PMID 6783955.
- ^ a b “Early development of sigma-receptor ligands”. Future Medicinal Chemistry 3 (1): 79–94. (January 2011). doi:10.4155/fmc.10.279. PMID 21428827.
- ^ a b c d e f g “Sigma-1 receptor ligands: potential in the treatment of neuropsychiatric disorders”. CNS Drugs 18 (5): 269–84. (2004). doi:10.2165/00023210-200418050-00001. PMID 15089113.
- ^ a b c d “(+)-[3H]SKF 10,047, (+)-[3H]ethylketocyclazocine, mu, kappa, delta and phencyclidine binding sites in guinea pig brain membranes”. European Journal of Pharmacology 109 (1): 33–41. (February 1985). doi:10.1016/0014-2999(85)90536-9. PMID 2986989.
- ^ a b c d e “A sigma-like binding site in rat pheochromocytoma (PC12) cells: decreased affinity for (+)-benzomorphans and lower molecular weight suggest a different sigma receptor form from that of guinea pig brain”. Brain Research 527 (2): 244–53. (September 1990). doi:10.1016/0006-8993(90)91143-5. PMID 2174717.
- ^ a b “Pharmacological profiles of opioid ligands at kappa opioid receptors”. BMC Pharmacology 6: 3. (January 2006). doi:10.1186/1471-2210-6-3. PMC 1403760. PMID 16433932.
- ^ a b “Activity of opioid ligands in cells expressing cloned mu opioid receptors”. BMC Pharmacology 3: 1. (January 2003). doi:10.1186/1471-2210-3-1. PMC 140036. PMID 12513698.
- ^ a b “Activation profiles of opioid ligands in HEK cells expressing delta opioid receptors”. BMC Neuroscience 3: 19. (November 2002). doi:10.1186/1471-2202-3-19. PMC 137588. PMID 12437765.
- ^ a b c d e “Binding of dimemorfan to sigma-1 receptor and its anticonvulsant and locomotor effects in mice, compared with dextromethorphan and dextrorphan”. Brain Research 821 (2): 516–9. (March 1999). doi:10.1016/s0006-8993(99)01125-7. PMID 10064839.
- ^ “A new potent analgetic antagonist”. Nature 192 (4807): 1089. (December 1961). doi:10.1038/1921089a0. PMID 13900480.
- ^ a b c d Osborne Almeida; Toni S. Shippenberg (6 December 2012). Neurobiology of Opioids. Springer Science & Business Media. pp. 356–. ISBN 978-3-642-46660-1
- ^ a b Jürgen Schüttler; Helmut Schwilden (8 January 2008). Modern Anesthetics. Springer Science & Business Media. pp. 97–. ISBN 978-3-540-74806-9
- ^ “The effects of morphine- and nalorphine- like drugs in the nondependent and morphine-dependent chronic spinal dog”. The Journal of Pharmacology and Experimental Therapeutics 197 (3): 517–32. (June 1976). PMID 945347.
