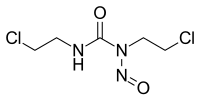
カルムスチン
| カルムスチン | |
|---|---|
| |

| |
別称 N,N’-Bis(2-chloroethyl)-N-nitroso-urea[要出典] | |
| 識別情報 | |
| CAS登録番号 | 154-93-8 |
| PubChem | 2578 |
| ChemSpider | 2480 |
| UNII | U68WG3173Y |
| EC番号 | 205-838-2 |
| 国連/北米番号 | 2811 |
| DrugBank | DB00262 |
| KEGG | D00254 |
| MeSH | Carmustine |
| ChEBI | |
| ChEMBL | CHEMBL513 |
| RTECS番号 | YS2625000 |
| ATC分類 | L01AD01 |
| |
| 特性 | |
| 化学式 | C5H9Cl2N3O2 |
| モル質量 | 214.05 g mol−1 |
| 外観 | Orange crystals |
| 匂い | Odourless |
| 融点 |
30 °C, 303 K, 86 °F |
| log POW | 1.375 |
| 酸解離定数 pKa | 10.194 |
| 塩基解離定数 pKb | 3.803 |
| 薬理学 | |
| 生物学的利用能 | 5–28% |
| 投与経路 |
|
| 代謝 | Hepatic |
| 消失半減期 | 15–30 min |
| 血漿タンパク結合 | 80% |
| 排泄 |
|
| 法的状況 | Prescription only (℞) |
| 胎児危険度分類 | D(US) |
| 危険性 | |
| GHSピクトグラム |  
|
| GHSシグナルワード | DANGER |
| Hフレーズ | H300, H350, H360 |
| Pフレーズ | P301+310, P308+313 |
| EU分類 | |
| Rフレーズ | R45, R46, R60, R61, R28 |
| Sフレーズ | S22, S36/37/39, S45 |
| 半数致死量 LD50 | 20 mg kg−1 (oral, rat) |
| 関連する物質 | |
| 関連するureas | Dimethylurea |
| 関連物質 | |
| 特記なき場合、データは常温 (25 °C)・常圧 (100 kPa) におけるものである。 | |
カルムスチン (英語: Carmustine) は、別名BCNU (bis-chloroethylnitrosourea) とも呼ばれるβ-クロロ-ニトロソウレア化合物であり、アルキル化剤として癌化学療法に用いられる。日本では2012年9月に承認を取得した[2]。
BCNUはジアルキル化剤であるので、2本のDNAを架橋固定して、DNA複製および転写を阻害する。血液脳関門を通過する。原薬は黄橙色の固体である。
商品名はギリアデル。米国ではBiCNUという商品名で、インドではCarustineという商品名で販売されているほか、欧州およびアジア諸国など29カ国で承認されている。
適応
[編集]日本では、脳内留置用製剤が悪性神経膠腫の腫瘍切除後に用いられる[3]。
米国では、脳腫瘍(神経膠腫、多形膠芽腫、髄芽腫、星状細胞腫を含む)のほか、多発性骨髄腫や悪性リンパ腫(ホジキンおよび非ホジキンに用いられる。BCNUはO6-ベンジルグアニン(日本未承認)などのアルキルグアニントランスフェラーゼ(AGT)阻害薬と併用されることが多い。AGT阻害薬はグアニンのN1とシトシンのN3の間で架橋されたDNAの修復を阻害する事でBCNUの有効性を高めることができる。
米国には静脈注射用製剤もあり、骨髄移植の一つ造血幹細胞移植で患者(被移植側)の白血球数を減らすためにも用いられる。この場合通常は、フルダラビンおよびメルファランが併用される。
副作用
[編集]治験での副作用発生率は54.2%であり、その主な内容は、脳浮腫(25.0%)、発熱(12.5%)、リンパ球数減少(12.5%)、片麻痺(不全片麻痺を含む)(12.5%)、悪心(8.3%)、嘔吐(8.3%)、食欲減退(8.3%)、頭痛(8.3%)、ALT (GPT) 増加(8.3%)であった[3]。
重大な副作用として、日本の添付文書には、
- 痙攣、大発作痙攣、脳浮腫、頭蓋内圧上昇、水頭症、脳ヘルニア、
- 創傷治癒不良、感染症(創傷感染、膿瘍、髄膜炎など)、
- 血栓塞栓症(脳梗塞、深部静脈血栓症、肺塞栓症など)、出血(腫瘍出血、脳出血、頭蓋内出血など)
が挙げられている。
留置
[編集]日本では上記の様に、悪性神経膠腫の切除術後に生体内分解性ポリマー基材(ポリフェプロサン20)に含浸した製剤が用いられる。
米国においても、脳腫瘍の治療に用いるために生体分解性ウェハー含浸製剤が認可されており[4]、開頭術中に用いられる[5]。
関連項目
[編集]出典
[編集]- ^ “Carmustine - Compound Summary”. PubChem Compound. USA: National Center for Biotechnology Information (25 March 2005). 11 April 2012閲覧。
- ^ “抗悪性腫瘍剤「ギリアデル脳内留置用剤7.7mg」の製造販売承認をノーベルファーマ社から承継” (2013年11月25日). 2014年11月10日閲覧。
- ^ a b “ギリアデル脳内留置用剤7.7mg 添付文書” (2016年7月). 2016年7月31日閲覧。
- ^ Ewend MG, Brem S, Gilbert M, et al. (June 2007). “Treatment of single brain metastasis with resection, intracavity carmustine polymer wafers, and radiation therapy is safe and provides excellent local control”. Clin. Cancer Res. 13 (12): 3637–41. doi:10.1158/1078-0432.CCR-06-2095. PMID 17575228.
- ^ Gliadel implants (Carmustine) Cancerbackup オリジナルの2007年10月27日時点でのアーカイブ 2021年9月22日閲覧。
