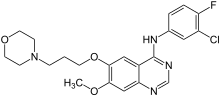
ゲフィチニブ
 | |
| IUPAC命名法による物質名 | |
|---|---|
| |
| 臨床データ | |
| 胎児危険度分類 |
|
| 法的規制 | |
| 薬物動態データ | |
| 生物学的利用能 | 59%(経口時) |
| 血漿タンパク結合 | 90% |
| 代謝 | 肝臓(主にCYP3A4) |
| 半減期 | 6時間 - 49時間 |
| 排泄 | 糞中86%、尿中4%未満 |
| データベースID | |
| CAS番号 | 184475-35-2 |
| ATCコード | L01XX31 (WHO) |
| PubChem | CID: 123631 |
| KEGG | D01977 |
| 化学的データ | |
| 化学式 | C22H24ClFN4O3 |
| 分子量 | 446.902 |
ゲフィチニブ(Gefitinib)は、上皮成長因子受容体 (EGFR) のチロシンキナーゼを選択的に阻害する内服抗がん剤。癌の増殖などに関係する特定の分子を狙い撃ちする分子標的治療薬の一種である。 商品名はイレッサ (Iressa) で、アストラゼネカが製造・販売[1]。褐色の錠剤で一錠250mgのゲフィチニブを含有する。ゲフィチニブ製剤は手術不能または再発した非小細胞肺癌に対する治療薬として用いられる。
イレッサは2002年7月5日、世界に先駆けて日本で承認され、2003年5月5日、アメリカ食品医薬品局 (FDA) での承認[2]を含め、いくつかの国で承認を受けた。しかし、無作為比較臨床試験(ISEL試験[3]、後述)の結果、プラセボと比較して生存期間を延長することができなかったため、2005年1月4日アストラゼネカは欧州医薬品局 (EMEA) への承認申請を取り下げ[4]、また2005年6月17日、FDAは本薬剤の新規使用を原則禁止とした[5]。その後2009年7月1日、欧州医薬品局は、後述のINTEREST試験とIPASS試験の2つの無作為化第III相臨床試験の結果をもとに、成人のEGFR遺伝子変異陽性の局所進行または転移を有する非小細胞肺癌を対象にイレッサの販売承認を行った[6]。2009年現在イレッサを承認している国は、日本を含めたアジア諸国、欧州、オーストラリア、メキシコ、アルゼンチンである。ゲフィチニブは白色から黄白色の粉末。開発コード名ZD1839。
作用機序
[編集]
ゲフィチニブは、細胞の上皮成長因子受容体 (EGFR) のシグナル伝達を遮断することで、腫瘍の増殖抑制、アポトーシス(細胞死)を誘導する。EGFRのチロシンキナーゼのATP結合部位にATPと競合的に結合することで、EGFRの自己リン酸化を阻害し、シグナル伝達を遮断する。実験室レベルでは、正常構造のEGFRに対しても効果を示す[7][8]が、実際の臨床では、腫瘍細胞のEGFR遺伝子が特殊な型の変異を伴っている場合に、ゲフィチニブは特に腫瘍縮小効果を示す[9][10]。
薬物動態学
[編集]経口投与されたゲフィチニブは比較的緩徐に吸収され、内服後最高血中濃度までの時間 (Tmax) は3-5時間、バイオアベイラビリティ(生物学的利用能、吸収効率)は約60%で食事の影響を受けない[11]。ゲフィチニブ225 mg/日内服後の最高血中濃度 (Cmax) は約320 ng/ml(約0.7 μmol/l)[12]。血中濃度が定常状態に達するまで連日内服で7〜10日かかる[13]。血中半減期は48時間[11]。主に肝代謝(シトクロムP450 3A4)により代謝され、糞便中に86%、尿中に4%未満が排泄される[11]。血漿タンパク結合結合率は90%[14]。
効果
[編集]非小細胞肺癌
[編集]要約
- 非小細胞肺癌に対して、ゲフィチニブは約10%から20%の患者に腫瘍縮小効果を示す。東洋人、女性、非喫煙者、腺癌ではゲフィチニブが腫瘍縮小効果を示す割合が高く、これはEGFR遺伝子変異が関係している可能性がある。
- 1種類から2種類の化学療法終了後の進行非小細胞肺癌に対して、ゲフィチニブはドセタキセルと同等の延命効果を示す可能性がある。
- 対象を絞り、非喫煙者、腺癌、アジア人の未治療進行非小細胞肺癌を対象とした臨床試験では、ゲフィチニブは化学療法よりも無増悪生存期間を延長した。
- EGFR遺伝子変異をもつ非小細胞肺癌に対しては特にゲフィチニブは奏功し、70%から80%程度の患者に腫瘍縮小効果を示す。
腫瘍縮小効果
[編集]2000年から2001年に、既治療進行非小細胞肺癌を対象とした2つの第II相臨床試験(IDEAL1[15]とIDEAL2[16])が施行され、ゲフィチニブ単剤で奏功率9%から19%、1年生存率24%から36%の結果が得られた。また、ゲフィチニブの腫瘍縮小効果は、東洋人、女性、腺癌、非喫煙者で高い傾向がみられた。腫瘍縮小を示した非小細胞肺癌を調べた結果、癌細胞がEGFR遺伝子変異を持つ場合に、高率に腫瘍が縮小することが明らかとなり[9][10]、また、非喫煙者、腺癌、女性、東洋人ではEGFRの遺伝子変異をもつ割合が高いために腫瘍縮小率が高い可能性が示された[17][18]。
化学療法との併用
[編集]また2000年から2001年に、未治療進行非小細胞肺癌に対して、初回治療に標準治療であるプラチナ製剤を含む化学療法にゲフィチニブを併用することにより、治療効果に上乗せがあるかどうかが検討された。ゲムシタビン・シスプラチン治療への上乗せ効果を検討したINTACT-1[19]と、パクリタキセル・カルボプラチン治療への上乗せ効果を検討したINTACT-2[20]の二つの第III相無作為化比較試験が施行されたが、いずれも有意な併用効果はみられず、化学療法との併用は効果がないと考えられた。
延命効果
[編集]非小細胞癌全体を対象とした比較
[編集]日本を含まない28か国、1,692例の既治療進行非小細胞肺癌患者を対象とした第III相臨床試験(ISEL試験[3]、2003年7月15日から2004年8月2日に症例登録)においてゲフィチニブは、登録肺癌全症例に対して、および肺腺癌に対して、プラセボと比較して有意な生存期間の延長を示すことができなかった。しかし、サブセット解析では、アジア人、非喫煙者に対してはゲフィチニブはプラセボと比較して有意に生存期間を延長させた。
全肺癌症例の生存期間中央値は、ゲフィチニブ群およびプラセボ群でそれぞれ5.6か月、5.1か月、P =0.11であり、肺腺癌症例ではそれぞれ6.3か月、5.4か月、P =0.07であった。規定のログランク検定 (Logrank test) では有意差がないものの、Cox回帰分析ではそれぞれP =0.030、P =0.033と有意差に達している。また東洋人の生存期間中央値は、ゲフィチニブ群およびプラセボ群でそれぞれ9.5か月、5.5か月、非喫煙者ではそれぞれ8.9か月、6.1か月であり、Cox回帰分析でそれぞれP =0.010、P =0.012であった。 その後さらに、既治療進行非小細胞肺癌に対する現在の標準療法であるドセタキセル療法と、ゲフィチニブ単剤療法の効果を比較した第III相無作為化比較臨床試験が2つ行われた。これら2つの試験は、すでに1 ~ 2種類の化学療法が行われた進行非小細胞肺癌患者にゲフィチニブ療法を行った場合の全生存期間が、ドセタキセル療法を行った場合の全生存期間よりも劣っていないこと(非劣勢)を証明することを目的として行われた。
2003年から2006年の間に489例の患者を対象として日本で行われたV15-32試験[21]は、ゲフィチニブのドセタキセルに対する非劣性を証明できなかった(ただし劣っていることも証明されなかった)。しかし、2004年から2006年の間に、日本を含まない24カ国において1,466例の患者を対象として行われたINTEREST試験では、全生存期間中央値はゲフィチニブ群が7.6か月であったのに対しドセタキセル群は8.9か月、1年生存率はゲフィチニブ群が32%でドセタキセルは34%、ハザード比は1.020(96%信頼区間 0.905-1.150)であり、ドセタキセルとゲフィチニブは既治療進行非小細胞肺癌に対して同等の効果があることが初めて証明された。
この2つの試験の違いとして、後治療の差が指摘されている。つまり、V15-32試験では、ドセタキセル群の53%もの患者がドセタキセル療法終了後にゲフィチニブ療法を受けていたために、ゲフィチニブの効果がドセタキセル群の患者にもあらわれた可能性である。ゲフィチニブ療法終了後にドセタキセル療法を受けた患者はゲフィチニブ群の36%であった。一方INTEREST試験では、ゲフィチニブ群の31%がゲフィチニブ療法終了後にドセタキセル療法を受け、ドセタキセル群の37%がゲフィチニブを含むEGFRチロシンキナーゼ阻害剤の投与を受けていた。
対象を選別しての比較
[編集]さらに、ゲフィチニブの効果が期待できる患者を選別して対象とした無作為化比較第III相臨床試験(IPASS試験)が行われた。この試験は、非喫煙か軽度の喫煙の経験者(15年以上禁煙)で腺癌のアジア人未治療進行非小細胞肺癌患者を、ゲフィチニブ治療群とカルボプラチンとパクリタキセルの併用化学療法群に無作為に振り分け、無増悪生存期間を評価する試験である。2006年5月から2007年10月の間に、日本人232人を含む1,217人が登録された。その結果、ゲフィチニブ治療がカルボプラチン/パクリタキセル併用化学療法よりも無増悪生存期間を延長することが証明されたと発表された(ハザード比 0.74、95%信頼区間 0.65 - 0.85)[22]。ただし、投与開始後6か月間はゲフィチニブの方が疾患制御率が悪く、6か月以降は曲線が交差してカルボプラチン/パクリタキセルの方が悪くなっておりハザード比が大きく変動しているので、比例ハザード(ハザード比が一定を維持)を前提とした統計解析は誤りであり意味がない。事前に計画されていたバイオマーカーに基づくサブグループ解析では、無増悪生存期間はEGFR遺伝子変異陽性患者ではイレッサ群が化学療法群に比べ有意に長く(ハザード比 0.48、95%信頼区間 0.36 - 0.64)、逆にEGFR遺伝子変異陰性患者では化学療法群がイレッサ群に比べ有意に長い(ハザード比 2.85、95%信頼区間 2.05 - 3.98)ことが示された。このことより適切に症例を選択することにより、ゲフィチニブ治療は従来の化学療法よりも優れた効果を示すことが示された。ただし、全生存期間は有意差が付かなかった(ハザード比 0.90、95%信頼区間 0.79 - 1.02)[23]。
EGFR遺伝子変異を有する非小細胞肺癌に対する効果
[編集]EGFR遺伝子変異を有する非小細胞肺癌に対して、ゲフィチニブはその70%から80%程度で腫瘍縮小効果を示すことが、いくつかの後ろ向き研究で指摘された。さらに、未治療非小細胞肺癌に対する前向き試験[24][25]で、これらの患者の75%程度でゲフィチニブが腫瘍縮小効果を示すことが確認された。
さらに、北東日本ゲフィチニブ研究グループで行われた、EGFR遺伝子変異を有する未治療進行非小細胞肺癌患者のみを対象とした無作為化比較第III相臨床試験の結果、ゲフィチニブ治療はカルボプラチン/パクリタキセル併用化学療法よりも有意に無増悪生存期間を延長することが示された。
脳神経膠芽腫
[編集]悪性再発脳神経膠芽腫(グリオブラストーマ)49例に対して、ゲフィチニブ(250 - 1,500 mg/日)またはエルロチニブ(150 - 500 mg/日)が投与され、49例中9例で、2方向計測で25%以上の腫瘍縮小がみられた。EGFRの細胞内領域の変異例はなく、EGFRvIIIとPTENの両者の発現がみられた例では有意に腫瘍縮小と相関がみられた[26]。
頭頸部扁平上皮癌
[編集]52例の頭頸部扁平上皮癌に対するゲフィチニブ(500 mg/日)の効果を検討した第II相試験にて、奏功率10.6%、病勢制御率53%の効果を示した[27]。ゲフィチニブ250 mg/日による臨床試験では70例中1例で腫瘍縮小 (PR) がみられたのみであった[28]。
その他の癌
[編集]31例の進行腎癌に対するゲフィチニブ(500 mg/日)の効果を検討した第II相試験にて、8例 (38%) で腫瘍の増大がみられなかったのみで、腫瘍の縮小はみられなかった[29]。
副作用
[編集]急性肺障害・間質性肺炎を併発(1〜10%)することがあり、これにより死に至り得る。また、下痢、発疹、ざ瘡(にきび)、乾燥皮膚、かゆみ、爪周囲炎が起こることが多い。
添付文書に記載されている重大な副作用は、上記のほか、
- 重度の下痢(<1%)、脱水(<1%)、消化管穿孔(<1%)、消化管潰瘍(<1%)、消化管出血(<1%)、
- 中毒性表皮壊死融解症(Toxic Epidermal Necrolysis:TEN)(<1%)、皮膚粘膜眼症候群(Stevens-Johnson症候群)(<1%)、多形紅斑(<1%)、
- 肝炎(<1%)、肝機能障害(AST(GOT)、ALT(GPT)、LDH、γ-GTP、Al-P、ビリルビン等の上昇 >10%)、黄疸(<1%)、肝不全(<1%)、急性膵炎(<1%)、
- 血尿(<1%)、出血性膀胱炎(<1%)
である[1]。
急性肺障害・間質性肺炎
[編集]投与後4週間以内に発症しやすい。日本において、ゲフィチニブ投与後8週間以内の急性肺障害・間質性肺炎(以下肺障害)の発症率は約5.8%(193例/3322例)、肺障害による死亡率は2.3%(75例/3322例)であった。また PS (performance status) 2以上、喫煙歴のある人、すでに間質性肺炎を合併している人、化学療法を受けたことのある人、では肺障害が起こりやすいことが示唆された[30][31]。また、ゲフィチニブ投与12週以内の肺障害の発症率は、化学療法による肺障害の発症率の1.9倍(4.0%対2.1%)、背景因子を調整すると3.2倍の高さであり、通常の化学療法に比べても肺障害がおこりやすいことが明らかとなった[32]。
ただし、欧米では肺障害はほとんど問題になっておらず、前述のISEL試験では、ゲフィチニブ投与群で3%、プラセボ投与群で4%の発症率であり、ゲフィチニブにより肺障害のリスクは増えていない。ゲフィチニブによる肺障害には民族差がある可能性がある[33]。
「薬害」について
[編集]事実関係
[編集]通常は他の薬の審査待ちで、1年ほどの審査期間が掛かるが、イレッサの場合は優先して審査したので、5か月ほどのスピード承認となった。当初は副作用が少ないと言われていたが、治験では3例で間質性肺炎を発症していずれも治療で回復したが、治験外使用では7例で間質性肺炎を発症したうちの3例が死亡している[34]。承認前に判明していた間質性肺炎は、国内臨床試験で133人中3人、治験外使用では国内で296人中2人、海外を含めると1万人以上で10例前後だったとされる[35]。当初の添付文書の「重大な副作用」の4番目に「間質性肺炎(頻度不明):間質性肺炎があらわれることがあるので,観察を十分に行い,異常がみとめられた場合には,投与を中止し,適切な処置を行うこと」と記載されていた[36]。 販売後の情報収集体制強化を行う市販直後調査より、厚生労働省は同年10月15日、イレッサとの関連性が否定できない副作用26例、うち死亡13例を盛り込んだ緊急安全性情報(イエローレター)を発表。2002年10月(報告月)の1か月で51人、同年11月(報告月)で81人、同12月(報告月)で37人が、それぞれゲフィチニブ服用後の急性肺障害・間質性肺炎等での死亡が報告されたが、その後の死亡報告数は減少している。2006年3月までの累計で643人がゲフィチニブ服用後の急性肺障害・間質性肺炎等での死亡が報告された[37]。2013年4月現在、日本において承認取消や使用制限は行なわれていない。
2004年、患者の遺族達が国と製薬会社を相手取って大阪地方裁判所と東京地方裁判所に提訴した。地裁結審時の原告は計15人[38](大阪地裁側が患者4人[39]の遺族11人[40]、東京地裁側が患者3人の遺族4人[36])となった。
判決
[編集]2011年2月25日、大阪地裁は添付文書に警告欄を設けた2002年10月15日までに服用した患者3人について販売元企業であるアストラゼネカに賠償を命じ、同日以降に服用を始めた患者1人については賠償責任を否定した。その一方で、「死亡を含む重い副作用の危険が具体化すると高い可能性では認識できず、当時の医学、薬学的知見の下では著しく合理性を欠くとは言えない」として国の責任は否定した[39]。
2011年3月23日、東京地裁は第1版添付文書の記載に不備があるとして、この点についてのみであるが国と製薬会社双方の責任を認めた[41]。
2012年5月25日の大阪高等裁判所判決(大阪訴訟の控訴審)[42]、2011年11月15日の東京高等裁判所判決(東京訴訟の控訴審)[43][44]はいずれも製薬会社・国両方の賠償責任を認めず、一審判決を取り消して原告敗訴の判決を言い渡した。2013年4月12日、最高裁判所は各々の二審判決を支持、上告を棄却した[45]。
作用機序をめぐる変遷
[編集]ゲフィチニブは、上皮成長因子受容体 (EGFR) チロシンキナーゼ阻害薬 (Epidermal Growth Factor Receptor-Tyrosine Kinase Inhibitor; EGFR-TKI) であり、EGFRのATP結合部位にATPと競合的に結合して自己リン酸化を阻害することによりシグナル伝達を遮断して、細胞の増殖や分化を抑制する薬として開発された[46]。実験室レベルでは、EGFRを発現する様々な癌細胞(卵巣癌、乳癌、大腸癌、非小細胞肺癌)に有効であることが示された[7][8]。しかし、EGFRは非小細胞肺癌の40-80%で過剰発現がみられる[47]のに対し、ゲフィチニブは非小細胞肺癌患者の10-19%にしか腫瘍縮小効果を示さず[16][15]、EGFRは非小細胞肺癌のうち扁平上皮癌で過剰発現の頻度が高い[48]のに対し、ゲフィチニブは腺癌で有効性が高く[49]、また実際EGFRの発現とゲフィチニブの効果の間には相関がないことが示され[50]、ゲフィチニブは非小細胞癌の一部で劇的な腫瘍縮小効果を示すもののその正確な作用機序は不明であった。
2004年4月29日、ボストン・マサチューセッツ総合病院 (MGH) のトーマス・リンチら[9]と、ボストン・ダナ・ファーバー癌研究所のギジェルモ・パエズら[10]はそれぞれ同日に、ゲフィチニブにより縮小した肺癌のEGFRに遺伝子変異が認められ、この遺伝子変異とゲフィチニブの臨床効果の間に強い相関がみられたという衝撃的な発表を行った。遺伝子変異を持ったEGFRは、そのATP結合部位に構造変化が生じる結果、EGFRが恒常的に活性化して悪性度が高まる一方、ゲフィチニブとの親和性が高まり、EGFRの下流のシグナルが遮断されることによりアポトーシスが誘導され、腫瘍縮小効果を示すという。それまでゲフィチニブは非喫煙者、腺癌、女性、東洋人で有効性が高いことが報告されていたが、これらは非喫煙者、腺癌、女性、東洋人においてEGFRの遺伝子変異をもつ割合が高いことによる可能性が数々の後ろ向き研究で示された[17]。また、このEGFR遺伝子変異にさらに二次的な遺伝子変異がおこると、ゲフィチニブ耐性となることが示された[51][52]。
これに対して、コロラド大学保健科学センターのフェレリコ・カプーゾおよびフレッド・ヒルシュらのグループは、FISH法により検出されるEGFR遺伝子コピー数の増加が、遺伝子変異よりも強く腫瘍縮小および予後と関連していると反論した[53]。また、ゲフィチニブと同様の作用機序を示すエルロチニブを用いた二重盲検無作為化比較試験において、EGFR遺伝子変異は延命効果 (survival benefit) をもたらさず[54]、またエルロチニブに対する腫瘍縮小効果はFISH法によるEGFRの遺伝子コピー数増加と相関していたもののEGFR遺伝子変異とは相関がなかったと報告された[55]。しかし、EGFR遺伝子変異を有する未治療非小細胞肺癌に対する前向き試験[24][25]によって、これらの患者の75%程度でゲフィチニブが腫瘍縮小効果を示すことが確認され、このEGFR遺伝子変異はゲフィチニブの腫瘍縮小を予測する因子であることは定説になりつつある。ただし、EGFR遺伝子変異がなくてもゲフィチニブが有効である症例も存在し、このEGFR遺伝子変異以外にも治療効果を規定する因子がある可能性は十分ある。
一方、ゲフィチニブは、標準的化学療法との併用療法の意義を検証した第III相比較試験 (INTACT1&2) の事後解析では、標準化学療法のみの群でも、EGFR遺伝子変異例がEGFR遺伝子を持たない例よりも予後良好であることから、EGFR遺伝子変異自体が予後良好因子である可能性も指摘されており、ゲフィチニブがEGFR遺伝子変異を持つ非小細胞肺癌を縮小させることができても、それが予後を延長させることに結びついているのかどうかはまた未決着の問題であり、今後の研究が待たれる。
EGFR遺伝子変異を有する症例を対象として、従来から標準治療とされてきたプラチナ製剤併用化学療法とゲフィチニブの比較試験が行われた。その結果、ゲフィチニブが無増悪生存期間で有意に優れていたことが報告され、現在では標準治療の1つとなっている。
出典
[編集]- ^ a b “イレッサ錠250 添付文書” (2015年1月). 2016年7月1日閲覧。
- ^ “Iressa, FDA Approves Drug for Lung Cancer”. MedicineNet.com. (2005年6月20日) 2011年10月6日閲覧。
- ^ a b Thatcher N, Chang A, Parikh P, Rodrigues Pereira J, Ciuleanu T, von Pawel J, Thongprasert S, Tan EH, Pemberton K, Archer V, Carroll K (2005). “Gefitinib plus best supportive care in previously treated patients with refractory advanced non-small-cell lung cancer (Iressa Survival Evaluation in Lung Cancer; ISEL)”. Lancet 366: 1527-1537. doi:10.1016/S0140-6736(05)67625-8. PMID 16257339.
- ^ "GEFITINIB (IRESSA™) MARKETING AUTHORISATION APPLICATION WITHDRAWN IN EU" (Press release). AstraZeneca Pharmaceuticals. 4 January 2005. 2011年10月6日閲覧。
- ^ U.S. Food and Drug Administration. “Gefitinib (marketed as Iressa) Information”. Postmarket Drug Safety Information for Patients and Providers. 2011年10月6日閲覧。
- ^ 『イレッサ、欧州にて非小細胞肺がんを対象に販売承認取得』(プレスリリース)アストラゼネカ ジャパン、2009年7月6日。2011年10月6日閲覧。
- ^ a b Anderson NG, Ahmad T, Chan K, Dobson R, Bundred NJ (2001). “ZD1839 (Iressa), a novel epidermal growth factor receptor (EGFR) tyrosine kinase inhibitor, potently inhibits the growth of EGFR-positive cancer cell lines with or without erbB2 overexpression”. Int. J. Cancer 94: 774-782. doi:10.1002/ijc.1557. PMID 11745477.
- ^ a b Ciardiello F, Tortora G (2001). “Review. A novel approach in the treatment of cancer: targeting the epidermal growth factor receptor”. Clin. Cancer Res. 7: 2958-2970. PMID 11595683.
- ^ a b c Lynch TJ, Bell DW, Sordella R, Gurubhagavatula S, Okimoto RA, Brannigan BW, Harris PL, Haserlat SM, Supko JG, Haluska FG, Louis DN, Christiani DC, Settleman J, Haber DA (2004). “Activating mutations in the epidermal growth factor receptor underlying responsiveness of non-small-cell lung cancer to gefitinib”. NEJM 350: 2129-2139. PMID 15118073.
- ^ a b c Paez JG, Jänne PA, Lee JC, Tracy S, Greulich H, Gabriel S, Herman P, Kaye FJ, Lindeman N, Boggon TJ, Naoki K, Sasaki H, Fujii Y, Eck MJ, Sellers WR, Johnson BE, Meyerson M (2004). “EGFR mutations in lung cancer: correlation with clinical response to gefitinib therapy”. Science 304: 1497-1500. doi:10.1126/science.1099314. PMID 15118125.
- ^ a b c Frampton JE, Easthope SE (2004). “Gefitinib. A review of its use in the management of advanced non-small-cell lung cancer”. Drugs 64: 2475-2492. PMID 15482004.
- ^ Baselga J, Rischin D, Ranson M, Calvert H, Raymond E, Kieback DG, Kaye SB, Gianni L, Harris A, Bjork T, Averbuch SD, Feyereislova A, Swaisland H, Rojo F, Albanell J (2002). “Phase I safety, pharmacokinetic, and pharmacodynamic trial of ZD1839, a selective oral epidermal growth factor receptor tyrosine kinase inhibitor, in patients with five selected solid tumor types”. J. Clin. Oncol. 20: 4292-4302. doi:10.1200/JCO.2002.03.100. PMID 12409327.
- ^ Ranson M, Hammond LA, Ferry D, Kris M, Tullo A, Murray PI, Miller V, Averbuch S, Ochs J, Morris C, Feyereislova A, Swaisland H, Rowinsky EK (2002). “ZD1839, a selective oral epidermal growth factor receptor-tyrosine kinase inhibitor, is well tolerated and active in patients with solid, malignant tumors: results of a phase I trial”. J. Clin. Oncol. 20: 2240-2250. doi:10.1200/JCO.2002.10.112. PMID 11980995.
- ^ FDA (2004年5月6日). “Iressa Label” (PDF). 2011年10月6日閲覧。
- ^ a b Fukuoka M, Yano S, Giaccone G, Tamura T, Nakagawa K, Douillard JY, Nishiwaki Y, Vansteenkiste J, Kudoh S, Rischin D, Eek R, Horai T, Noda K, Takata I, Smit E, Averbuch S, Macleod A, Feyereislova A, Dong RP, Baselga J (2003). “Multi-institutional randomized phase II trial of gefitinib for previously treated patients with advanced non-small-cell lung cancer”. J. Clin. Oncol. 21: 2237-2246. doi:10.1200/JCO.2003.10.038. PMID 12748244.
- ^ a b Kris MG, Natale RB, Herbst RS, Lynch TJ Jr, Prager D, Belani CP, Schiller JH, Kelly K, Spiridonidis H, Sandler A, Albain KS, Cella D, Wolf MK, Averbuch SD, Ochs JJ, Kay AC (2003). “Efficacy of gefitinib, an inhibitor of the epidermal growth factor receptor tyrosine kinase, in symptomatic patients with non-small cell lung cancer: a randomized trial”. JAMA 290: 2149-2158. doi:10.1001/jama.290.16.2149. PMID 14570950.
- ^ a b Pao W, Miller V, Zakowski M, Doherty J, Politi K, Sarkaria I, Singh B, Heelan R, Rusch V, Fulton L, Mardis E, Kupfer D, Wilson R, Kris M, Varmus H (2004). “EGF receptor gene mutations are common in lung cancers from "never smokers" and are associated with sensitivity of tumors to gefitinib and erlotinib”. Proc. Natl. Acad. Sci. USA 101: 13306-13311. doi:10.1073/pnas.0405220101. PMC 516528. PMID 15329413.
- ^ Mitsudomi T, Kosaka T, Endoh H, Horio Y, Hida T, Mori S, Hatooka S, Shinoda M, Takahashi T, Yatabe Y (2005). “Mutations of the epidermal growth factor receptor gene predict prolonged survival after gefitinib treatment in patients with non-small-cell lung cancer with postoperative recurrence”. J. Clin. Oncol. 23 (11): 2513-2520. doi:10.1200/JCO.2005.00.992. PMID 15738541.
- ^ Giaccone G, Herbst RS, Manegold C, Scagliotti G, Rosell R, Miller V, Natale RB, Schiller JH, Von Pawel J, Pluzanska A, Gatzemeier U, Grous J, Ochs JS, Averbuch SD, Wolf MK, Rennie P, Fandi A, Johnson DH (2004). “Gefitinib in combination with gemcitabine and cisplatin in advanced non-small-cell lung cancer: a phase III trial--INTACT 1”. J. Clin. Oncol. 22: 777-784. doi:10.1200/JCO.2004.08.001. PMID 14990632.
- ^ Herbst RS, Giaccone G, Schiller JH, Natale RB, Miller V, Manegold C, Scagliotti G, Rosell R, Oliff I, Reeves JA, Wolf MK, Krebs AD, Averbuch SD, Ochs JS, Grous J, Fandi A, Johnson DH (2004). “Gefitinib in combination with paclitaxel and carboplatin in advanced non-small-cell lung cancer: a phase III trial--INTACT 2”. J. Clin. Oncol. 22: 785-794. doi:10.1200/JCO.2004.07.215. PMID 14990633.
- ^ Maruyama R, Nishiwaki Y, Tamura T, Yamamoto N, Tsuboi M, Nakagawa K, Shinkai T, Negoro S, Imamura F, Eguchi K, Takeda K, Inoue A, Tomii K, Harada M, Masuda N, Jiang H, Itoh Y, Ichinose Y, Saijo N, Fukuoka M (2008). “Phase III study, V-15-32, of gefitinib versus docetaxel in previously treated Japanese patients with non-small-cell lung cancer”. J. Clin. Oncol. 26 (26): 4244-4252. doi:10.1200/JCO.2007.15.0185. PMID 18779611.
- ^ “イレッサ(ゲフィチニブ)アジアにおける進行非小細胞肺がん患者を対象とした大規模臨床試験結果(IPASS) - 欧州臨床腫瘍学会にて発表 -”. アストラゼネカ (2008年9月16日). 2015年6月3日閲覧。
- ^ “IPASS試験の最終解析結果から、 イレッサがEGFR遺伝子変異陽性の進行非小細胞肺がんに対する 有用なファーストライン治療選択肢であることが確認される”. アストラゼネカ (2010年10月12日). 2015年3月23日閲覧。
- ^ a b Inoue A, Suzuki T, Fukuhara T, Maemondo M, Kimura Y, Morikawa N, Watanabe H, Saijo Y, Nukiwa T (2006). “Prospective phase II study of gefitinib for chemotherapy-naive patients with advanced non-small-cell lung cancer with epidermal growth factor receptor gene mutations”. J. Clin. Oncol. 24: 1-6. doi:10.1200/JCO.2005.05.4692. PMID 16785471.
- ^ a b Asahina H, Yamazaki K, Kinoshita I, Sukoh N, Harada M, Yokouchi H, Ishida T, Ogura S, Kojima T, Okamoto Y, Fujita Y, Dosaka-Akita H, Isobe H, Nishimura M (2006). “A phase II trial of gefitinib as first-line therapy for advanced non-small cell lung cancer with epidermal growth factor receptor mutations”. Br. J. Cancer 95: 998-1004. doi:10.1038/sj.bjc.6603393. PMC 2360715. PMID 17047648.
- ^ Mellinghoff IK, Wang MY, Vivanco I, Haas-Kogan DA, Zhu S, Dia EQ, Lu KV, Yoshimoto K, Huang JH, Chute DJ, Riggs BL, Horvath S, Liau LM, Cavenee WK, Rao PN, Beroukhim R, Peck TC, Lee JC, Sellers WR, Stokoe D, Prados M, Cloughesy TF, Sawyers CL, Mischel PS (2005). “Molecular determinants of the response of glioblastomas to EGFR kinase inhibitors”. NEJM 353: 2012-2024. PMID 16282176.
- ^ Cohen EE, Rosen F, Stadler WM, Recant W, Stenson K, Huo D, Vokes EE (2003). “Phase II trial of ZD1839 in recurrent or metastatic squamous cell carcinoma of the head and neck”. J. Clin. Oncol. 21: 1980-1987. doi:10.1200/JCO.2003.10.051. PMID 12743152.
- ^ Cohen EE, Kane MA, List MA, Brockstein BE, Mehrotra B, Huo D, Mauer AM, Pierce C, Dekker A, Vokes EE (2005). “Phase II trial of gefitinib 250 mg daily in patients with recurrent and/or metastatic squamous cell carcinoma of the head and neck”. Clin. Cancer Res. 11: 8418-8424. doi:10.1158/1078-0432.CCR-05-1247. PMID 16322304.
- ^ Dawson NA, Guo C, Zak R, Dorsey B, Smoot J, Wong J, Hussain A (2004). “A phase II trial of gefitinib (Iressa, ZD1839) in stage IV and recurrent renal cell carcinoma”. Clin. Cancer Res. 20: 7812-7819. doi:10.1158/1078-0432.CCR-04-0310. PMID 15585612.
- ^ 吉田茂「ゲフィチニブ プロスペクティブ調査(特別調査)結果報告」『医薬ジャーナル』第41巻、2005年、772-789頁。
- ^ 厚生労働省医薬食品局 (2004年10月). “イレッサ錠250プロスペクティブ調査(特別調査)調査報告書について”. 医薬品・医療用具等安全性情報 206号. 2011年10月6日閲覧。
- ^ 厚生労働省医薬食品局 (2006年). “非小細胞肺癌患者におけるゲフィチニブ投与および非投与での急性肺障害・間質性肺炎の相対リスクおよび危険因子を検討するためのコホート内ケースコントロールスタディ 結果報告書”. 2011年10月6日閲覧。
- ^ 宮崎昌樹、岡本勇「肺癌:個別化医療への最先端研究:人種差、性差を考えたゲフィチニブ治療」『分子呼吸器病』第2号、2007年、154-158頁、ISSN 1342-436X。
- ^ 「薬事行政の根幹」と反発 イレッサ訴訟、強硬姿勢の国 - 中国新聞 [リンク切れ]
- ^ “「イレッサ」副作用訴訟、2月25日に初判決”. 日本経済新聞. (2011年2月18日) 2011年10月6日閲覧。
- ^ a b “平成16年(ワ)第25016号外 薬害イレッサ東日本損害賠償請求事件原告最終準備書面(第3分冊)” (PDF). pp. 8-10. 2011年10月6日閲覧。
- ^ 『ゲフィチニブ服用後の急性肺障害・間質性肺炎等に係る副作用報告の報告件数等について』(プレスリリース)厚生労働省、2006年4月26日。2011年10月6日閲覧。
- ^ イレッサ訴訟、国も和解拒否へMSN産経ニュース [リンク切れ]
- ^ a b イレッサ副作用、国の責任否定=製薬会社に6000万円賠償命令-大阪地裁時事ドットコム[リンク切れ]
- ^ 【イレッサ訴訟】国の「不作為責任」は認めず 大阪地裁「合理性認められる」MSN産経ニュース - http://sankei.jp.msn.com/affairs/news/110225/trl11022516080011-n1.htm
- ^ “東京地裁判決の骨子および要旨”. 薬害イレッサ弁護団. 2012年8月24日閲覧。
- ^ “イレッサ訴訟、企業の責任認めず 患者側逆転敗訴、大阪高裁”. 共同通信. (2012年5月25日) 2012年5月26日閲覧。
- ^ 原告側が逆転敗訴…イレッサ訴訟控訴審読売新聞
- ^ 患者側が逆転敗訴 イレッサ訴訟で東京高裁日本経済新聞
- ^ 平成24年(受)第293号 損害賠償請求事件 平成25年4月12日 第三小法廷判決
- ^ Baselga J, Averbuch SD (2000). “ZD1839 ('Iressa') as an anticancer agent”. Drugs 60 Suppl 1: 33-40. PMID 11129170.
- ^ Arteaga CL (2003). “ErbB2-targeted therapeutic approaches in human cancer”. Exp. Cell Res. 284: 122-130. doi:10.1016/S0014-4827(02)00104-0. PMID 12648471.
- ^ Hirsch FR, Varella-Garcia M, Bunn PA Jr, Di Maria MV, Veve R, Bremmes RM, Barón AE, Zeng C, Franklin WA (2003). “Epidermal growth factor receptor in non-small-cell lung carcinomas: correlation between gene copy number and protein expression and impact on prognosis”. J. Clin. Oncol. 21: 3798-3807. doi:10.1200/JCO.2003.11.069. PMID 12953099.
- ^ Miller VA, Kris MG, Shah N, Patel J, Azzoli C, Gomez J, Krug LM, Pao W, Rizvi N, Pizzo B, Tyson L, Venkatraman E, Ben-Porat L, Memoli N, Zakowski M, Rusch V, Heelan RT (2004). “Bronchioloalveolar pathologic subtype and smoking history predict sensitivity to gefitinib in advanced non-small-cell lung cancer”. J. Clin. Oncol. 22: 1103-1109. doi:10.1200/JCO.2004.08.158. PMID 15020612.
- ^ Cappuzzo F, Gregorc V, Rossi E, Cancellieri A, Magrini E, Paties CT, Ceresoli G, Lombardo L, Bartolini S, Calandri C, de Rosa M, Villa E, Crino L (2003). “Gefitinib in pretreated non-small-cell lung cancer (NSCLC): analysis of efficacy and correlation with HER2 and epidermal growth factor receptor expression in locally advanced or metastatic NSCLC”. J. Clin. Oncol. 21: 2658-2663. doi:10.1200/JCO.2003.01.039. PMID 12860941.
- ^ Pao W, Miller VA, Politi KA, Riely GJ, Somwar R, Zakowski MF, Kris MG, Varmus H (2005). “Acquired resistance of lung adenocarcinomas to gefitinib or erlotinib is associated with a second mutation in the EGFR kinase domain”. PLoS Med. 2: e73. doi:10.1371/journal.pmed.0020073. PMC 549606. PMID 15737014.
- ^ Kobayashi S, Boggon TJ, Dayaram T, Jänne PA, Kocher O, Meyerson M, Johnson BE, Eck MJ, Tenen DG, Halmos B (2005). “EGFR mutation and resistance of non-small-cell lung cancer to gefitinib”. NEJM 352: 786-792. PMID 15728811.
- ^ Cappuzzo F, Hirsch FR, Rossi E, Bartolini S, Ceresoli GL, Bemis L, Haney J, Witta S, Danenberg K, Domenichini I, Ludovini V, Magrini E, Gregorc V, Doglioni C, Sidoni A, Tonato M, Franklin WA, Crino L, Bunn PA Jr, Varella-Garcia M (2005). “Epidermal growth factor receptor gene and protein and gefitinib sensitivity in non-small-cell lung cancer”. J. Natl. Cancer Inst. 97: 643-655. doi:10.1093/jnci/dji112. PMID 15870435.
- ^ Tsao MS, Sakurada A, Cutz JC, Zhu CQ, Kamel-Reid S, Squire J, Lorimer I, Zhang T, Liu N, Daneshmand M, Marrano P, da Cunha Santos G, Lagarde A, Richardson F, Seymour L, Whitehead M, Ding K, Pater J, Shepherd FA (2005). “Erlotinib in lung cancer - molecular and clinical predictors of outcome”. NEJM 353: 133-144. PMID 16014883.
- ^ Shepherd FA, Rodrigues Pereira J, Ciuleanu T, Tan EH, Hirsh V, Thongprasert S, Campos D, Maoleekoonpiroj S, Smylie M, Martins R, van Kooten M, Dediu M, Findlay B, Tu D, Johnston D, Bezjak A, Clark G, Santabárbara P, Seymour L; National Cancer Institute of Canada Clinical Trials Group (2005). “Erlotinib in previously treated non-small-cell lung cancer”. NEJM 353: 123-132. PMID 16014882.
関連項目
[編集]外部リンク
[編集]
