サフラニン
| サフラニン | |
|---|---|
| |

| |
Safranin | |
| 識別情報 | |
| CAS登録番号 | 477-73-6 |
| PubChem | 2723800 |
| ChemSpider | 2005991 |
| |
| |
| 特性 | |
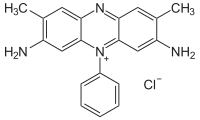
| 化学式 | C20H19N4+, Cl- |
| モル質量 | 350,84 g/mol |
| 特記なき場合、データは常温 (25 °C)・常圧 (100 kPa) におけるものである。 | |
サフラニン(Safranin)またはサフラニンO、ベーシックレッド2は組織学、細胞生物学で用いられる染料である。真核細胞の細胞核や細菌細胞を赤く染める性質を持ち、グラム染色などの対比染色に利用される。また、軟骨[1]、ムチン、肥満細胞顆粒も染色する。植物細胞においては、細胞壁のリグニンのみを染色する用途に利用される[2]。
図の化合物はジメチルサフラニンとも呼ばれるが、下の環のオルト位にメチル基が付加したトリメチルサフラニンも存在する。どちらの化合物もほぼ同じ性質を持ち、特に区別されずに、混合されて使われている。
類縁体
[編集]アゾニウム化合物の中でも、2,8-ジメチル-3,7-ジアミノフェナジン誘導体はSafraninesと呼ばれ、1分子のp-ジアミンと2分子の一級アミンの同時酸化により得られる。まずp-アミノアゾ化合物と一級アミンが縮合し、その後生成したジフェニルメタフェニレンジアミンとp-ニトロソジアルキルアニリンが反応する。
結晶は緑の金属光沢を示し、水に容易に溶けて青-紫の染料となる。強塩基であり、一酸塩として安定でアルコール溶液は橙の蛍光を示す。フェノサフラニンの遊離塩基は不安定だが、塩化物は緑の板状固体として単離できる。容易にジアゾ化でき、ジアゾニウム塩とアルコールを煮沸するとアポサフラニン(C18H12N3)が得られる。F. Kehrmannによると、アポサフラニンは冷濃硫酸存在下でジアゾ化でき、ジアゾニウム塩とアルコールを煮沸することでフェニルフェナゾニウム塩が得られる。アポサフラニンと濃塩酸を加熱することでアポサフラノン(C18H12N2O)が得られる。これらの化合物はオルト、パラキノンとして存在する。流通しているのはo-トルサフラニンである。
最初に工業生産されたアニリン染料は、ウィリアム・パーキンが不純なアニリン・二クロム酸カリウム・硫酸を加熱して作ったモーブである。1878年、パーキンは酸化還元反応によってモーブのトリル基を外すことで、パラサフラニン(1,8-ジメチルサフラニン)を合成できることを示した[3]。
出典
[編集]- ^ Rosenberg L (1971). “Chemical Basis for the Histological Use of Safranin O in the Study of Articular Cartilage” (abstract). J Bone Joint Surg Am. 53 (1): 69–82. PMID 4250366.
- ^ Baldacci‐Cresp, Fabien, et al. (2020). “A rapid and quantitative safranin‐based fluorescent microscopy method to evaluate cell wall lignification”. The Plant Journal 102 (5): 1074-1089. doi:10.1111/tpj.14675.
- ^ W. H. Perkin F.R.S. (1879). “LXXIV.—On mauveine and allied colouring matters”. J. Chem. Soc., Trans. 35: 717–732. doi:10.1039/CT8793500717.
参考文献
[編集] この記事にはアメリカ合衆国内で著作権が消滅した次の百科事典本文を含む: Chisholm, Hugh, ed. (1911). "Safranine". Encyclopædia Britannica (英語). Vol. 23 (11th ed.). Cambridge University Press. p. 10000.
この記事にはアメリカ合衆国内で著作権が消滅した次の百科事典本文を含む: Chisholm, Hugh, ed. (1911). "Safranine". Encyclopædia Britannica (英語). Vol. 23 (11th ed.). Cambridge University Press. p. 10000.
