シクロール仮説
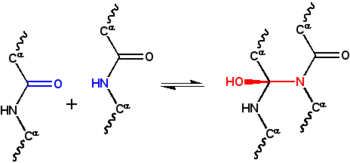
シクロール仮説(シクロールかせつ、英: cyclol hypothesis)は、折り畳まれた球状タンパク質の初の構造モデルである[1]。1930年代末にドロシー・リンチによって構築された本仮説は3つの仮定に基づいている。まずはじめに、本仮説は、2つのペプチド結合がシクロール反応(図1)によって架橋されうることを仮定する。これらの架橋はペプチド基間の「非共有結合性」水素結合の共有結合版である。これらの反応はエルゴペプチド類やその他の化合物において観察される。次に、ある条件下において、アミノ酸が自然に可能な最大の数のシクロール架橋を作り、シクロール分子(図2)およびシクロール生地(cyclol fabrics; 図3)が生じることを仮定する。これらのシクロール分子およびシクロール生地はこれまで観察されたことはない。最後に、本仮説は、球状タンパク質が自由端を持たないシクロール生地から形成されるプラトン立体および半正多面体に対応する三次構造を持つことを仮定する。こういった「閉シクロール」分子についても観察されたことはない。
その後のデータは、球状タンパク質の構造に対するこの最初の模型が修正される必要があることを実証したものの、シクロール反応それ自身や主として疎水性相互作用がタンパク質の折り畳みの原因であるという仮説といった、シクロール模型ののいくつかの要素は立証されている。シクロール仮説は多くの科学者を刺激し、タンパク質の構造および化学についての疑問の研究が行われ、DNA二重らせんやタンパク質の二次構造について仮説が立てられたより正確な模型の先駆者であった。シクロール模型の提唱と検証もまた、科学的方法の一部として機能する経験的反証可能性の優れた例証を与える。
歴史的文脈
[編集]1930年代中頃までには、テオドール・スヴェドベリによって研究された超遠心分析によって、タンパク質はきちんと定められた化学構造を持ち、小分子の凝集体ではないことが示されていた[2]。同じ研究は、タンパク質の分子量が整数によって結び付けられるいくつかのきちんと定められたクラスに分類されることを示しているように見えた[3](例えば、分子量Mw = 2p3q Da; pおよびqは負でない整数)[4]。しかしながら、正確な分子量とタンパク質中のアミノ酸の数を決定するのは困難であった。スヴェドベリは、溶液条件の変化によってタンパク質の小さなサブユニットへの解体(現在は四次構造における変化として知られる)が起こることも示していた[5]。
タンパク質の化学構造は当時まだ論争中であった[6]。最も受け入られていた(そして最終的には正しかった)仮説は、タンパク質が直線状のポリペプチド、すなわちペプチド結合によってつながれたアミノ酸の分岐のないポリマーであるというものであった[7][8]。しかしながら、典型的なタンパク質は著しく長く(数百アミノ酸残基からなる)、数名の著名な科学者らはこういった長く、直線状の高分子が溶液中で安定であるかどうかについて確信がなかった[9][10]。そのうえ、ある酵素がタンパク質を切断するがペプチドを切断しないのに対して、別の酵素はペプチドを切断するが折り畳まれたタンパク質を切断しないことを観察されたため、タンパク質のポリペプチド性に関して疑いが生じた[11]。試験管内でタンパク質を合成する試みは失敗に終わった。これは主にアミノ酸のキラリティが原因である(自然界に存在するタンパク質は「左手型」のアミノ酸だけから構成される)。そのため、エミール・アブデルハルデンのジケトピペラジン仮説といったタンパク質の別の化学的模型が検討された[12][13]。しかしながら、どの代替模型も、なぜタンパク質の加水分解とタンパク質分解によってアミノ酸とペプチドのみが得られるかを説明できなかった。リンデルストロム=ラングによって明白とされたように[14]、これらのタンパク質分解のデータは、変性されたタンパク質がポリペプチドであることを示していたが、折り畳まれたタンパク質の構造に関するデータは得られていなかった。そのため、変性は折り畳まれたタンパク質をポリペプチドへと変換する化学的変化を含むこともあり得た。
タンパク質の変性(凝固と区別される)の過程はハリエット・チックとチャールズ・マーティン によって1910年に発見されていたが[15][16][17][18]、その性質はまだ謎に包まれていた。ティム・アンソンとアルフレッド・ミルスキーは、変性が「可逆的な、2段階過程」(酵素による切断を含む化学反応の対象に多くの化学基がなる)であることを示していた[19][20]。1929年、呉憲(Hsien Wu)は、変性がタンパク質のアンフォールディング、つまりアミノ酸側鎖が溶媒に曝されることになる純粋に立体配座(コンホメーション)的な変化に対応する、という正しい仮説を立てた[21]。呉の仮説はミルスキーとライナス・ポーリングによっても独立に提唱された[22]。にもかかわらず、タンパク質科学者らは、変性がタンパク質構造における「化学的」変化に対応する可能性を排除できず[20]、この仮説はことによると1950年代まで検討されていた[23][24]。
X線結晶構造解析は1911年に分野として始まったばかりで、単純な塩の結晶からコレステロールといった複雑な分子の結晶へと比較的急速に進展していた。しかしながら、最小のタンパク質でさえ1000を超える原子を含むため、タンパク質構造の決定はより複雑であった。1934年、ドロシー・クローフット・ホジキンは小タンパク質であるインスリンの構造に関する結晶データを取っていたが、インスリンやその他のタンパク質の構造は1960年代末まで解かれなかった。しかしながら、羊毛や髪といった多くの天然繊維状タンパク質に関する先駆的なX線繊維回折データがウィリアム・アストベリーによって1930年代初頭に収集されていた。アストベリーはαヘリックスやβシートといった二次構造要素の初歩的模型を提唱した。
タンパク質構造は1930年代まであまり理解されていなかったため、その構造を安定化するために必要な物理的相互作用も同様に未知であった。アストベリーは、繊維状タンパク質の構造がβシート中の水素結合によって安定化される、との仮説を立てた[25][26]。球状タンパク質も水素結合によって安定化されるという着想は1932年にドロシー・ジョーダン・ロイドによって提唱され[27][28]、ミルスキーとポーリングによって後に擁護された[22]。1933年に行われたアストベリーによるOxford Junior Scientific Societyへの講演において、物理学者のフレデリック・フランクは、繊維状タンパク質のα-ケラチンが別の機構、すなわち、上述したシクロール反応によるペプチド結合の「共有結合性」架橋によって安定化されているかもしれない、と提案した[29]。シクロール架橋は2つのペプチド基を互いに近付ける。この時NおよびC原子は1.5オングストローム離れているが、典型的な水素結合では3オングストローム程度離れている。この着想はジョン・デスモンド・バナールの興味を引き付けた。バナールは数学者のドロシー・リンチに、この着想がタンパク質の構造を理解するのに役立つかもしれない、と提案した。
基本理論
[編集]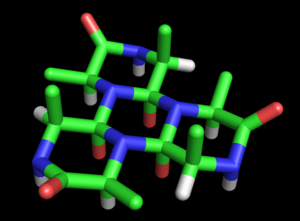
リンチはバナールの提案を本格的なタンパク質構造の模型へと発展させた。基本的なシクロール模型はリンチの最初の論文(1936年)で説明されている[30]。リンチは、ポリペプチドが環化して閉じた環を形成するかもしれないこと(環状ペプチドが存在するのでこれは真である)、これらの環がシクロール反応によって内部架橋を形成するかもしれない(これも真であるが、稀である)という可能性を記している。ペプチド結合のシクロール形がアミド形よりも安定であると仮定して、リンチは、特定の環状ペプチドが自然に最大数のシクロール結合を形成するだろう、と結論付けた。もし分子中の化学結合がおおよそ1.5オングストロームの同じ長さを取るならば、こういったシクロール分子は六方対称性を有する。
これらの環は無限に拡大して、シクロール生地を形成できる(図3)。こういった生地は、長距離の準結晶性秩序を示す。タンパク質は何百もの残基を密に詰め込まなければならないため、リンチはこれがタンパク質においてありえそうだと考えた。こうういった分子および生地のもう1つの興味深い特徴は、それらのアミノ酸側鎖が1つの面からだけ軸方向に上向きになっており、反対側の面には側鎖がないことである。これは、タンパク質の配列に依存しない性質を説明するものではないかと、リンチは推測した。
最初の論文において、リンチは、シクロール模型が単なる「作業仮説」に過ぎず、タンパク質のモデルとして有効である可能性があるが、それを確認する必要がある、と明白に述べている。この論文とその続報におけるリンチも目標はよく定義された検証可能な模型を提案すること、その仮定の結果を検討すること、実験的に検証可能な予測を行うこと、であった。これらの目標においては、リンチは成功した。しかしながら、数年のうちに、実験とさらなるモデリングが、シクロール仮説が球状タンパク質の模型として擁護できないことを示した。
エネルギーの安定化
[編集]
2つの連続した編集者への書簡(1936年)において[31][32]、リンチとフランクは、ペプチド基のシクロール形が実際にアミド形よりも安定かどうかという問題に取り組んだ。比較的単純な計算は、シクロール形がアミド形よりも著しく「不安定」であることを示した。したがって、シクロール模型は、埋め合わせのエネルギー源が同定できない限り、捨てられなければならない。当初、フランクは、シクロール形が周囲の溶媒とのより良い相互作用によって安定化されるかもしれない、と提案した。後に、リンチとアーヴィング・ラングミュアは、非極性側鎖の疎水性会合がシクロール反応のエネルギー的コストを乗り越えるための安定化エネルギーを与える、という仮説を立てた[33][34]。
シクロール結合の不安定性は、本模型の「優位性」として見られた。なぜなら、変性の特性について自然な説明を与えるためである。シクロール結合のより安定なアミド結合への復帰によって構造が広がり、それらの結合がプロテアーゼによる攻撃を受けるようになり、実験と一致する[35][36]。初期の研究は、圧力によって変性されたタンパク質が、高温によって変性された同じタンパク質としばしば異なる状態にあることを示した。これは、変性のシクロール模型を支持しているかもしれないと解釈された[37]。
疎水性安定化のラングミュア・リンチ仮説はシクロール模型と共に失脚したが、これは主にタンパク質が水素結合によって安定化されるという仮説を好んだライナス・ポーリングの影響によるものであった。疎水性相互作用がタンパク質折り畳みの主な原動力であると認られるまでには、さらに20年を要した[38]。
立体的相補性
[編集]シクロールに関する3つ目の論文[39](1936年)において、リンチは、ステロイド類といった多くの「生理学的に活性な」物質が炭素原子の縮合した六角形の環から構成されており、したがって、アミノ酸側鎖を持たないシクロール分子の面と立体的に相補的かもしれない、と記した。リンチは、立体相補性が、小分子が炭素に結合するかどうかを決定する主要な因子の1つである、と提唱した。
リンチは、タンパク質が全ての生体分子の合成に必要である、と推測した。細胞がタンパク質を消化するのは極度の飢餓状態であることから、リンチは、タンパク質がなければ生命は存在できない、とさらに推測した。
ハイブリッド型模型
[編集]その始まりから、シクロール反応は水素結合の共有結合性アナログと見なされた。したがって、両方の種類の結合を持つハイブリッド型模型を考えるのは自然であった。これは、シクロール模型に関するリンチの4つ目の論文の主題であった[40]。この論文は、球状タンパク質が水素結合によって安定化されると最初に提唱したドロシー・ジョーダン・ロイド[27]との共著であった。1937年に書かれた続報は、モーリス・ハギンズやライナス・ポーリングといったタンパク質中の水素結合に関する他の研究者ら[41]を参照している。
リンチはウィリアム・アストベリーとも論文を書き、>CαHαとアミドカルボニル基 >C=Oのケト-エノール異性化の可能性を記している[42]。この異性化によって架橋した>Cα-C(OHα)<が生成し、ここでも再び酸素原子がヒドロキシ基へ変換されている。こういった反応では5員環も生じうるが、古典的シクロール仮説は6員環を生成する。このケト-エノール架橋仮説はこれ以上発展しなかった[43]。
空間を包み込む生地
[編集]
シクロールに関する5つ目の論文[44](1937年)において、リンチは、2つの平面シクロール生地を、化学結合の角度を保ったまま平面間の角度をつけてつなぐことができる条件を明らかにした。リンチは数学的に単純化して、平面ではない6員環の原子を、化学結合の中点からなる平面の「中点六角形(median hexagon)」で表現できることを突き止めた。この「中点六角形」の表現により、平面間の二面角が四面体結合角δ = arccos(-1/3) ≈ 109.47°と等しければ、シクロール生地の平面が正しく結合できることが容易に理解できた。
この基準に合致する幅広い種類の閉多面体を構築することができ、そのうち最も単純なのが切頂四面体や切頂八面体、八面体である。これらはプラトン立体(正多面体)または半正多面体である。最初の一連の「閉シクロール」(切頂四面体をモデルとしたもの)を考えると、リンチはそのアミノ酸の数が72n2(nは閉シクロールのCnの添え字)として二次関数的成長することを示した。したがって、C1シクロールは72残基、C2シクロールは288残基(以下同様)を有する。この予測は、マックス・ベルクマンとカール・ニーマンが行ったアミノ酸分析により[4]予備的な実験的支持を得た。このアミノ酸分析は、タンパク質は288個のアミノ酸残基の整数倍(n=2)で構成されていることを示唆していた。より一般的には、球状タンパク質のシクロール模型は、タンパク質の分子量が整数で結ばれたいくつかのクラスに分類されることを示唆していた[2][3]テオドール・スヴェドベリの初期の超遠心分析の結果を説明した。
シクロール模型は、折り畳まれたタンパク質に当時備わっているとされた一般的な特性と一致していた[45]。(1) 遠心分離の研究では、折り畳まれたタンパク質は水よりもかなり密度が高く(約1.4 g/mL)、したがって密に詰め込まれていることがわかっていた。リンチは、密な詰め込みは規則的な詰め込みを意味すると考えた。(2) タンパク質は大きいにもかかわらず、容易に対称性を有する結晶になるものがあり、これは会合時に対称面が調和するという考えに合致する。(3)タンパク質は金属イオンと結合するが、金属結合部位は特定の結合形状(八面体など)をしているはずなので、タンパク質全体も同様の結晶形状をしていると考えるのが妥当である。(4) 前述のように、シクロールモデルは、変性や、折り畳まれたタンパク質をプロテアーゼで切断することの難しさを、簡単な化学的説明で表していた。(5) タンパク質は、他のタンパク質を含むすべての生物学的分子の合成を担っていると考えられていた。DNAが複製の際に自身を鋳型にするというワトソン–クリック概念と類似して、固定された均一な構造は、タンパク質が合成の際に自らを鋳型にするのに有用であると、リンチは指摘した。また、糖やステロールなどの多くの生体分子が六角形の構造を持っていることを考えると、それらを合成するタンパク質も同様に六角形の構造を持っていると考えるのが妥当である。リンチは、このモデルとそれを裏付ける分子量の実験データを3つの総説にまとめた[46]。
予測されたタンパク質構造
[編集]球状タンパク質のモデルを提案したリンチは、それが利用可能な構造データと一致するかどうかを調べた。リンチは、ウシのツベルクリンタンパク質(523)は72残基からなるC1閉シクロールであり[47]、消化酵素ペプシンは288残基からなるC2閉シクロールであるという仮説を立てた[48][49]。当時のタンパク質の質量を測定する方法は、超遠心法分析や化学的方法など不正確なものであったため、これらの残基数の予測を検証することは困難であった。
また、リンチはインスリンが288残基からなるC2閉シクロールであると予測した。限定的なインスリンのX線結晶構造解析データが利用可能であり、これをリンチは自分のモデルを「裏付ける」ものと解釈した[50][51][52][53][54][55] 。しかし、この解釈は未成熟であるとして、厳しい批判を受けた[56][57][58]。ドロシー・クローフット・ホジキンが撮影したインスリンのパターソン・ダイアグラムを注意深く観察したところ、シクロールとおおよそ一致していた。しかしながら、シクロールモデルが確認されたと主張するには十分な一致ではなかった[59][60][61]。
シクロール模型の非現実性
[編集]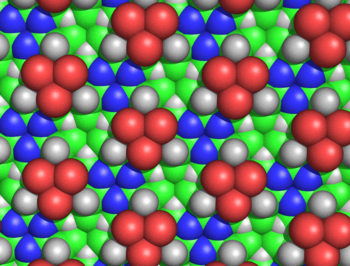
シクロール生地はいくつかの理由でもっともらしくないことが示された。ハンス・ノイラートとHenry Bullは、シクロール生地の側鎖の密な詰め込みが、タンパク質フィルムで実験的に観察された密度と一致しないことを示した[62]。モーリス・ハギンズは、シクロール生地に含まれるいくつかの非結合原子が、ファンデルワールス半径の許容範囲を超えて接近していることを計算した。例えば、くぼみの内側のHα原子とCα原子は、1.68 Åしか離れていない(図5)[63]。ホロウィッツは、タンパク質の外側には多数のヒドロキシ基が存在しないことを化学的に示した[64](これはシクロール模型の重要な予測の反証である)が、マイヤーとホーエネムサーは、アミノ酸のシクロール縮合は遷移状態として微量でも存在しないことを示した[65]。シクロール模型に対するより一般的な化学的議論は、ベルクマンとニーマン[66]、ならびにノイベルガーによってなされた[67][68]。赤外分光データは、タンパク質中のカルボニル基の数は加水分解しても変化しないこと[69]、また、無傷の(正常な)折り畳まれたタンパク質にはアミドカルボニル基が完全に揃っていることが示された[70]。これらの観察結果はどちらも、折り畳まれたタンパク質中でそのようなカルボニル基がヒドロキシ基に変換されるというシクロール仮説とは矛盾する。最後に、タンパク質にはかなりの量(通常5%)のプロリンが含まれていることが知られていた。プロリンにはアミド水素がなく、その窒素はすでに3つの共有結合を形成しているため、プロリンはシクロール反応を起こすことができず、シクロール基を持つ生地にも取り込まれないように見える。シクロール模型に対する化学的・構造的証拠は、ポーリングとニーマンによって百科事典的にまとめられている[71]。さらに、すべてのタンパク質は288個のアミノ酸残基の整数倍を含んでいるという結果は[4]、1939年に同様に正しくないことが示された[72]。
リンチは、シクロール模型に対する立体衝突、自由エネルギー、化学的側面、残基数などの批判に対して、答えた。立体衝突については、結合角と結合長を少し変形させれば、立体衝突を和らげるか、少なくとも合理的な水準まで減らすことができると述べている[73]。例えば、ヘキサメチルベンゼンのメチル基間の距離が2.93 Åであるように、1つの分子内の非結合基間の距離がファンデルワールス半径から予想されるよりも短くなることがあると述べた。シクロール反応の自由エネルギー罰について、リンチはポーリングの計算に同意せず、分子内エネルギーについてはほとんど知られていないため、それだけでシクロール模型を否定することはできないと述べた。化学的な批判に対しては、モデル化合物や単純な二分子反応を研究しても、シクロール模型には関係ないことや、立体障害のために表面のヒドロキシ基が反応しなかったのではないかと提案した[74]。残基数に関する批判に対しては、リンチは模型を拡張して他の残基数を許容した。特に、リンチはわずか48残基の「最小」閉シクロールを作成した[75]。その(誤った)根拠に基づいて、インスリンモノマーの分子量がおよそ6000 Daであることを初めて示唆したのかもしれない[76][77]。
したがって、リンチは、球状タンパク質のシクロール模型はまだ発展の可能性があると主張し[78][79]、細胞骨格の構成要素としてシクロール生地を提案しさえもした[80]。しかしながら、ほとんどのタンパク質科学者はこの模型を信じなくなり、リンチは科学的関心をX線結晶構造解析の数学的問題に向け、それに大きく貢献した。例外として、スミス大学でのリンチの同僚であった物理学者のグラディス・アンスローは、1940年代にタンパク質とペプチドの紫外線吸収スペクトルを研究し、その結果を解釈する際にシクロールの可能性を認めていた[81][82]。フレデリック・サンガーによってインスリンの配列が決定され始めると、アンスローは1948年にリンチが発表した「最小シクロール」模型[75]の骨格を基に、側鎖を持つ3次元シクロール模型を発表した[83]。
部分的な救済
[編集]
シクロール模型全体が破綻すると、一般的にはその要素が否定されることになった。例外としては、J・D・バナールが、タンパク質の折り畳みは疎水性結合によって行われるというラングミュア-リンチ仮説を短期間で受け入れたことが挙げられる[85]。にもかかわらず、1950年代には、天然に存在する小さな環状ペプチドにシクロール結合が確認された。
現代の用語を明確にすることは適切である。古典的なシクロール反応は、あるペプチド基のアミノ基(NH)が別のペプチド基のカルボニル基(C=O)に付加するもので、得られる化合物は現在アザシクロールと呼ばれている。同様に、ペプチドのカルボニル基にヒドロキシ基(OH)が付加するとオキサシクロールとなる。同様に、ペプチジルカルボニル基にチオール部位(SH)を付加すると、チアシクロールが形成される[86]。
菌類であるClaviceps purpurea由来のオキサシクロールアルカロイドであるエルゴタミンが最初に同定されたシクロールであった[87]。また,環状デプシペプチドであるセラタモリドもオキサシクロール反応で生成される[88]。また,化学的に類似した環状のチアシクロルも得られている[89]。また、低分子[90]やトリペプチドには古典的なアザシクロールが見られる[91][92][93]。ペプチドは、アザシクロール形成の逆反応から自然に生成される[94][95][96]。これは、シクロール模型の重要な予測である。エネルギーが不利に高いためにそのような分子は存在しないはずだというライナス・ポーリングの計算にもかかわらず、現在では何百ものサイクロル分子が同定されている[71]。
主にX線結晶学の数学に取り組んでいた長い中断の後、リンチはこれらの発見を受けて、シクロール模型と生化学におけるその関連性に新たな熱意を持って取り組んだ[97][98][99][100][101]。彼女はまた、シクロール理論と低分子ペプチド一般について記述した2冊の本を出版した[102][103]。
科学的方法の例証
[編集]タンパク質構造のシクロール模型は、科学的方法の一部として機能する経験的反証可能性の一例である。独自の仮説は説明のつかない実験的観察を説明するために立てられる。その仮説の結果を検討し、予測を導き出して実験で検証する。今回の場合では、「ペプチド基は、アミド形よりもシクロール形の方が有利である」というのが重要な仮説であった。この仮説は、シクロール-6分子とシクロール生地の予測につながり、球状タンパク質の半正多面体の模型を示唆した。折り畳まれたタンパク質のカルボニル基は、大部分がヒドロキシ基に変換されるはずだという予測は、検証可能な重要な予測であったが、分光学的および化学的実験により、この予測が正しくないことが示された。また、シクロール模型は、折り畳まれたタンパク質やフィルム中のアミノ酸の横方向の密度が高いと予測しているが、これは実験とは一致しない。したがって、シクロール模型は否定され、1940年代から1950年代に提案されたαヘリックス模型のような、タンパク質の構造に関する新しい仮説の探求が始まることになる。
シクロール仮説は、立体的な衝突、プロリンを受け入れることができないこと、シクロール反応自体が不利となる高い自由エネルギーなど、アプリオリな欠陥があるため、提唱すべきではなかったと主張されることがある[104][105]。このような欠陥により、シクロール仮説はあり得ないものとなったが、不可能になったわけではない。シクロール模型は、球状タンパク質について初めて提案された明確な構造であり、当時は分子内力やタンパク質の構造についてほとんど知られていなかったため、すぐに否定することはできなかった。この模型は、タンパク質のいくつかの一般的な特性をきちんと説明し、当時の異常な実験結果を説明した。一般的には間違っていたが、シクロール反応や、タンパク質の折り畳みにおける疎水性相互作用の役割など、サイクロル理論のいくつかの要素は最終的に検証されました。水素原子のボーア模型は、その考案者でさえも当初はあり得ないと考えていたが[106][107][108][109]、最終的に正しい量子力学の理論へと導いたのである。同様に、ライナス・ポーリングは、DNAの明確なモデルを提案した[110]。これも同様に本当とは思えないものだったが、他の研究者にとっては示唆に富むものであった[111][112]。
逆に、シクロール模型は、「明らかに正しい」科学理論の証ともいえる大きな対称性と美しさを持った間違った科学理論の例である。例えば、DNAのワトソン・クリック二重らせんモデル[112]は、その水素結合と対称性から「明らかに正しい」と言われることがあるが、条件によっては対称性のない別の構造が好まれることもある[113]。同様に、美しい一般相対性理論は、アインシュタインが実験的検証を必要としないと考えていたが、この理論でさえ、場の量子論との整合性のために修正が必要である[114]。
出典
[編集]- ^ Tiselius, A (1939). “The Chemistry of Proteins and Amino Acids”. Annual Review of Biochemistry 8: 155–184. doi:10.1146/annurev.bi.08.070139.001103.
- ^ a b Svedberg, T (1929). “Mass and size of protein molecules”. Nature 123 (3110): 871. Bibcode: 1929Natur.123..871S. doi:10.1038/123871a0.
- ^ a b Svedberg, T (1934). “Sedimentation of molecules in centrifugal fields”. Chemical Reviews 14: 1–15. doi:10.1021/cr60047a001.
- ^ a b c Bergmann, M; Niemann C (1937). “On the structure of proteins: cattle hemoglobin, egg albumin, cattle fibrin, and gelatin”. Journal of Biological Chemistry 118: 301–314. doi:10.1016/S0021-9258(18)74540-7.
- ^ Svedberg, T (1930). “The pH Stability Regions of Proteins”. Transactions of the Faraday Society 26: 741–744. doi:10.1039/TF9302600737.
- ^ Fruton, JS (1979). “Early theories of protein structure”. Annals of the New York Academy of Sciences 325 (1): 1–18. Bibcode: 1979NYASA.325....1F. doi:10.1111/j.1749-6632.1979.tb14125.x. PMID 378063.
- ^ Hofmeister, F (1902). “Über Bau und Gruppierung der Eiweisskörper”. Ergebnisse der Physiologie 1: 759–802. doi:10.1007/BF02323641.
- ^ Fischer, E (1902). “Über die Hydrolyse der Proteinstoffe”. Chemiker Zeitung 26: 939–940.
- ^ Fischer, E (1913). “Synthese von Depsiden, Flechtenstoffen und Gerbstoffen”. Berichte der Deutschen Chemischen Gesellschaft 46 (3): 3253–3289. doi:10.1002/cber.191304603109.
- ^ Sørensen, SPL (1930). “The constitution of soluble proteins as reversibly dissociable component systems”. Comptes Rendus des Travaux du Laboratoire Carlsberg 18: 1–124.
- ^ Fruton, JS (1999). Proteins, Enzymes, Genes: The Interplay of Chemistry and Biology. New Haven, CT: Yale University Press. ISBN 0-585-35980-6
- ^ Abderhalden, E (1924). “Diketopiperazines”. Naturwissenschaften 12 (36): 716–720. Bibcode: 1924NW.....12..716A. doi:10.1007/BF01504819.
- ^ Abderhalden, E; Komm E (1924). “Über die Anhydridstruktur der Proteine”. Zeitschrift für Physiologische Chemie 139 (3–4): 181–204. doi:10.1515/bchm2.1924.139.3-4.181.
- ^ Linderstrøm-Lang, K; Hotchkiss RD; Johansen G (1938). “Peptide Bonds in Globular Proteins”. Nature 142 (3605): 996. Bibcode: 1938Natur.142..996L. doi:10.1038/142996a0.
- ^ Chick, H; Martin CJ (1910). “On the "Heat" Coagulation of Proteins”. Journal of Physiology 40 (5): 404–430. doi:10.1113/jphysiol.1910.sp001378. PMC 1533708. PMID 16993016.
- ^ Chick, H; Martin CJ (1911). “On the "Heat" Coagulation of Proteins. II. The Action of Hot Water upon Egg-albumen and the Influence of Acid and Salts upon Reaction Velocity”. Journal of Physiology 43 (1): 1–27. doi:10.1113/jphysiol.1911.sp001456. PMC 1512746. PMID 16993081.
- ^ Chick, H; Martin CJ (1912). “On the "Heat" Coagulation of Proteins. III. The Influence of Alkali upon Reaction Velocity”. Journal of Physiology 45 (1–2): 61–69. doi:10.1113/jphysiol.1912.sp001535. PMC 1512881. PMID 16993182.
- ^ Chick, H; Martin CJ (1912). “On the "Heat" Coagulation of Proteins. IV. The Conditions controlling the Agglutination of Proteins already acted upon by Hot Water”. Journal of Physiology 45 (4): 261–295. doi:10.1113/jphysiol.1912.sp001551. PMC 1512885. PMID 16993156.
- ^ Anson, ML; Mirsky AE (1929). “Protein Coagulation and Its Reversal”. Journal of General Physiology 13 (2): 121–132. doi:10.1085/jgp.13.2.121. PMC 2141032. PMID 19872511.
- ^ a b Anson, ML (1945). “Protein Denaturation and the Properties of Protein Groups”. Advances in Protein Chemistry 2: 361–386. doi:10.1016/S0065-3233(08)60629-4. ISBN 978-0-12-034202-0.
- ^ Wu, H (1931). “Studies on Denaturation of Proteins. XIII. A Theory of Denaturation”. Chinese Journal of Physiology 5: 321–344. Preliminary reports were presented before the XIIIth International Congress of Physiology at Boston (19–24 August 1929) and in the October 1929 issue of the American Journal of Physiology.
- ^ a b Mirsky, AE; Pauling L (1936). “On the Structure of Native, Denatured, and Coagulated Proteins”. Proceedings of the National Academy of Sciences of the United States of America 22 (7): 439–447. Bibcode: 1936PNAS...22..439M. doi:10.1073/pnas.22.7.439. PMC 1076802. PMID 16577722.
- ^ Neurath, H; Greenstein JP; Putnam FW; Erickson JO (1944). “The Chemistry of Protein Denaturation”. Chemical Reviews 34 (2): 157–265. doi:10.1021/cr60108a003.
- ^ Putnam, F (1953). “Protein Denaturation”. The Proteins (H. Neurath and K. Bailey, Eds.) 1B: 807–892.
- ^ Astbury, WT; Woods HJ (1931). “The Molecular Weight of Proteins”. Nature 127 (3209): 663–665. Bibcode: 1931Natur.127..663A. doi:10.1038/127663b0.
- ^ Astbury, WT (1933). “Some Problems in the X-Ray Analysis of the Structure of Animal Hairs and Other Protein Fibres”. Transactions of the Faraday Society 29 (140): 193–211. doi:10.1039/tf9332900193.
- ^ a b Jordan Lloyd, D (1932). “Colloidal Structure and its Biological Significance”. Biological Reviews 7 (3): 254–273. doi:10.1111/j.1469-185x.1962.tb01043.x.
- ^ Jordan Lloyd, D; Marriott (1933). “Title unknown”. Transactions of the Faraday Society 29: 1228. doi:10.1039/tf9332901228.
- ^ Astbury, WT (1936). “Unknown title”. Journal of the Textile Institute 27: 282–?.
- ^ Wrinch, DM (1936). “The Pattern of Proteins”. Nature 137 (3462): 411–412. Bibcode: 1936Natur.137..411W. doi:10.1038/137411a0.
- ^ Wrinch, DM (1936). “Energy of Formation of 'Cyclol' Molecules”. Nature 138 (3484): 241–242. Bibcode: 1936Natur.138..241W. doi:10.1038/138241a0.
- ^ Frank, FC (1936). “Energy of Formation of 'Cyclol' Molecules”. Nature 138 (3484): 242. Bibcode: 1936Natur.138..242F. doi:10.1038/138242a0.
- ^ Langmuir, I; Wrinch DM (1939). “Nature of the Cyclol Bond”. Nature 143 (3611): 49–52. Bibcode: 1939Natur.143...49L. doi:10.1038/143049a0.
- ^ Langmuir, I (1939). “The Structure of Proteins”. Proceedings of the Physical Society 51 (4): 592–612. Bibcode: 1939PPS....51..592L. doi:10.1088/0959-5309/51/4/305.
- ^ Wrinch, DM (1938). “On the Hydration and Denaturation of Proteins”. Philosophical Magazine 25: 705–739.
- ^ Wrinch, DM (1936). “Hydration and Denaturation of Proteins”. Nature 142 (3588): 260. Bibcode: 1938Natur.142..259.. doi:10.1038/142259a0.
- ^ Dow, RB; Matthews JE; Jr. and Thorp WTS (1940). “The Effect of High Pressure Treatment on the Physiological Activity of Insulin”. American Journal of Physiology 131 (2): 382–387. doi:10.1152/ajplegacy.1940.131.2.382.
- ^ Kauzmann, W (1959). “Some Factors in the Interpretation of Protein Denaturation”. Advances in Protein Chemistry 14: 1–63. doi:10.1016/S0065-3233(08)60608-7. ISBN 978-0-12-034214-3. PMID 14404936.
- ^ Wrinch, DM (1936). “Structure of Proteins and of Certain Physiologically Active Compounds”. Nature 138 (3493): 651–652. Bibcode: 1936Natur.138..651W. doi:10.1038/138651a0.
- ^ Wrinch, DM; Jordan Lloyd D (1936). “The Hydrogen Bond and the Structure of Proteins”. Nature 138 (3496): 758–759. Bibcode: 1936Natur.138..758W. doi:10.1038/138758a0.
- ^ Wrinch, DM (1937). “Nature of the Linkage in Proteins”. Nature 139 (3521): 718. Bibcode: 1937Natur.139..718W. doi:10.1038/139718a0.
- ^ Astbury, WT; Wrinch DM (1937). “Intramolecular Folding of Proteins by Keto-Enol Interchange”. Nature 139 (3523): 798. Bibcode: 1937Natur.139..798A. doi:10.1038/139798a0.
- ^ Wrinch, D. “The Fabric Theory of Protein Structure”. Philosophical Magazine 30: 64–67.
- ^ Wrinch, DM (1937). “The Cyclol Theory and the 'Globular' Proteins”. Nature 139 (3527): 972–973. Bibcode: 1937Natur.139..972W. doi:10.1038/139972a0.
- ^ Wrinch, DM (1947). “The Native Protein”. Science 106 (2743): 73–76. Bibcode: 1947Sci...106...73W. doi:10.1126/science.106.2743.73. PMID 17808858.
- ^ Wrinch, DM (1937). “On the Pattern of Proteins”. Proceedings of the Royal Society A160: 59–86.
Wrinch, DM (1937). “The Cyclol Hypothesis and the "Globular" Proteins”. Proceedings of the Royal Society A161: 505–524.
Wrinch, DM (1938). “On the Molecular Weights of the Globular Proteins”. Philosophical Magazine 26: 313–332. - ^ Wrinch, DM (1939). “The Tuberculin Protein TBU-Bovine (523)”. Nature 144 (3636): 77. Bibcode: 1939Natur.144...77W. doi:10.1038/144077a0.
- ^ Wrinch, DM (1937). “On the structure of pepsin”. Philosophical Magazine 24: 940.
- ^ Wrinch, DM (1938). “Structure of Pepsin”. Nature 142 (3587): 217. Bibcode: 1938Natur.142..215.. doi:10.1038/142215a0.
- ^ Wrinch, DM (1937). “On the Structure of Insulin”. Science 85 (2215): 566–567. Bibcode: 1937Sci....85..566W. doi:10.1126/science.85.2215.566. PMID 17769864.
- ^ Wrinch, DM (1937). “On the Structure of Insulin”. Transactions of the Faraday Society 33: 1368–1380. doi:10.1039/tf9373301368.
- ^ Wrinch, DM (1938). “The Structure of the Insulin Molecule”. Journal of the American Chemical Society 60 (8): 2005–2006. doi:10.1021/ja01275a514.
- ^ Wrinch, DM (1938). “The Structure of the Insulin Molecule”. Science 88 (2276): 148–149. Bibcode: 1938Sci....88..148W. doi:10.1126/science.88.2276.148-a. PMID 17751525.
- ^ Wrinch, DM; Langmuir I (1938). “The Structure of the Insulin Molecule”. Journal of the American Chemical Society 60 (9): 2247–2255. doi:10.1021/ja01276a062.
- ^ Langmuir, I; Wrinch DM (1939). “A Note on the Structure of Insulin”. Proceedings of the Physical Society 51 (4): 613–624. Bibcode: 1939PPS....51..613L. doi:10.1088/0959-5309/51/4/306.
- ^ Bragg, WL (1939). “Patterson Diagrams in Crystal Analysis”. Nature 143 (3611): 73–74. Bibcode: 1939Natur.143...73B. doi:10.1038/143073a0.
- ^ Bernal, JD (1939). “Vector Maps and the Cyclol Hypothesis”. Nature 143 (3611): 74–75. Bibcode: 1939Natur.143...74B. doi:10.1038/143074a0.
- ^ Robertson, JM (1939). “Vector Maps and Heavy Atoms in Crystal Analysis and the Insulin Structure”. Nature 143 (3611): 75–76. Bibcode: 1939Natur.143...75R. doi:10.1038/143075a0.
- ^ Riley, DP; Fankuchen I (1939). “A Derived Patterson Analysis of the Skeleton of the Cyclol C2 Molecule”. Nature 143 (3624): 648–649. Bibcode: 1939Natur.143..648R. doi:10.1038/143648a0.
- ^ Wrinch, DM (1940). “Patterson Projection of the Skeletons of the Structure proposed for the Insulin Molecule”. Nature 145 (3687): 1018. Bibcode: 1940Natur.145.1018W. doi:10.1038/1451018a0.
- ^ Riley, D (1940). “A Patterson Analysis derived from the Cyclol C2 Skeleton”. Nature 146 (3694): 231. Bibcode: 1940Natur.146..231R. doi:10.1038/146231a0.
- ^ Neurath, H; Bull HB (1938). “The Surface Activity of Proteins”. Chemical Reviews 23 (3): 391–435. doi:10.1021/cr60076a001.
- ^ Huggins, M (1939). “The Structure of Proteins”. Journal of the American Chemical Society 61 (3): 755. doi:10.1021/ja01872a512.
- ^ Haurowitz, F (1938). “Die Anordnung der Peptidketten in Sphäroprotein-Molekülen”. Hoppe-Seyler's Zeitschrift für Physiologische Chemie 256: 28–32. doi:10.1515/bchm2.1938.256.1.28.
- ^ Meyer, KH; Hohenemser W (1938). “Possibility of the Formation of Cyclols from Simple Peptides”. Nature 141 (3582): 1138–1139. Bibcode: 1938Natur.141.1138M. doi:10.1038/1411138b0.
- ^ Bergmann, M; Niemann C (1938). “The Chemistry of Amino Acids and Proteins”. Annual Review of Biochemistry 7 (2): 99–124. doi:10.1146/annurev.bi.07.070138.000531. PMC 537431.
- ^ Neuberger, A (1939). “Chemical criticism of the cyclol and frequency hypothesis of protein structure”. Proceedings of the Royal Society 170: 64–65.
- ^ Neuberger, A (1939). “Chemical Aspects of the Cyclol Hypothesis”. Nature 143 (3620): 473. Bibcode: 1939Natur.143..473N. doi:10.1038/143473a0.
- ^ Haurowitz, F; Astrup T (1939). “Ultraviolet absorption of genuine and hydrolysed protein”. Nature 143 (3612): 118–119. Bibcode: 1939Natur.143..118H. doi:10.1038/143118b0.
- ^ Klotz, IM; Griswold P (1949). “Infrared Spectra and the Amide Linkage in a Native Globular Protein”. Science 109 (2830): 309–310. Bibcode: 1949Sci...109..309K. doi:10.1126/science.109.2830.309. PMID 17782718.
- ^ a b Pauling, L; Niemann C (1939). “The Structure of Proteins”. Journal of the American Chemical Society 61 (7): 1860–1867. doi:10.1021/ja01876a065.
- ^ Hotchkiss, RD (1939). “The Determination of Peptide Bonds in Crystalline Lactoglobulin”. Journal of Biological Chemistry 131: 387–395. doi:10.1016/S0021-9258(18)73511-4.
- ^ Wrinch, DM (1941). “The Geometrical Attack on Protein Structure”. Journal of the American Chemical Society 63 (2): 330–33. doi:10.1021/ja01847a004.
- ^ Wrinch, DM (1940). “The Cyclol Hypothesis”. Nature 145 (3678): 669–670. Bibcode: 1940Natur.145..669W. doi:10.1038/145669a0.
- ^ a b Wrinch, DM (1948). “The Native Proteins as Polycondensations of Amino Acids”. Science 107 (2783): 445–446. Bibcode: 1948Sci...107R.445W. doi:10.1126/science.107.2783.445-a. PMID 17844448.
- ^ Wrinch, DM (1948). “Skeletal Units in Protein Crystals”. Science 115 (2987): 356–357. Bibcode: 1952Sci...115..356W. doi:10.1126/science.115.2987.356. PMID 17748855.
- ^ Wrinch, DM (1948). “Molecules of the Insulin Structure”. Science 116 (3021): 562–564. Bibcode: 1952Sci...116..562W. doi:10.1126/science.116.3021.562. PMID 13015111.
- ^ Wrinch, DM (1939). “The Structure of the Globular Proteins”. Nature 143 (3620): 482–483. Bibcode: 1939Natur.143..482W. doi:10.1038/143482a0.
- ^ Wrinch, DM (1939). “The Cyclol Theory and the Structure of Insulin”. Nature 143 (3627): 763–764. Bibcode: 1939Natur.143..763W. doi:10.1038/143763a0.
- ^ Wrinch, DM (1939). “Native Proteins, Flexible Frameworks and Cytoplasmic Organization”. Nature 150 (3800): 270–271. Bibcode: 1942Natur.150..270W. doi:10.1038/150270a0.
- ^ Anslow, GA (1942). “Bond Energies in Some Protein Fabrics and Side Chains”. Physical Review 61 (7–8): 547. Bibcode: 1942PhRv...61..541.. doi:10.1103/PhysRev.61.541.
- ^ Anslow, GA (1945). “Ultraviolet Spectra of Biologically Important Molecules”. Journal of Applied Physics 16 (1): 41–49. Bibcode: 1945JAP....16...41A. doi:10.1063/1.1707499.
- ^ Anslow, GA (1953). “The Sites of the Amino-Acid Residues on a Cyclol Model of Insulin”. Journal of Chemical Physics 21 (11): 2083–2084. Bibcode: 1953JChPh..21.2083A. doi:10.1063/1.1698765.
- ^ Guedez, T; Núñez A; Tineo E; Núñez O (2002). “Ring size configuration effect and the transannular intrinsic rates in bislactam macrocycles”. Journal of the Chemical Society, Perkin Transactions 2 2002 (12): 2078–2082. doi:10.1039/b207233e.
- ^ Bernal, JD (1939). “Structure of proteins”. Nature 143 (3625): 663–667. Bibcode: 1939Natur.143..663B. doi:10.1038/143663a0.
- ^ Wieland T and Bodanszky M, The World of Peptides, Springer Verlag, pp.193–198. ISBN 0-387-52830-X
- ^ Hofmann, A; Ott H; Griot R; Stadler PA; Frey AJ (1963). “Synthese von Ergotamin”. Helvetica Chimica Acta 46: 2306–2336. doi:10.1002/hlca.19630460650.
- ^ Shemyakin, MM; Antonov VK; Shkrob AM (1963). “Activation of the amide group by acylation”. Peptides, Proc. 6th Europ. Pept. Symp., Athens: 319–328.
- ^ Zanotti, G; Pinnen F; Lucente G; Cerrini S; Fedeli W; Mazza F (1984). “Peptide thiacyclols. Synthesis and structural studies”. J. Chem. Soc. Perkin Trans. 1: 1153–1157. doi:10.1039/p19840001153.
- ^ Griot, RG; Frey AJ (1963). “The formation of cyclols from N-hydroxyacyl lactames”. Tetrahedron 19 (11): 1661–1673. doi:10.1016/S0040-4020(01)99239-7.
- ^ Lucente, G; Romeo A (1971). “Synthesis of cyclols from small peptides via amide-amide reaction”. Chem. Commun. ?: 1605–1607. doi:10.1039/c29710001605.
- ^ Rothe M, Schindler W, Pudill R, Kostrzewa U, Theyson R, and Steinberger R. (1971) "Zum Problem der Cycloltripeptidsynthese", Peptides, Proc. 11th Europ. Pept. Symp., Wien, 388–399.
- ^ Rothe M and Roser KL. (1988) "Conformational flexibility of cyclic tripeptides", Abstr. 20th Europ. Pept. Symp. Tübingen, p. 36.
- ^ Wieland T and Mohr H. (1956) "Diacylamide als energiereiche Verbindungen. Diglycylimid", Liebigs Ann. Chem., 599, 222–232.
- ^ Wieland T and Urbach H. (1958) "Weitere Di-Aminoacylimide und ihre intramolekulare Umlagerung", Liebigs Ann. Chem., 613, 84–95.
- ^ Brenner, M (1958). Wolstenholme GEW; O'Connor CM. eds. “The aminoacyl insertion”. Ciba Foundation Symposium on Amino Acids and Peptides with Antimetabolic Activity.
- ^ Wrinch, DM (1957). “Structure of Bacitracin A”. Nature 179 (4558): 536–537. Bibcode: 1957Natur.179..536W. doi:10.1038/179536a0.
- ^ Wrinch, DM (1957). “An Approach to the Synthesis of Polycyclic Peptides”. Nature 180 (4584): 502–503. Bibcode: 1957Natur.180..502W. doi:10.1038/180502b0.
- ^ Wrinch, DM (1962). “Some Issues in Molecular Biology and Recent Advances in the Organic Chemistry of Small Peptides”. Nature 193 (4812): 245–247. Bibcode: 1962Natur.193..245W. doi:10.1038/193245a0. PMID 14008494.
- ^ Wrinch, DM (1963). “Recent Advances in Cyclol Chemistry”. Nature 199 (4893): 564–566. Bibcode: 1963Natur.199..564W. doi:10.1038/199564a0.
- ^ Wrinch, DM (1965). “A Contemporary Picture of the Chemical Aspects of Polypeptide Chain Structures and Certain Problems of Molecular Biology”. Nature 206 (4983): 459–461. Bibcode: 1965Natur.206..459W. doi:10.1038/206459a0. PMID 5319104.
- ^ Wrinch, DM (1960). Chemical Aspects of the Structures of Small Peptides: An Introduction. Copenhagen: Munksgaard
- ^ Wrinch, DM (1965). Chemical Aspects of Polypeptide Chain Structures and the Cyclol Theory. New York: Plenum Press
- ^ Kauzmann, W (1993). “Reminiscences from a life in protein physical chemistry”. Protein Science 2 (4): 671–691. doi:10.1002/pro.5560020418. PMC 2142355. PMID 8518739.
- ^ Tanford, C; Reynolds J (2001). Nature's robots: A history of proteins. Oxford: Oxford University Press. ISBN 0-19-850466-7
- ^ Pais, A (1986). Inward Bound: Of Matter and Forces in the Physical World. Oxford University Press. ISBN 0-19-851971-0
Bohr, N (1913). “On the Constitution of Atoms and Molecules (Part 1 of 3)”. Philosophical Magazine 26: 1–25. Bibcode: 1913PMag...26....1B. doi:10.1080/14786441308634955. オリジナルの2007-07-04時点におけるアーカイブ。. - ^ Bohr, N (1913). “On the Constitution of Atoms and Molecules, Part II Systems Containing Only a Single Nucleus”. Philosophical Magazine 26 (153): 476–502. Bibcode: 1913PMag...26..476B. doi:10.1080/14786441308634993.
- ^ Bohr, N (1913). “On the Constitution of Atoms and Molecules, Part III”. Philosophical Magazine 26: 857–875. Bibcode: 1913PMag...26..857B. doi:10.1080/14786441308635031.
- ^ Bohr, N (1914). “The spectra of helium and hydrogen”. Nature 92 (2295): 231–232. Bibcode: 1913Natur..92..231B. doi:10.1038/092231d0.
- ^ Pauling, L; Corey RB (1953). “A Proposed Structure For The Nucleic Acids”. Proceedings of the National Academy of Sciences 39 (2): 84–97. Bibcode: 1953PNAS...39...84P. doi:10.1073/pnas.39.2.84. PMC 1063734. PMID 16578429.
- ^ Franklin, RE; Gosling R (1953). “Molecular configuration of sodium thymonucleate”. Nature 171 (4356): 740–741. Bibcode: 1953Natur.171..740F. doi:10.1038/171740a0. PMID 13054694.
- ^ a b Watson, JD; Crick F (1953). “Molecular structure of nucleic acids: A structure for deoxyribonucleic acid”. Nature 171 (4356): 737–738. Bibcode: 1953Natur.171..737W. doi:10.1038/171737a0. PMID 13054692.
- ^ Saenger, W (1988). Principles of Nucleic Acid Structure. Springer Verlag. ISBN 0-387-90762-9
- ^ Pais, A. (1982). Subtle is the Lord: The Science and the Life of Albert Einstein. Oxford University Press. ISBN 0-19-853907-X
推奨文献
[編集]- “Protein Units Put in Graphic 'Cage'”, The New York Times: p. 14, (19 April 1940).
- “Waffle-Iron Theory of Proteins”, The New York Times: p. E9, (2 February 1947).
- Senechal, Marjorie, ed. (1980), Structures of Matter and Patterns in Science, inspired by the work and life of Dorothy Wrinch, 1894–1976: Proceedings of a Symposium held at Smith College, Northampton, Massachusetts on 28–30 September 1977, Schenkman Publishing Company.
- "Selected papers of Dorothy Wrinch, from the Sophia Smith Collection", in Structures of Matter and Patterns in Science.
- Senechal, Marjorie (2013), I Died For Beauty: Dorothy Wrinch and the Cultures of Science, Oxford University Press.
外部リンク
[編集]- 生体分子構造解析特論 第2回スライド&ノート - 渡邉信久
