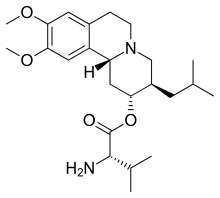
バルベナジン
 | |
| IUPAC命名法による物質名 | |
|---|---|
| |
| 臨床データ | |
| 販売名 | ジスバル(日本)、イングレッザ(米国) |
| Drugs.com | monograph |
| MedlinePlus | a617023 |
| ライセンス | US Daily Med:リンク |
| 法的規制 |
|
| 薬物動態データ | |
| 血漿タンパク結合 | >99% |
| 代謝 | 加水分解による活性化、 CYP3A、CYP2D6による不活性化 |
| 代謝物質 | [+]-α-Dihydrotetrabenazine (active metabolite) |
| 半減期 | 15–22 時間 |
| 排泄 | 60% 尿、30% 便 |
| 識別 | |
| CAS番号 | 1025504-45-3 |
| ATCコード | N07XX13 (WHO) |
| PubChem | CID: 24795069 |
| DrugBank | DB11915 |
| ChemSpider | 28536134 |
| UNII | 54K37P50KH |
| KEGG | D10675 |
| ChEMBL | CHEMBL2364639 |
| 別名 | NBI-98854 |
| 化学的データ | |
| 化学式 | C24H38N2O4 |
| 分子量 | 418.58 g·mol−1 |
| |
| |
バルベナジン(英: Valbenazine) は、ニューロクライン・バイオサイエンシズが開発した遅発性ジスキネジアの治療薬[1]。小胞モノアミントランスポーター2 (VMAT2) 阻害薬として作用する[2]。アメリカの商品名はイングレッザ[3]。日本の商品名はジスバル[4]。
医学用途
[編集]バルベナジンは、遅発性ジスキネジアの治療に使用される[5]。遅発性ジスキネジアは、薬剤誘発性の神経障害で不随意運動を特徴とする[6] 。バルベナジンがアメリカ食品医薬品局に承認された臨床試験は、6週間の期間で行われた[5] 。業界がスポンサーとなった研究では、バルベナジンの使用が最大48週間にわたって安全かつ効果的であることが確認され、遅発性ジスキネジアの短期(6週間)の改善を維持できることが示された[7]。
副作用
[編集]副作用には傾眠とQT延長が含まれる可能性がある[8]。 推奨用量では重大なQT延長はまだ報告されていないが、CYP2D6またはCYP3A4の肝酵素を抑制する薬剤を服用していたり、CYP2D6の代謝が遅い場合は、重大なQT延長のリスクがある可能性がある[8]。
バルベナジンの妊婦への研究は乏しいため、妊娠中または授乳中の女性には使用を避けることが推奨される[8]。
歴史
[編集]- 2017年
- 2021年
- 2022年
- 2023年
薬理学
[編集]作用機序
[編集]バルベナジンは、選択的に小胞モノアミントランスポーター2 (VMAT2)を阻害することにより、ドーパミン放出を可逆的に減少させる[12]。in vitroにおいて、バルベナジンがはVMAT2に対して高い選択性を示し、VMAT1やその他のモノアミン受容体に対してはほとんど親和性を示さない[12]。遅発性ジスキネジアの正確な原因は不明であるが、神経遮断薬によるドパミン過感受性が原因である可能性があると考えられている[13] 。バルベナジンは、VMAT2がドパミンをシナプス小胞に取り込むことを選択的に減少させ[14]、シナプス間隙におけるパミンの全体的なレベルを減少させ、ドパミン過感受性に関連する症状を緩和させる。 バルベナジンがVMAT2を選択的に阻害することの重要性は、VMAT2が主にドパミンの輸送に関与しており、他のモノアミン(ノルアドレナリン、セロトニン、ヒスタミンなど)の輸送には比較的影響が少ない点である[15]。
薬物動態
[編集]バルベナジンは、プロドラッグであり、[+]-α-ジヒドロテトラベナジン(DTBZ)とアミノ酸L-バリンのエステルである。バルベナジンの半減期は15~22時間、分解に関与する肝酵素はCYP3A4、CYP3A5およびCYP2D6である。尿(60%)および便(30%)で排泄される。
研究
[編集]バルベナジンはトゥレット障害の治療薬として研究されている[16][17]。
脚注
[編集]- ^ a b “Ingrezza- valbenazine capsule; Ingrezza- valbenazine kit”. DailyMed (18 August 2023). 17 November 2023閲覧。
- ^ “NBI-98854, a selective monoamine transport inhibitor for the treatment of tardive dyskinesia: A randomized, double-blind, placebo-controlled study”. Movement Disorders 30 (12): 1681–7. (October 2015). doi:10.1002/mds.26330. PMC 5049616. PMID 26346941.
- ^ a b c “遅発性ジスキネジア治療薬バルベナジン(MT-5199:VMAT2阻害剤)国内における製造販売承認申請のお知らせ”. 田辺三菱製薬株式会社. 田辺三菱製薬株式会社 (2021年4月22日). 2024年10月11日閲覧。
- ^ a b “田辺三菱、「ジスバル」の承認取得 国内初の遅発性ジスキネジア薬”. 日刊薬業 - 医薬品産業の総合情報サイト. 株式会社じほう (2022年3月28日). 2024年10月11日閲覧。
- ^ a b “Ingrezza- valbenazine capsule; Ingrezza- valbenazine kit”. DailyMed (18 August 2023). 17 November 2023閲覧。
- ^ “Tardive dyskinesia”. rarediseases.info.nih.gov (1 June 2017). 18 June 2017時点のオリジナルよりアーカイブ。21 February 2018閲覧。
- ^ “Long-term Valbenazine Appears Safe for Patients With Tardive Dyskinesia”. www.medscape.com. Reuters Health Information. 21 February 2018閲覧。[リンク切れ]
- ^ a b c “Valbenazine: Drug Information”. UpToDate. 2017年7月14日閲覧。
- ^ Al Idrus, Amirah (January 2, 2018). “After Disappointing 2016, New Drug Approvals Roared Back to Life in 2017”. FierceBiotech. 2024年9月21日閲覧。
- ^ a b “遅発性ジスキネジア治療剤の新薬ジスバルカプセル40mg発売/田辺三菱|CareNet.com”. CareNet.com. CareNet,Inc (2022年6月14日). 2024年10月11日閲覧。
- ^ a b “【中医協】「ウィフガート」「ジスバル」は薬価引き下げへ 3品目の費用対効果評価案を報告”. 日刊薬業 - 医薬品産業の総合情報サイト. 株式会社じほう (2023年10月11日). 2024年10月11日閲覧。
- ^ a b “NBI-98854 – VMAT2 Inhibitor | Tics in Children Treatment | Neurocrine Biosciences”. www.neurocrine.com. 2015年1月30日時点のオリジナルよりアーカイブ。2016年11月13日閲覧。
- ^ “tardive-dyskinesia”. www.priory.com. 2016年11月13日閲覧。
- ^ Neuroscience (Sixth ed.). Sinauer Associates. (2018). ISBN 978-1-60535-380-7
- ^ “NBIX: NDA for Valbenazine in Tardive Dyskinesia to be Filed in 2016…” 2016年11月13日閲覧。
- ^ “Tourette Syndrome Clinical Trials”. Neurocrine Biosciences. 2016年11月14日時点のオリジナルよりアーカイブ。2016年11月13日閲覧。
- ^ 臨床試験番号 NCT02581865 研究名 "Safety and Efficacy Study of NBI-98854 in Adults With Tourette Syndrome" - ClinicalTrials.gov
