ファルカリンジオール
表示
| ファルカリンジオール | |
|---|---|
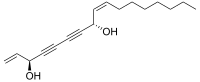
| |
(3R,8S,9Z)-1,9-Heptadecadiene-4,6-diyne-3,8-diol | |
別称 cis-Heptadeca-1,9-diene-4,6-diyne-3,8-diol | |
| 識別情報 | |
| CAS登録番号 | 55297-87-5 |
| PubChem | 5281148 |
| ChemSpider | 4444588 |
| ChEMBL | CHEMBL69018 |
| |
| |
| 特性 | |
| 化学式 | C17H24O2 |
| モル質量 | 260.371 |
| 特記なき場合、データは常温 (25 °C)・常圧 (100 kPa) におけるものである。 | |
ファルカリンジオール (Falcarindiol) は、ニンジンの根で見られる、抗菌活性を持つポリアセチレン構造を有する化合物である[1][2]。
ニンジンの苦味の主成分となっている[3]。ファルカリンジオールやその他のファルカリンジオール型のポリアセチレンは、イノンドやパセリなど、セリ科のニンジン以外の植物でも見られる[4]。さまざまな生理活性が報告されており[5][6][7]、健康増進代謝作用があると考えられることから、サプリメントとして研究されている[8]。
関連項目
[編集]出典
[編集]- ^ Garrod, B. (1978). “Cis-heptadeca-1,9-diene-4,6-diyne-3,8-diol, an antifungal polyacetylene from carrot root tissue”. Physiologial Plant Pathology 13 (2): 241–246. doi:10.1016/0048-4059(78)90039-5.
- ^ Kemp, M. S. (1978). “Falcarindiol: An antifungal polyacetylene from Aegopodium podagraria”. Phytochemistry 17 (5): 1002. doi:10.1016/S0031-9422(00)88669-0.
- ^ Czepa, A.; Hofmann, T. (2003). “Structural and sensory characterization of compounds contributing to the bitter off-taste of carrots (Daucus carota L.) and carrot puree”. Journal of Agricultural and Food Chemistry 51 (13): 3865–3873. doi:10.1021/jf034085+. PMID 12797757.
- ^ Christensen, L. P.; Brandt, K. (2006). “Bioactive polyacetylenes in food plants of the Apiaceae family: Occurrence, bioactivity and analysis”. Journal of Pharmaceutical and Biomedical Analysis 41 (3): 683–693. doi:10.1016/j.jpba.2006.01.057. PMID 16520011.
- ^ Atanasov, A. G.; Blunder, M.; Fakhrudin, N.; Liu, X.; Noha, S. M.; Malainer, C.; Kramer, M. P.; Cocic, A.; Kunert, O.; Schinkovitz, A.; Heiss, E. H.; Schuster, D.; Dirsch, V. M.; Bauer, R. (2013). “Polyacetylenes from Notopterygium incisum - new selective partial agonists of peroxisome proliferator-activated receptor-gamma”. PLoS ONE 8 (4): e61755. doi:10.1371/journal.pone.0061755. PMC 3632601. PMID 23630612.
- ^ Jin, H. R.; Zhao, J.; Zhang, Z.; Liao, Y.; Wang, C. Z.; Huang, W. H.; Li, S. P.; He, T. C.; Yuan, C. S.; Du, W. (2012). “The antitumor natural compound falcarindiol promotes cancer cell death by inducing endoplasmic reticulum stress”. Cell Death and Disease 3 (8): e376. doi:10.1038/cddis.2012.122. PMC 3434669. PMID 22914324.
- ^ Wyrembek, P.; Negri, R.; Kaczor, P.; Czyżewska, M.; Appendino, G.; Mozrzymas, J. W. (2012). “Falcarindiol allosterically modulates GABAergic currents in cultured rat hippocampal neurons”. Journal of Natural Products 75 (4): 610–616. doi:10.1021/np2008522. PMID 22432736.
- ^ Christensen, L. P. (2011). “Aliphatic C17-Polyacetylenes of the Falcarinol Type as Potential Health Promoting Compounds in Food Plants of the Apiaceae Family”. Recent Patents on Food, Nutrition and Agriculture 3 (1): 64–77. doi:10.2174/2212798411103010064. PMID 21114468.
