ベンズバレン
表示
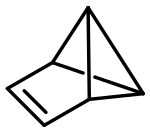
| ベンズバレン | |
|---|---|
| |
tricyclo[3.1.0.02,6]hex-3-ene | |
| 識別情報 | |
| CAS登録番号 | [https://commonchemistry.cas.org/detail?cas_rn=6&title=5 6 5 6 5] |
| PubChem | 136470 |
| ChemSpider | 120239 |
| |
| |
| 特性 | |
| 化学式 | C6H6 |
| モル質量 | 78.11 g mol−1 |
| 特記なき場合、データは常温 (25 °C)・常圧 (100 kPa) におけるものである。 | |
ベンズバレン(英: benzvalene)は、ベンゼンの異性体の1つである有機化合物である[1]。Thomas J. Katzらが1971年に合成した[2][3]。
1971年の合成では、シクロペンタジエンをジメチルエーテル中でメチルリチウムで処理し、その後ジクロロメタンとメチルリチウムで −45 ℃ で処理する。溶液中の炭化水素は、特異な嫌な匂いを持つと言われる。分子の持つ立体歪みのため、純粋な物質は、ひっかく等するだけで容易に爆発する。
ベンズバレンは、約10日の半減期でベンゼンに変換する。この対称禁制転移は、ジラジカル中間体を経て生じると考えられている[4]。
ポリベンズバレン
[編集]ベンズバレンは、開環メタセシス重合によってポリベンズバレンを形成する[5]。このポリマーは、非常に歪んだビシクロブタン環を含むため、やはり取り扱いに注意を要する物質となっている。この環は、1,3-ジエンに異性化することができ、このためポリベンズバレンはポリアセチレンの原料として研究されている。
出典
[編集]- ^ Christl, Manfred (1981). “Benzvalene—Properties and Synthetic Potential”. Angewandte Chemie International Edition in English 20 (67): 529–546. doi:10.1002/anie.198105291. ISSN 0570-0833.
- ^ Katz, Thomas J.; Wang, E. Jang; Acton, Nancy (1971). “Benzvalene synthesis”. Journal of the American Chemical Society 93 (15): 3782–3783. doi:10.1021/ja00744a045. ISSN 0002-7863.
- ^ Katz, Thomas J.; Roth, Ronald J.; Acton, Nancy; Carnahan, Eileen Jang (1999). “Synthesis of Benzvalene†”. The Journal of Organic Chemistry 64 (20): 7663–7664. doi:10.1021/jo990883g. ISSN 0022-3263.
- ^ Rearrangements and interconversions of compounds of the formula (CH)n Lawrence T. Scott, Maitland. Jones Chem. Rev., 1972, 72 (2), pp 181-202 doi:10.1021/cr60276a004
- ^ Swager, Timothy M.; Dougherty, Dennis A.; Grubbs, Robert H. (1988). “Strained rings as a source of unsaturation: polybenzvalene, a new soluble polyacetylene precursor”. Journal of the American Chemical Society 110 (9): 2973–2974. doi:10.1021/ja00217a049. ISSN 0002-7863.
