ホースラディッシュペルオキシダーゼ
| Horseradish peroxidase | |||||||
|---|---|---|---|---|---|---|---|
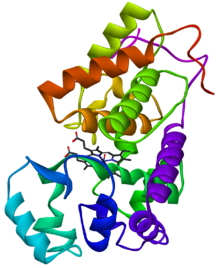 Horseradish peroxidase C1[1] | |||||||
| 識別子 | |||||||
| 由来生物 | |||||||
| 3文字略号 | Peroxidase C1A | ||||||
| 代替略号 | PRXC1A | ||||||
| PDB | 1W4W More structures | ||||||
| UniProt | P00433 | ||||||
| 他データ | |||||||
| EC番号 | 1.11.1.7 | ||||||
| |||||||
ホースラディッシュペルオキシダーゼ (Horseradish peroxidase, HRP) はホースラディッシュの根から見つかった酵素であり、生物化学の分野で良く用いられている。西洋わさびの根から 15 種類のペルオキシダーゼアイソザイムが単離されており、主に等電点を用いて分類されるが、もっとも一般的なものはCタイプ (中性) である。また、補因子としてヘム鉄を配位するヘムタンパク質である。過酸化水素を電子供与体として基質の酸化を触媒するが、他にも様々な化合物を電子供与体とすることが可能である。
構造
[編集]1997に初めてX線結晶構造解析により立体構造が決定され、[2] それ以後も様々な基質との相互作用による構造変化が決定されている。[3] 巨大なαヘリックスを有する糖タンパク質であり、補因子としてヘム鉄を配位している。
基質
[編集]HRP酵素またはそのコンジュゲートが基質とする過酸化水素などは、単独ではほとんど吸光が無いためその反応を分光光度計で測定する事は難しい。従って、HRPによって還元される事で検出可能な発色を示す色素を用いることで、その反応を可視化する必要がある。[4][5]
HRPの基質は、HRPの生化学的な特徴を活用するために数多く報告され、商品化されている。これらの基質はいくつかの異なるカテゴリーに分類される。HRPは発色基質 (TMB、DAB、ABTSなど) の発色生成物への変換を触媒し、化学発光基質 (ルミノールによる化学発光増強など) に作用する事で光を発生する。[要出典]

応用
[編集]HRPは、標識分子を結合できる6つのリジン残基を持つ44,173.9ダルトンの糖タンパク質である。適切な基質と反応させると、標識分子の発色、蛍光、[6]または発光誘導体を生成し、検出と定量が可能になる。HRPはしばしばコンジュゲート(遺伝的または化学的に結合した分子)中で使用され、標的物質の存在を判定及び定量するために使用される。例えば、ウエスタンブロットで少量の特定タンパク質を検出するために、HRPと結合した抗体を使用することがある。この場合、抗体部分が目的のタンパク質に特異的に結合した後、HRP部分によって基質が還元されることにより、検出可能なシグナルを生成する。[7]HRPは、その単量体の性質と発色生成物の生成のしやすさから、ELISAや免疫組織化学などの技術でも一般的に使用されている。ヘム含有酸化還元酵素であるペルオキシダーゼは、電子供与体によって過酸化水素の還元的開裂を触媒する商業的に重要な酵素である。
HRPは、アルカリホスファターゼのような他の一般的な代替品よりも分子量が小さいため安定性が高く、安価であることから、分子標識としての用途には多くの点で理想的である。また、反応速度が速いので、比較的短時間で強いシグナルを発生させることができる。[8] 高濃度のリン酸はHRPの安定性を著しく低下させる。生物医学的応用に加えて、HRPは重要な環境分野にも応用可能な酵素の一つである。この酵素は、様々な工業廃水中の主要汚染物質と考えられているヒドロキシル化芳香族化合物(HAC)の除去に適している。 [9]
さらに、HRPによって神経細胞を標識する技術は、近年、重要な手法になっている。新しい手法であるが、この方法はおそらく、1870年の発見以来、ゴルジ染色を使用した神経生物学者よりも多くの神経生物学者に使用されているとも言われる。[10]
増強化学発光(ECL)
[編集]HRPは、ルミノールからいくつかの中間体を経て3-アミノフタレートへの酸化反応を触媒する。この反応は428 nmの低強度の発光を伴う。しかし、ある種の化学物質の存在下では、放出される光が1000倍まで増強され、光を検出しやすくなり、反応の感度が高まる。発光の増強は増強化学発光(ECL)と呼ばれる。一般に知られている修飾フェノール(主にヨードフェノール)など、いくつかの増強剤が利用される。しかし、他の発光増強剤を使用したいくつかの基質が市販されており、その結果、発光シグナルはフェノール増強基質の最大13倍となる。[11] 光の強さは、反応している酵素分子の数と比例し、したがって基質との結合量と比例する。ECLは準備が簡単で、感度が高く、サザンブロットでは約0.5 pg、ノーザンブロットでは約0.5 pgの核酸を検出する。化学発光基質による検出には、発色基質と比較していくつかの利点がある。感度は10倍から100倍高く、広いダイナミックレンジで発光の定量が可能である。一方で、発色沈殿物の感度のダイナミックレンジは1桁程度である。化学発光基質を使用する場合、標識の除去ははるかに容易である。[要出典]
HRPミミック
[編集]天然のHRPを模倣するために、多くの材料が研究されてきた。例えば、酸化鉄ナノ粒子やヘミンを含む複合体がHRPの模倣に用いられてきた。[12] これらのHRP様人工酵素は、バイオマーカーの検出や腫瘍の免疫染色から生物の付着防止まで、多くの用途に用いられてきた。
関連項目
[編集]脚注
[編集]- ^ PDB: 1w4w; “Complexes of horseradish peroxidase with formate, acetate, and carbon monoxide”. Biochemistry 44 (2): 635–42. (January 2005). doi:10.1021/bi0483211. PMID 15641789.
- ^ PDB: 1ATJ; “Crystal structure of horseradish peroxidase C at 2.15 A resolution”. Nature Structural Biology 4 (12): 1032–8. (December 1997). doi:10.1038/nsb1297-1032. PMID 9406554.
- ^ “Peroxidase C1A Related PDB sequences”. UniPDB. European Bioinformatics Institute. 2023年11月10日閲覧。
- ^ “Horseradish peroxidase: a modern view of a classic enzyme”. Phytochemistry 65 (3): 249–59. (February 2004). doi:10.1016/j.phytochem.2003.10.022. PMID 14751298.
- ^ “Synthesis and characterization of polymers produced by horseradish peroxidase in dioxane”. Journal of Polymer Science 29 (11): 1561–74. (October 1991). Bibcode: 1991JPoSA..29.1561A. doi:10.1002/pola.1991.080291105.
- ^ “A fluorescent peroxidase probe increases the sensitivity of commercial ELISAs by two orders of magnitude”. Chem Commun 49 (88): 10379–10381. (2013). doi:10.1039/c3cc44783a. PMC 4011665. PMID 24071916.
- ^ “Investigation of the blood-ganglion barrier properties in rat sympathetic ganglia by using lanthanum ion and horseradish peroxidase as tracers”. Acta Anatomica 153 (2): 135–44. (1995). doi:10.1159/000313647. PMID 8560966.
- ^ “Comparison of horseradish peroxidase and alkaline phosphatase-labelled antibodies in enzyme immunoassays”. Annals of Clinical Biochemistry 24 ( Pt 2) (2): 145–52. (March 1987). doi:10.1177/000456328702400204. PMID 3035992.
- ^ “Optimization of peroxidase-catalyzed oxidative coupling process for phenol removal from wastewater using response surface methodology”. Environmental Science & Technology 41 (20): 7073–9. (October 2007). Bibcode: 2007EnST...41.7073G. doi:10.1021/es070626q. PMID 17993150.
- ^ “Cell marking with horseradish peroxidase”. Principles of neural development. Sunderland, Mass: Sinauer Associates. (1985). p. 114. ISBN 978-0-87893-744-8
- ^ High Intensity HRP-Chemiluminescence ELISA Substrate Archived 2016-04-08 at the Wayback Machine..
- ^ “Nanomaterials with enzyme-like characteristics (nanozymes): next-generation artificial enzymes”. Chemical Society Reviews 42 (14): 6060–93. (July 2013). doi:10.1039/C3CS35486E. PMID 23740388.
