「リステリア・モノサイトゲネス」の版間の差分
→分類: 斜体の修正 タグ: モバイル編集 モバイルウェブ編集 |
|||
| 14行目: | 14行目: | ||
}} |
}} |
||
'''リステリア・モノサイトゲネス'''('''''Listeria monocytogenes''''')とは、[[真正細菌]]の[[種 (分類学)|種]]の1つである。名前は[[:w:Joseph Lister, 1st Baron Lister|Joseph Lister]]の姓に由来する。食品媒介性病原細菌の1種であり、[[リステリア症]]の病原菌として知られている。その非常に高い病原性は、宿主の生体防御機構の第一線となる[[食細胞]]による殺菌を免れるエスケープ機構を有することによると考えられている。レジオネラ菌、サルモネラ菌、ブルセラ菌などと同じく、[[マクロファージ]]に貪食されても殺菌されずに生存し、さらに増殖する細菌([[細胞内寄生性細菌]])である<ref>{{Cite journal|和書|last=光山|author=|first=正雄|year=1997|title=リステリアのエスケープ機構と感染宿主応答|journal=日本細菌学雑誌|volume=52|issue=3|page=593-600| |
'''リステリア・モノサイトゲネス'''('''''Listeria monocytogenes''''')とは、[[真正細菌]]の[[種 (分類学)|種]]の1つである。名前は[[:w:Joseph Lister, 1st Baron Lister|Joseph Lister]]の姓に由来する。食品媒介性病原細菌の1種であり、[[リステリア症]]の病原菌として知られている。その非常に高い病原性は、宿主の生体防御機構の第一線となる[[食細胞]]による殺菌を免れるエスケープ機構を有することによると考えられている。レジオネラ菌、サルモネラ菌、ブルセラ菌などと同じく、[[マクロファージ]]に貪食されても殺菌されずに生存し、さらに増殖する細菌([[細胞内寄生性細菌]])である<ref>{{Cite journal|和書|last=光山|author=|first=正雄|year=1997|title=リステリアのエスケープ機構と感染宿主応答|journal=日本細菌学雑誌|volume=52|issue=3|page=593-600|doi=10.3412/jsb.52.593}}</ref>。 |
||
== 特徴 == |
== 特徴 == |
||
| 22行目: | 22行目: | ||
== 分類 == |
== 分類 == |
||
リステリア属(''Listeria''属)は、''Bacillus''属や''Staphylococcus''属と同じ、バシラス綱バシラス目に属する。リステリア属には現在、リステリア・モノサイトゲネスを含む10種、''L. fleischmannii''、''L. grayi''、''L. innocua''、''L. ivanovii''、''L. marthii''、''L. rocourtiae''、''L. seeligeri''、''L. weihenstephanensis''および''L. welshimeri''が含まれる。なお、かつて''L. denitrificans''もリステリア属に含まれていたが、現在は''[[:w:Jonesia|Jonesia]]''属に再分類された<ref name="collins">{{cite journal|author=M. D. Collins, S. Wallbanks, D. J. Lane, J. Shah, R. Nietupskin, J. Smida, M. Dorsch and E. Stackebrandt |title=Phylogenetic Analysis of the Genus ''Listeria'' Based on Reverse Transcriptase Sequencing of 16S rRNA |journal=International Journal of Systematic and Evolutionary Microbiology. |date=April 1991 |volume=41 |issue=2 |pages=240–246 | |
リステリア属(''Listeria''属)は、''Bacillus''属や''Staphylococcus''属と同じ、バシラス綱バシラス目に属する。リステリア属には現在、リステリア・モノサイトゲネスを含む10種、''L. fleischmannii''、''L. grayi''、''L. innocua''、''L. ivanovii''、''L. marthii''、''L. rocourtiae''、''L. seeligeri''、''L. weihenstephanensis''および''L. welshimeri''が含まれる。なお、かつて''L. denitrificans''もリステリア属に含まれていたが、現在は''[[:w:Jonesia|Jonesia]]''属に再分類された<ref name="collins">{{cite journal|author=M. D. Collins, S. Wallbanks, D. J. Lane, J. Shah, R. Nietupskin, J. Smida, M. Dorsch and E. Stackebrandt |title=Phylogenetic Analysis of the Genus ''Listeria'' Based on Reverse Transcriptase Sequencing of 16S rRNA |journal=International Journal of Systematic and Evolutionary Microbiology. |date=April 1991 |volume=41 |issue=2 |pages=240–246 |pmid=1713054 |doi=10.1099/00207713-41-2-240}}</ref>。リステリア・モノサイトゲネスの他に ''L. ivanovii'' もマウスに対して病原性を示すが、こちらはヒトへの感染症は引き起こさない<ref>Seafood HACCP Alliance (2007). [http://seafood.ucdavis.edu/haccp/compendium/chapt15.htm "Compendium of Fish and Fishery Product Processes, Hazards, and Controls, Chapter 15: ''Listeria monocytogenes''".] {{webarchive|url=https://web.archive.org/web/20090623093037/http://seafood.ucdavis.edu/HACCP/Compendium/Chapt15.htm|date=2009-06-23}} Seafood Network Information Center. Retrieved January 28, 2009.</ref>。'ステリア・モノサイトゲネスには病原性のある13の血清型が知られているが、ヒトから単離されるものの90%以上は3つの血清型1/2a、1/2b、および4bのみである。血清型4b株は世界中のリステリア症発症の33%から35%を占め、1980年代以降のヨーロッパと北米での食中毒の大規模流行の原因となっている<ref>{{cite journal|last1=Ward|first1=T. J.|last2=Gorski|first2=L.|last3=Borucki|first3=M. K.|last4=Mandrell|first4=R. E.|last5=Hutchins|first5=J.|last6=Pupedis|first6=K.|year=2004|title=Intraspecific Phylogeny and Lineage Group Identification Based on the prfA Virulence Gene Cluster of Listeria monocytogenes|journal=Journal of Bacteriology|volume=186|issue=15|pages=4994–5002|doi=10.1128/JB.186.15.4994-5002.2004|pmid=15262937|pmc=451661}}</ref>。 |
||
== 歴史 == |
== 歴史 == |
||
| 43行目: | 43行目: | ||
''リステリア・モノサイトゲネス''はヒトの脳、脊髄膜、および/または血流に感染する<ref>{{Cite web|url=https://www.health.ny.gov/diseases/communicable/listeriosis/fact_sheet.htm|title=Listeriosis (Listeria infection)|accessdate=2015-11-16|website=www.health.ny.gov}}</ref>。感染経路には、低温殺菌されていない乳製品や未加工食品がある<ref>{{Cite web|url=https://www.cdc.gov/listeria/sources.html|title=CDC - Sources - Listeriosis|accessdate=2015-11-16|website=www.cdc.gov}}</ref>。 |
''リステリア・モノサイトゲネス''はヒトの脳、脊髄膜、および/または血流に感染する<ref>{{Cite web|url=https://www.health.ny.gov/diseases/communicable/listeriosis/fact_sheet.htm|title=Listeriosis (Listeria infection)|accessdate=2015-11-16|website=www.health.ny.gov}}</ref>。感染経路には、低温殺菌されていない乳製品や未加工食品がある<ref>{{Cite web|url=https://www.cdc.gov/listeria/sources.html|title=CDC - Sources - Listeriosis|accessdate=2015-11-16|website=www.cdc.gov}}</ref>。 |
||
''リステリア・モノサイトゲネス''による侵襲性感染はリステリア症と呼ばれる。感染が侵襲性でない場合は熱性胃腸炎となる。リステリア症の症状としては、敗血症、および、妊娠中の子宮内または子宮頸部感染が含まれる敗血症<ref name="Gray_1966">{{cite journal|year=1966|title=Listeria monocytogenes and listeric infection|url=|journal=Bacteriol. Rev.|volume=30|issue=|pages=309–382|author1=Gray M. L.|author2=Killinger A. H.| |
''リステリア・モノサイトゲネス''による侵襲性感染はリステリア症と呼ばれる。感染が侵襲性でない場合は熱性胃腸炎となる。リステリア症の症状としては、敗血症、および、妊娠中の子宮内または子宮頸部感染が含まれる敗血症<ref name="Gray_1966">{{cite journal|year=1966|title=Listeria monocytogenes and listeric infection|url=|journal=Bacteriol. Rev.|volume=30|issue=|pages=309–382|author1=Gray M. L.|author2=Killinger A. H.|pmc=440999 |pmid=4956900}}</ref>、髄膜炎(または髄膜脳炎)<ref name="Gray_1966" />、脳炎<ref name="Armstrong1993">{{cite journal|year=1993|title=Brainstem encephalitis (Rhombencephalitis) due to Listeria monocytogenes: case report and review|url=|journal=Clin. Infect. Dis.|volume=16|issue=5|pages=689–702|doi=10.1093/clind/16.5.689|pmid=8507761|author1=Armstrong R. W.|author2=Fung P. C.}}</ref>、角膜潰瘍<ref name="Holland_1987">{{cite journal|year=1987|title=Corneal ulcer due to Listeria monocytogenes|url=|journal=Cornea|volume=6|issue=2|pages=144–146|doi=10.1097/00003226-198706020-00008|pmid=3608514|author1=Holland S.|author2=Alfonso E.|author3=Heidegger D.|author4=Mendelsohn A.|author5=Ullman S.|author6=Miller D.}}</ref>、肺炎<ref name="whitelock_1989">{{cite journal|year=1989|title=Listeria pneumonia. A case report|url=|journal=South African Medical Journal|volume=75|issue=4|pages=188–189|pmid=2919343|author1=Whitelock-Jones L.|author2=Carswell J.|author3=Rassmussen K. C.}}</ref>、および妊娠中の女性の子宮内または子宮頸部感染などがある。これらの症状は自然流産や死産の原因となる。妊娠中にリステリア症になった女性から生まれた子供は[[敗血性乳児肉芽腫症]]を発症して全身に化膿性肉芽腫が生じ、身体的な発育障害が起こる危険がある。上記の症状の前段階として、インフルエンザのような持続的な発熱が起こる。吐き気、嘔吐、下痢などの胃腸症状は、より深刻なリステリア症の前段階であることがある。制酸薬かシメチジンの使用はこれら胃腸症状と関連することが医学的に知られている。深刻な場合のリステリア症の潜伏期間は不明であるが、数日から3週間だと考えられている。胃腸症状の潜伏期間についても正確には不明であるが、12時間以上経った後だと見られている。初期の研究では、''リステリア・モノサイトゲネス''は[[エンドトキシン]]として機能するリポ多糖を有する、グラム陽性菌としては特殊な細菌だとみなされていた<ref name="Wexler_1979">{{cite journal|year=1979|title=Isolation, characterization, and biological properties of an endotoxin-like material from the gram-positive organism Listeria monocytogenes|url=|journal=Infection and Immunity|volume=23|issue=3|pages=845–857|pmid=110684|pmc=414241|author1=Wexler H.|author2=Oppenheim J. D.}}</ref>。しかし、後の研究で''リステリア・モノサイトゲネス''が持つリポ多糖はエンドトキシンではないことが明らかとなった。リステリア属の細胞壁は、ガラクトシル・グルコシル・ジグリセルドなどの、末端のリン酸モノエステルで繋がった糖脂質部分を含んだリポタイコ酸を有する。この資質領域がポリマー鎖を宿主の細胞膜に固定する。このリポタイコ酸は、グラム陰性菌のリポ多糖類に似ており、細胞表面唯一の両親媒性ポリマーである<ref>{{cite journal|last1=Fiedler|first1=F|year=1988|title=Biochemistry of the cell surface of Listeria strains: a locating general view|journal=Infection|volume=16 Suppl 2|issue=S2|pages=S92–7|doi=10.1007/BF01639729|pmid=3417357}}</ref><ref>{{cite journal|last1=Farber|first1=JM|last2=Peterkin|first2=PI|year=1991|title=Listeria monocytogenes, a food-borne pathogen|journal=Microbiological Reviews|volume=55|issue=3|pages=476–511|pmid=1943998|pmc=372831}}</ref>。 |
||
''リステリア・モノサイトゲネス''は宿主の腸管粘膜の[[M細胞]]や[[パイエル板]]のD-[[ガラクトース]]受容体に結合できるようにD-ガラクトース残基を細胞表面に有する。宿主のD-ガラクトース受容体に結合した時、この細菌は腸管粘膜を通過して宿主体内に侵入することができる。 |
''リステリア・モノサイトゲネス''は宿主の腸管粘膜の[[M細胞]]や[[パイエル板]]のD-[[ガラクトース]]受容体に結合できるようにD-ガラクトース残基を細胞表面に有する。宿主のD-ガラクトース受容体に結合した時、この細菌は腸管粘膜を通過して宿主体内に侵入することができる。 |
||
| 61行目: | 61行目: | ||
''リステリア・モノサイトゲネス''の病原性の高さは、宿主の食細胞による殺菌から免れるエスケープ機構を有する点による。通常、マクロファージに貪食された細菌は、食胞内で各種活性酸素に暴露され、次いで、食胞膜がリソソーム顆粒膜と融合(食胞-リソソーム融合、P-L融合)してアズール顆粒から種々の殺菌性タンパク質が供給され、殺菌される。''リステリア・モノサイトゲネス''は多くの細胞内寄生菌と同じく、[[カタラーゼ]]や[[スーパーオキシドディスムターゼ]](SOD)といった[[フリーラジカル]]消去酵素活性が高いため、食胞内での活性酸素に対する抵抗力を持つ。食胞-リソソーム融合後の殺菌性タンパク質に抵抗することは困難であるため、多くの細胞内寄生菌は食胞-リソソーム融合を阻害するが、''リステリア・モノサイトゲネス''の場合は融合が起こる前に食胞膜を傷害して小胞から細胞質へと脱出する。 |
''リステリア・モノサイトゲネス''の病原性の高さは、宿主の食細胞による殺菌から免れるエスケープ機構を有する点による。通常、マクロファージに貪食された細菌は、食胞内で各種活性酸素に暴露され、次いで、食胞膜がリソソーム顆粒膜と融合(食胞-リソソーム融合、P-L融合)してアズール顆粒から種々の殺菌性タンパク質が供給され、殺菌される。''リステリア・モノサイトゲネス''は多くの細胞内寄生菌と同じく、[[カタラーゼ]]や[[スーパーオキシドディスムターゼ]](SOD)といった[[フリーラジカル]]消去酵素活性が高いため、食胞内での活性酸素に対する抵抗力を持つ。食胞-リソソーム融合後の殺菌性タンパク質に抵抗することは困難であるため、多くの細胞内寄生菌は食胞-リソソーム融合を阻害するが、''リステリア・モノサイトゲネス''の場合は融合が起こる前に食胞膜を傷害して小胞から細胞質へと脱出する。 |
||
エスケープ機構を可能にする細菌因子について解明が進んでいる。''リステリア・モノサイトゲネス''に特徴的な溶血素のリステリオリシンO(LLO)遺伝子''hlyA''が欠失し、産生能が失われると、マクロファージ内増殖とマウスに対する致死的病原性が無くなる<ref>{{Cite journal|author=Domann E、Chakraborty T|year=|date=1989-08-11|title=Nucleotide sequence of the listeriolysin gene from a Listeria monocytogenes serotype 1/2a strain|journal=Nucleic acids research|volume=17|issue=15|page=6406| |
エスケープ機構を可能にする細菌因子について解明が進んでいる。''リステリア・モノサイトゲネス''に特徴的な溶血素のリステリオリシンO(LLO)遺伝子''hlyA''が欠失し、産生能が失われると、マクロファージ内増殖とマウスに対する致死的病原性が無くなる<ref>{{Cite journal|author=Domann E、Chakraborty T|year=|date=1989-08-11|title=Nucleotide sequence of the listeriolysin gene from a Listeria monocytogenes serotype 1/2a strain|journal=Nucleic acids research|volume=17|issue=15|page=6406|pmid=2505236|pmc=318305}}</ref>。''hlyA''の近傍には''prfA''、''plcA''、''mpl''、''actA''、''plcB''など病原性に関与する遺伝子群が存在する。これら遺伝子の完全なセットはリステリア属の中では、唯一ヒトに起病性を持つ''リステリア・モノサイトゲネス''以外には見つかっていない。また、これら遺伝子とは異なる部位の染色体DNA上に、細胞侵入性を規定する''inlA''、''inlB''、''iapなどの''遺伝子がある<ref>{{Cite journal|author=Portnoy DA, Chakraborty T, Goebel W, Cossart P|month=4|year=1992|title=Molecular determinants of Listeria monocytogenes pathogenesis|journal=Infection and immunity|volume=60|page=1263-7|pmid=1312514|pmc=256991}}</ref>。 |
||
''リステリア・モノサイトゲネス''の[[病原性因子]]を以下に述べる。 |
''リステリア・モノサイトゲネス''の[[病原性因子]]を以下に述べる。 |
||
* [[リステリオリシンO]](LLO)ー [[溶血素]]。1,587 [[塩基対|bp]]の''hlyA''にコードされ、529個のアミノ酸から成る分子量約58,000のタンパク質である。マクロファージに貪食されて食胞に取り込まれた際に、食胞膜を傷害して食胞から細胞質への脱出を導く。 |
* [[リステリオリシンO]](LLO)ー [[溶血素]]。1,587 [[塩基対|bp]]の''hlyA''にコードされ、529個のアミノ酸から成る分子量約58,000のタンパク質である。マクロファージに貪食されて食胞に取り込まれた際に、食胞膜を傷害して食胞から細胞質への脱出を導く。 |
||
* [[PI-PLC]] - hlyAの上流に位置する951 bpの''plcA''にコードされた分子量36,000の、[[ホスファチジルイノシトール]]を[[加水分解]][[基質]]とする[[ホスホリパーゼ|リン脂質加水分解酵素]]である。おそらく、食胞膜の構成成分であるホスファチジルイノシトールを分解してLLOと共同してエスケープに関与すると考えられている。''plcA''はリステリア属7菌種のうちでも病原性の''L. monocytogenes''と''L. ivanovii''にしか存在せず、またこの遺伝子を[[ノックアウトマウス|ノックアウト]]するとマウスに対する病原性は低下するため、''plcA''は細胞内寄生を可能にする病原性因子の1つとみなされている<ref>{{Cite journal|和書|author=Leimeister-Wächter M, Domann E, Chakraborty T|year=1991|title=Detection of a gene encoding a phosphatidylinositol-specific phospholipase C that is co-ordinately expressed with listeriolysin in Listeria monocytogenes|journal=Molecular microbiology|volume=5|issue=2|pages=361-366| |
* [[PI-PLC]] - hlyAの上流に位置する951 bpの''plcA''にコードされた分子量36,000の、[[ホスファチジルイノシトール]]を[[加水分解]][[基質]]とする[[ホスホリパーゼ|リン脂質加水分解酵素]]である。おそらく、食胞膜の構成成分であるホスファチジルイノシトールを分解してLLOと共同してエスケープに関与すると考えられている。''plcA''はリステリア属7菌種のうちでも病原性の''L. monocytogenes''と''L. ivanovii''にしか存在せず、またこの遺伝子を[[ノックアウトマウス|ノックアウト]]するとマウスに対する病原性は低下するため、''plcA''は細胞内寄生を可能にする病原性因子の1つとみなされている<ref>{{Cite journal|和書|author=Leimeister-Wächter M, Domann E, Chakraborty T|year=1991|title=Detection of a gene encoding a phosphatidylinositol-specific phospholipase C that is co-ordinately expressed with listeriolysin in Listeria monocytogenes|journal=Molecular microbiology|volume=5|issue=2|pages=361-366|pmid=1645838}}</ref>。 |
||
* [[金属プロテアーゼ]] ー ''mpl''遺伝子にコードされている。おそらく亜鉛プロテアーゼであり、PC-PLCの活性化や機能的成熟化に役割を果たすと考えられている。 |
* [[金属プロテアーゼ]] ー ''mpl''遺伝子にコードされている。おそらく亜鉛プロテアーゼであり、PC-PLCの活性化や機能的成熟化に役割を果たすと考えられている。 |
||
* [[レシチナーゼC]](PC-PLC)- plcB遺伝子をノックアウトすると、食胞からの脱出にはほとんど影響ないが、培養マクロファージの単層培養で細胞間感染の拡大が抑制される。隣接細胞へ伝播するために細胞質膜を分解するのに役立つと推測されている。 |
* [[レシチナーゼC]](PC-PLC)- plcB遺伝子をノックアウトすると、食胞からの脱出にはほとんど影響ないが、培養マクロファージの単層培養で細胞間感染の拡大が抑制される。隣接細胞へ伝播するために細胞質膜を分解するのに役立つと推測されている。 |
||
* [[ActA]] - ActAは''actA''遺伝子にコードされた610アミノ酸の分子量約9万のタンパク質である。ActAには[[プロリン]]を多く含んだ部位があり、この部位が宿主細胞質のVASPと結合すると細菌表面でのアクチンの重合を促す<ref>{{Cite journal|author=T Nishibori, H Xiong, I Kawamura, M Arakawa, and M Mitsuyama|month=8|year=1996|title=Induction of cytokine gene expression by listeriolysin O and roles of macrophages and NK cells|journal=Infection and Immunity|volume=64|issue=8|pages=3188–3195| |
* [[ActA]] - ActAは''actA''遺伝子にコードされた610アミノ酸の分子量約9万のタンパク質である。ActAには[[プロリン]]を多く含んだ部位があり、この部位が宿主細胞質のVASPと結合すると細菌表面でのアクチンの重合を促す<ref>{{Cite journal|author=T Nishibori, H Xiong, I Kawamura, M Arakawa, and M Mitsuyama|month=8|year=1996|title=Induction of cytokine gene expression by listeriolysin O and roles of macrophages and NK cells|journal=Infection and Immunity|volume=64|issue=8|pages=3188–3195|pmc=174206}}</ref>。重合体の成長に従って細菌細胞は前方へと押し出し、食胞を脱出した後に宿主細胞質内を移動して隣接細胞へと伝播する推進力とする<ref>{{Cite journal|author=Lasa I, David V, Gouin E, Marchand JB, Cossart P.|month=11|year=1995|title=The amino-terminal part of ActA is critical for the actin-based motility of Listeria monocytogenes; the central proline-rich region acts as a stimulator|journal=Molecular microbiology|volume=18|issue=3|page=|pages=425-436|pmid=8748027}}</ref>。 |
||
* ''[[prfA]]'' ー 上記の5つの病原性因子の上流に位置する遺伝子で、これら遺伝子の発現を一括して上方制御している。''prfA''産物(27 [[ダルトン|kDa]]、PrfA)は[[DNA結合タンパク質]]である。各遺伝子の[[プロモーター]]領域に結合して転写活性を高めると考えられている。''prfA''を欠失させると上記の遺伝子の全てが発現しなくなり、非病原性リステリア属細菌にはこの遺伝子は見いだされない。 |
* ''[[prfA]]'' ー 上記の5つの病原性因子の上流に位置する遺伝子で、これら遺伝子の発現を一括して上方制御している。''prfA''産物(27 [[ダルトン|kDa]]、PrfA)は[[DNA結合タンパク質]]である。各遺伝子の[[プロモーター]]領域に結合して転写活性を高めると考えられている。''prfA''を欠失させると上記の遺伝子の全てが発現しなくなり、非病原性リステリア属細菌にはこの遺伝子は見いだされない。 |
||
* [[インターナリン]] - 作用機構は不明だが、非貪食性上皮細胞への侵入性を決定するタンパク質と考えられている。インターナリンをコードするinlAまたはその下流の類似遺伝子inlBを欠失させた''リステリア・モノサイトゲネス''の変異株では、両方ともに腸管上皮細胞への侵入性が野生株の20%以下と低い。インターナリンファミリーには他にも遺伝子''inlC''、''inlD''、''inlE''、''inlF''が存在する。ただし、これら遺伝子の変異株では上皮細胞侵入性が変わらず、病原性因子かどうかは不明である<ref>{{Cite journal|author=Dramsi, S., Dehoux, P., Lebrun, M., Goossens, P. L., & Cossart, P.|month=5|year=1997|title=Identification of four new members of the internalin multigene family of Listeria monocytogenes EGD|journal=Infection and immunity|volume=65|issue=5|pages=1615-1625| |
* [[インターナリン]] - 作用機構は不明だが、非貪食性上皮細胞への侵入性を決定するタンパク質と考えられている。インターナリンをコードするinlAまたはその下流の類似遺伝子inlBを欠失させた''リステリア・モノサイトゲネス''の変異株では、両方ともに腸管上皮細胞への侵入性が野生株の20%以下と低い。インターナリンファミリーには他にも遺伝子''inlC''、''inlD''、''inlE''、''inlF''が存在する。ただし、これら遺伝子の変異株では上皮細胞侵入性が変わらず、病原性因子かどうかは不明である<ref>{{Cite journal|author=Dramsi, S., Dehoux, P., Lebrun, M., Goossens, P. L., & Cossart, P.|month=5|year=1997|title=Identification of four new members of the internalin multigene family of Listeria monocytogenes EGD|journal=Infection and immunity|volume=65|issue=5|pages=1615-1625|pmid=9125538|pmc=175184}}</ref>。 |
||
* ''iap'' - この遺伝子の産物は60 kDaの菌体表層タンパク質であり、[[ムレイン加水分解酵素]]として''リステリア・モノサイトゲネス''の短桿菌としての形態の維持に重要であると考えられている。感染マウスの脾細胞ではこのタンパク質の[[エピトープ]]を認識する細胞傷害性[[T細胞]]が誘導される<ref>{{Cite journal|author=Sujata Vijh & Eric G. Pamer|month=4|year=1997|title=Immunodominant and subdominant CTL responses to Listeria monocytogenes infection|journal=The Journal of Immunology|volume=158|issue=7|pages=3366-3371| |
* ''iap'' - この遺伝子の産物は60 kDaの菌体表層タンパク質であり、[[ムレイン加水分解酵素]]として''リステリア・モノサイトゲネス''の短桿菌としての形態の維持に重要であると考えられている。感染マウスの脾細胞ではこのタンパク質の[[エピトープ]]を認識する細胞傷害性[[T細胞]]が誘導される<ref>{{Cite journal|author=Sujata Vijh & Eric G. Pamer|month=4|year=1997|title=Immunodominant and subdominant CTL responses to Listeria monocytogenes infection|journal=The Journal of Immunology|volume=158|issue=7|pages=3366-3371|pmid=9120295}}</ref>。 |
||
以上のように、''リステリア・モノサイトゲネス''には細胞内寄生に関与する遺伝子が非常に多い。''リステリア・モノサイトゲネス''の病原性因子で最も重要なLLO遺伝子''hlyA''と強い相同性を有する遺伝子は、他のいくつかの病原性グラム陽性菌(''[[化膿レンサ球菌|Streptococcus pyogenes]]''、[[肺炎レンサ球菌|''S. pneumoniae'']]、''[[ウェルシュ菌|Clostridium perfringens]]''など)に存在するが、いずれも細胞内寄生性を示さない<ref>{{Cite journal|author=光山 正雄|month=3|year=1997|title=リステリアのエスケープ機構と感染宿主応答|journal=日本細菌学雑誌|volume=52|issue=3|pages=593-600| |
以上のように、''リステリア・モノサイトゲネス''には細胞内寄生に関与する遺伝子が非常に多い。''リステリア・モノサイトゲネス''の病原性因子で最も重要なLLO遺伝子''hlyA''と強い相同性を有する遺伝子は、他のいくつかの病原性グラム陽性菌(''[[化膿レンサ球菌|Streptococcus pyogenes]]''、[[肺炎レンサ球菌|''S. pneumoniae'']]、''[[ウェルシュ菌|Clostridium perfringens]]''など)に存在するが、いずれも細胞内寄生性を示さない<ref>{{Cite journal|author=光山 正雄|month=3|year=1997|title=リステリアのエスケープ機構と感染宿主応答|journal=日本細菌学雑誌|volume=52|issue=3|pages=593-600|doi=10.3412/jsb.52.593}}</ref>。この事実は、細胞内寄生は単一の遺伝子によって規定されるものではなく、多くの遺伝子の複合によって可能となるものであることを示唆する。 |
||
主に''リステリア・モノサイトゲネス''が感染を始める部位は宿主の腸上皮であり、ジッパー機構により非食細胞に侵入する。栄養素の取り込みは、[[インターナリン]](Inl)が宿主細胞接着因子であるE-[[カドヘリン]]または、肝細胞増殖因子受容体であるMet(c-Met)に結合することによって始まる。この結合は特定の[[RhoファミリーGタンパク質|Rho]]-[[GTPアーゼ]]を活性化させ、このRho-GTPアーゼはその後、[[ウィスコット・アルドリッチ症候群タンパク質]](WAsp)に結合して安定化させる。次いで、WAspは[[Arp2/3]]複合体に結合し、アクチン核形成点として働くことができる。その後のアクチン重合は、エンドサイトーシスの前に貪食細胞によって通常、異物の周囲に形成されるアクチンベースの構造体である「食細胞カップ」を作り出す。インターナリン結合の正味の効果は、宿主の接合形成装置を利用して細菌を内在化することである。リステリア・モノサイトゲネスは食細胞(例えば[[マクロファージ]])にも侵入することはできるが、非食細胞への侵入のためのインターナリンのみを必要とする。 |
主に''リステリア・モノサイトゲネス''が感染を始める部位は宿主の腸上皮であり、ジッパー機構により非食細胞に侵入する。栄養素の取り込みは、[[インターナリン]](Inl)が宿主細胞接着因子であるE-[[カドヘリン]]または、肝細胞増殖因子受容体であるMet(c-Met)に結合することによって始まる。この結合は特定の[[RhoファミリーGタンパク質|Rho]]-[[GTPアーゼ]]を活性化させ、このRho-GTPアーゼはその後、[[ウィスコット・アルドリッチ症候群タンパク質]](WAsp)に結合して安定化させる。次いで、WAspは[[Arp2/3]]複合体に結合し、アクチン核形成点として働くことができる。その後のアクチン重合は、エンドサイトーシスの前に貪食細胞によって通常、異物の周囲に形成されるアクチンベースの構造体である「食細胞カップ」を作り出す。インターナリン結合の正味の効果は、宿主の接合形成装置を利用して細菌を内在化することである。リステリア・モノサイトゲネスは食細胞(例えば[[マクロファージ]])にも侵入することはできるが、非食細胞への侵入のためのインターナリンのみを必要とする。 |
||
| 112行目: | 112行目: | ||
''リステリア・モノサイトゲネス''をいくつかのタイプのがんの[[免疫療法]]に利用することが研究されている<ref>{{Cite journal|last=Chu|first=Nina J.|last2=Armstrong|first2=Todd D.|last3=Jaffee|first3=Elizabeth M.|date=2015-04-01|title=Nonviral oncogenic antigens and the inflammatory signals driving early cancer development as targets for cancer immunoprevention|journal=Clinical Cancer Research|volume=21|issue=7|pages=1549–1557|doi=10.1158/1078-0432.CCR-14-1186|issn=1078-0432|pmid=25623216|pmc=4383709}}</ref><ref>{{Cite journal|last=Singh|first=Reshma|last2=Wallecha|first2=Anu|date=2011-05-01|title=Cancer immunotherapy using recombinant Listeria monocytogenes: transition from bench to clinic|journal=Human Vaccines|volume=7|issue=5|pages=497–505|doi=10.4161/hv.7.5.15132|issn=1554-8619|pmid=21422819}}</ref>。 |
''リステリア・モノサイトゲネス''をいくつかのタイプのがんの[[免疫療法]]に利用することが研究されている<ref>{{Cite journal|last=Chu|first=Nina J.|last2=Armstrong|first2=Todd D.|last3=Jaffee|first3=Elizabeth M.|date=2015-04-01|title=Nonviral oncogenic antigens and the inflammatory signals driving early cancer development as targets for cancer immunoprevention|journal=Clinical Cancer Research|volume=21|issue=7|pages=1549–1557|doi=10.1158/1078-0432.CCR-14-1186|issn=1078-0432|pmid=25623216|pmc=4383709}}</ref><ref>{{Cite journal|last=Singh|first=Reshma|last2=Wallecha|first2=Anu|date=2011-05-01|title=Cancer immunotherapy using recombinant Listeria monocytogenes: transition from bench to clinic|journal=Human Vaccines|volume=7|issue=5|pages=497–505|doi=10.4161/hv.7.5.15132|issn=1554-8619|pmid=21422819}}</ref>。 |
||
生きた弱毒化''リステリア・モノサイトゲネス''を使った癌ワクチンADXS11-001は、子宮頸癌の治療薬として開発中である<ref name="OBnews">{{cite journal|author=Fran Lowry|date=2008-05-15|title=Live Listeria Vaccine Proves Safe Against End-Stage Cervical Ca in Human Trial|journal=Ob. Gyn. News|volume=43|issue=10|page=2 | |
生きた弱毒化''リステリア・モノサイトゲネス''を使った癌ワクチンADXS11-001は、子宮頸癌の治療薬として開発中である<ref name="OBnews">{{cite journal|author=Fran Lowry|date=2008-05-15|title=Live Listeria Vaccine Proves Safe Against End-Stage Cervical Ca in Human Trial|journal=Ob. Gyn. News|volume=43|issue=10|page=2 |doi=10.1016/S0029-7437(08)70329-X}}</ref>。 |
||
== 脚注 == |
== 脚注 == |
||
2020年1月25日 (土) 17:32時点における版
| リステリア・モノサイトゲネス | |||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
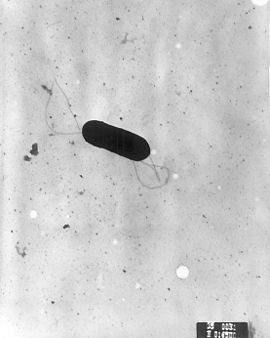 Listeria monocytogenesの電子顕微鏡写真
| |||||||||||||||||||||
| 分類 | |||||||||||||||||||||
| |||||||||||||||||||||
| 学名 | |||||||||||||||||||||
| Listeria monocytogenes (E. Murray et al. 1926) Pirie 1940 |
リステリア・モノサイトゲネス(Listeria monocytogenes)とは、真正細菌の種の1つである。名前はJoseph Listerの姓に由来する。食品媒介性病原細菌の1種であり、リステリア症の病原菌として知られている。その非常に高い病原性は、宿主の生体防御機構の第一線となる食細胞による殺菌を免れるエスケープ機構を有することによると考えられている。レジオネラ菌、サルモネラ菌、ブルセラ菌などと同じく、マクロファージに貪食されても殺菌されずに生存し、さらに増殖する細菌(細胞内寄生性細菌)である[1]。
特徴
リステリア・モノサイトゲネスはグラム陽性、非胞子形成性、通性嫌気性の桿菌である。カタラーゼ陽性かつオキシダーゼ陰性であり、赤血球を破壊するβ溶血素を発現する。運動性を有し、光学顕微鏡で見ると転倒運動するさまが観察できる[2] 。室温(20−25 °C)では周毛性鞭毛による活発な運動性を示すが、ヒト体温(37 °C)では鞭毛の合成をしなくなる[3]。30 °C以下で鞭毛による運動性を示し、37 °Cでは通常示さない[4]。他の食中毒菌と同様に加熱により死滅するが、4 °C以下の温度や12%食塩濃度下でも増殖する能力を持ち、一般的な冷蔵温度や塩漬け食品でも繁殖できる[5]。リステリア・モノサイトゲネスは、アクチンロケットと呼ばれる、爆発的なアクチン分子の重合によるアクチンポリマーにより真核生物の細胞内へと移動できる。
研究によると、ヒト胃腸管面積の10%でリステリア・モノサイトゲネスが存在することが示唆されている[6]。
分類
リステリア属(Listeria属)は、Bacillus属やStaphylococcus属と同じ、バシラス綱バシラス目に属する。リステリア属には現在、リステリア・モノサイトゲネスを含む10種、L. fleischmannii、L. grayi、L. innocua、L. ivanovii、L. marthii、L. rocourtiae、L. seeligeri、L. weihenstephanensisおよびL. welshimeriが含まれる。なお、かつてL. denitrificansもリステリア属に含まれていたが、現在はJonesia属に再分類された[7]。リステリア・モノサイトゲネスの他に L. ivanovii もマウスに対して病原性を示すが、こちらはヒトへの感染症は引き起こさない[8]。'ステリア・モノサイトゲネスには病原性のある13の血清型が知られているが、ヒトから単離されるものの90%以上は3つの血清型1/2a、1/2b、および4bのみである。血清型4b株は世界中のリステリア症発症の33%から35%を占め、1980年代以降のヨーロッパと北米での食中毒の大規模流行の原因となっている[9]。
歴史
リステリア・モノサイトゲネス(Listeria monocytogenes)は、1924年にE.G.D. Murrayが6匹の若い兎の突然死を調べる過程で初めて発見され、1926年に発表された[10]。Murrayはこの微生物をBacterium monocytogenesと名付けたが、1940年にHarvey Pirieによって属名はListeriaに変更された[11]。リステリア・モノサイトゲネスによる感染についての医学的な記述はヒトを含めた動物に発生していることが1920年代に現れた。しかし、1952年が東ドイツで報告されるまでは、新生児への感染、敗血症、髄膜炎の原因菌としては認識されていなかった[12]。成人への感染は、悪性腫瘍治療の際に用いられる抗がん剤などに伴う免疫抑制状態や、臓器移植後の拒絶反応を防ぐために投与される免疫抑制剤や、何らかの疾患によってステロイドホルモン剤の長期服用が行われた時に発生する免疫抑制状態や、HIV感染などによる免疫系の弱体化を原因とする[13]。
また1981年に食中毒原因菌であることが科学的に証明された。その契機となった事件は、カナダ東部のノバスコシア州ハリファックスでキャベツを感染源とするリステリア症の大流行であった。主に妊婦と新生児で41人が感染し、18人が死亡した。原因となったキャベツはリステリア・モノサイトゲネスに汚染された羊糞肥料で栽培されていた[14]。その後も、リステリア・モノサイトゲネスによる世界的で重大な食中毒が今日まで報告されている[15]。
病原性

危険性
リステリア・モノサイトゲネスは、食品媒介性細菌の中で非常に危険であり、かつ、毒性が高い細菌の1つとされる[6] 。日本では食中毒統計においてリステリア・モノサイトゲネスによる食中毒の報告例はないが、食品安全委員会の評価書によると、リステリア感染症の推定患者数は年間200人(平成23年)とされている[5]。アメリカ合衆においては、毎年、1,600件の感染症発生と260件の死亡の原因と推定されており、食品媒介性細菌の感染症による死亡件数のうち、サルモネラ菌とボツリヌス菌に次いでリステリア症を原因とするものが3番目に多い。アメリカ合衆国でのリステリア症の死亡率は、他の食品媒介性感染症よりも高い。また、EUでは2008年以降、リステリア症の発症件数が増加傾向にあり、2014年では2,161件の発症が確認されるとともに210件の死亡が報告され、これは2013年と比べて16%の増加にあたる[16][17]。
リステリア・モノサイトゲネスによる疾患はヒト以上に獣医学の分野で頻繁に発生しており、特に反芻動物における髄膜脳炎の原因菌として知られている。
新生児は経腟的に感染して髄膜炎を発症することがあり、新生児の髄膜炎において3番目に多い原因である。ブリーチーズやカマンベールチーズ、フェタチーズ、ケソブランコなどのソフトチーズはリステリア・モノサイトゲネスを含んでいる恐れがあり、妊婦は食さないよう指示されることがある[18]。
症状
リステリア・モノサイトゲネスはヒトの脳、脊髄膜、および/または血流に感染する[19]。感染経路には、低温殺菌されていない乳製品や未加工食品がある[20]。
リステリア・モノサイトゲネスによる侵襲性感染はリステリア症と呼ばれる。感染が侵襲性でない場合は熱性胃腸炎となる。リステリア症の症状としては、敗血症、および、妊娠中の子宮内または子宮頸部感染が含まれる敗血症[21]、髄膜炎(または髄膜脳炎)[21]、脳炎[22]、角膜潰瘍[23]、肺炎[24]、および妊娠中の女性の子宮内または子宮頸部感染などがある。これらの症状は自然流産や死産の原因となる。妊娠中にリステリア症になった女性から生まれた子供は敗血性乳児肉芽腫症を発症して全身に化膿性肉芽腫が生じ、身体的な発育障害が起こる危険がある。上記の症状の前段階として、インフルエンザのような持続的な発熱が起こる。吐き気、嘔吐、下痢などの胃腸症状は、より深刻なリステリア症の前段階であることがある。制酸薬かシメチジンの使用はこれら胃腸症状と関連することが医学的に知られている。深刻な場合のリステリア症の潜伏期間は不明であるが、数日から3週間だと考えられている。胃腸症状の潜伏期間についても正確には不明であるが、12時間以上経った後だと見られている。初期の研究では、リステリア・モノサイトゲネスはエンドトキシンとして機能するリポ多糖を有する、グラム陽性菌としては特殊な細菌だとみなされていた[25]。しかし、後の研究でリステリア・モノサイトゲネスが持つリポ多糖はエンドトキシンではないことが明らかとなった。リステリア属の細胞壁は、ガラクトシル・グルコシル・ジグリセルドなどの、末端のリン酸モノエステルで繋がった糖脂質部分を含んだリポタイコ酸を有する。この資質領域がポリマー鎖を宿主の細胞膜に固定する。このリポタイコ酸は、グラム陰性菌のリポ多糖類に似ており、細胞表面唯一の両親媒性ポリマーである[26][27]。
リステリア・モノサイトゲネスは宿主の腸管粘膜のM細胞やパイエル板のD-ガラクトース受容体に結合できるようにD-ガラクトース残基を細胞表面に有する。宿主のD-ガラクトース受容体に結合した時、この細菌は腸管粘膜を通過して宿主体内に侵入することができる。
リステリア・モノサイトゲネスによる感染症を発症させるのに必要な細菌数は、株や宿主の感受性によって異なる。健康な成人では非常に多くの菌数を摂取しなければ発症しないため、賞味期限や保存方法が守られていれば、食中毒が発生することはない[5]。しかし、感受性には個人差があり、殺菌されたと思われる牛乳からでもリステリア症に発症した事例があり、感受性の高い人では1,000個未満の細胞数でも感染する可能性がある。リステリア・モノサイトゲネスは胃腸上皮に侵入することもある。他の病原細菌と同様、宿主の単球、マクロファージ、多形核白球に侵入すると、血液を介して全身に感染することができるようになる。貪食細胞に入り込むと、脳へ感染したり、妊娠した女性なら経胎盤的に胎児に移行したりすることもある。リステリア・モノサイトゲネスの病原性の強さは、貪食細胞の内部で生育・増殖する能力による。この細菌は元々、腸膜へ侵入するように進化してきた。そのための化学的メカニズムにはインターナリン(internalin)InlA/InlBが関わり、この細菌性タンパク質は腸細胞膜のカドヘリンに結合し、ジッパー機構により細菌細胞を宿主細胞内に侵入することを可能にする。これらの接着分子はヒトの血液-脳間および胎盤-胎児間の障壁にも存在し、リステリア属細菌が髄膜炎や子宮内での胎児への感染を引き起こす理由である可能性が高い。リステリア属細菌はマクロファージなどの貪食細胞に取り込まれても、食胞の膜を破壊するコレストロール依存性細胞溶解素のリステリオリシンO(Listeriosin O)を活性化させて、食胞を破壊し細胞質に逃げ出すことによって、宿主の細胞質に侵入することが可能となる[28]。細胞内および細胞間での運動性はActAタンパク質(actin assembly-inducing protein)によって可能となる。このタンパク質は、本来は細胞骨格を重合させための宿主のアクチン重合機構を細菌細胞の加速に利用する。
感染経路
リステリア・モノサイトゲネスの感染方法は食品媒介であることが確定している。これまで感染元となったことが確認された食品には乳製品(生乳、低温殺菌飲料乳[29]、チーズ、特に軟質熟成タイプとナチュラルチーズ、アイスクリーム)、生野菜、食肉加工品(生ハムや、生肉を発酵させて作ったソーセージ)、あらゆる種類の生肉、魚介類加工品(スモークサーモンなど魚肉の燻製)、コールスローなどのサラダ[5]がある。日本国内では乳製品、食肉加工品や魚介類加工品などから非常に微量ながらリステリア・モノサイトゲネスが検出される[5]。通常の微生物の栄養摂取や増殖が抑えられる0 °C環境でも生育することができ、冷蔵食品であっても指数関数的に増殖する。4 °Cといった冷蔵環境では第二鉄の量が生育に影響を及ぼす可能性が示されている[30]。
感染事例
- 1981年、カナダ東部のノバスコシア州ハリファックスでコールスローを感染源とするリステリア症の大流行であった。主に妊婦と新生児で41人が感染、18人が死亡した。原因は、コールスローに使用されていたキャベツに与えられていた羊糞であった[14]。この事件により、リステリア・モノサイトゲネスが食品媒介性であることが証明された[31]。
- 2001年3月、北海道でリステリア・モノサイトゲネスによるナチュラルチーズの集団食中毒が発生した[32][33]。日本で食品由来の感染が確認されたのはこの件が初。
- 2015年3月、米国の有名酪農ブランドがアイスクリームを大量リコールした。米国食品医薬品局(FDA)の発表では、カンザス州の病院で同社のアイスクリームを食べた5名の患者がリステリア症の治療を受け、そのうち3名が死亡した[34]。
病原性機構
エスケープ機構
リステリア・モノサイトゲネスの病原性の高さは、宿主の食細胞による殺菌から免れるエスケープ機構を有する点による。通常、マクロファージに貪食された細菌は、食胞内で各種活性酸素に暴露され、次いで、食胞膜がリソソーム顆粒膜と融合(食胞-リソソーム融合、P-L融合)してアズール顆粒から種々の殺菌性タンパク質が供給され、殺菌される。リステリア・モノサイトゲネスは多くの細胞内寄生菌と同じく、カタラーゼやスーパーオキシドディスムターゼ(SOD)といったフリーラジカル消去酵素活性が高いため、食胞内での活性酸素に対する抵抗力を持つ。食胞-リソソーム融合後の殺菌性タンパク質に抵抗することは困難であるため、多くの細胞内寄生菌は食胞-リソソーム融合を阻害するが、リステリア・モノサイトゲネスの場合は融合が起こる前に食胞膜を傷害して小胞から細胞質へと脱出する。
エスケープ機構を可能にする細菌因子について解明が進んでいる。リステリア・モノサイトゲネスに特徴的な溶血素のリステリオリシンO(LLO)遺伝子hlyAが欠失し、産生能が失われると、マクロファージ内増殖とマウスに対する致死的病原性が無くなる[35]。hlyAの近傍にはprfA、plcA、mpl、actA、plcBなど病原性に関与する遺伝子群が存在する。これら遺伝子の完全なセットはリステリア属の中では、唯一ヒトに起病性を持つリステリア・モノサイトゲネス以外には見つかっていない。また、これら遺伝子とは異なる部位の染色体DNA上に、細胞侵入性を規定するinlA、inlB、iapなどの遺伝子がある[36]。
リステリア・モノサイトゲネスの病原性因子を以下に述べる。
- リステリオリシンO(LLO)ー 溶血素。1,587 bpのhlyAにコードされ、529個のアミノ酸から成る分子量約58,000のタンパク質である。マクロファージに貪食されて食胞に取り込まれた際に、食胞膜を傷害して食胞から細胞質への脱出を導く。
- PI-PLC - hlyAの上流に位置する951 bpのplcAにコードされた分子量36,000の、ホスファチジルイノシトールを加水分解基質とするリン脂質加水分解酵素である。おそらく、食胞膜の構成成分であるホスファチジルイノシトールを分解してLLOと共同してエスケープに関与すると考えられている。plcAはリステリア属7菌種のうちでも病原性のL. monocytogenesとL. ivanoviiにしか存在せず、またこの遺伝子をノックアウトするとマウスに対する病原性は低下するため、plcAは細胞内寄生を可能にする病原性因子の1つとみなされている[37]。
- 金属プロテアーゼ ー mpl遺伝子にコードされている。おそらく亜鉛プロテアーゼであり、PC-PLCの活性化や機能的成熟化に役割を果たすと考えられている。
- レシチナーゼC(PC-PLC)- plcB遺伝子をノックアウトすると、食胞からの脱出にはほとんど影響ないが、培養マクロファージの単層培養で細胞間感染の拡大が抑制される。隣接細胞へ伝播するために細胞質膜を分解するのに役立つと推測されている。
- ActA - ActAはactA遺伝子にコードされた610アミノ酸の分子量約9万のタンパク質である。ActAにはプロリンを多く含んだ部位があり、この部位が宿主細胞質のVASPと結合すると細菌表面でのアクチンの重合を促す[38]。重合体の成長に従って細菌細胞は前方へと押し出し、食胞を脱出した後に宿主細胞質内を移動して隣接細胞へと伝播する推進力とする[39]。
- prfA ー 上記の5つの病原性因子の上流に位置する遺伝子で、これら遺伝子の発現を一括して上方制御している。prfA産物(27 kDa、PrfA)はDNA結合タンパク質である。各遺伝子のプロモーター領域に結合して転写活性を高めると考えられている。prfAを欠失させると上記の遺伝子の全てが発現しなくなり、非病原性リステリア属細菌にはこの遺伝子は見いだされない。
- インターナリン - 作用機構は不明だが、非貪食性上皮細胞への侵入性を決定するタンパク質と考えられている。インターナリンをコードするinlAまたはその下流の類似遺伝子inlBを欠失させたリステリア・モノサイトゲネスの変異株では、両方ともに腸管上皮細胞への侵入性が野生株の20%以下と低い。インターナリンファミリーには他にも遺伝子inlC、inlD、inlE、inlFが存在する。ただし、これら遺伝子の変異株では上皮細胞侵入性が変わらず、病原性因子かどうかは不明である[40]。
- iap - この遺伝子の産物は60 kDaの菌体表層タンパク質であり、ムレイン加水分解酵素としてリステリア・モノサイトゲネスの短桿菌としての形態の維持に重要であると考えられている。感染マウスの脾細胞ではこのタンパク質のエピトープを認識する細胞傷害性T細胞が誘導される[41]。
以上のように、リステリア・モノサイトゲネスには細胞内寄生に関与する遺伝子が非常に多い。リステリア・モノサイトゲネスの病原性因子で最も重要なLLO遺伝子hlyAと強い相同性を有する遺伝子は、他のいくつかの病原性グラム陽性菌(Streptococcus pyogenes、S. pneumoniae、Clostridium perfringensなど)に存在するが、いずれも細胞内寄生性を示さない[42]。この事実は、細胞内寄生は単一の遺伝子によって規定されるものではなく、多くの遺伝子の複合によって可能となるものであることを示唆する。
主にリステリア・モノサイトゲネスが感染を始める部位は宿主の腸上皮であり、ジッパー機構により非食細胞に侵入する。栄養素の取り込みは、インターナリン(Inl)が宿主細胞接着因子であるE-カドヘリンまたは、肝細胞増殖因子受容体であるMet(c-Met)に結合することによって始まる。この結合は特定のRho-GTPアーゼを活性化させ、このRho-GTPアーゼはその後、ウィスコット・アルドリッチ症候群タンパク質(WAsp)に結合して安定化させる。次いで、WAspはArp2/3複合体に結合し、アクチン核形成点として働くことができる。その後のアクチン重合は、エンドサイトーシスの前に貪食細胞によって通常、異物の周囲に形成されるアクチンベースの構造体である「食細胞カップ」を作り出す。インターナリン結合の正味の効果は、宿主の接合形成装置を利用して細菌を内在化することである。リステリア・モノサイトゲネスは食細胞(例えばマクロファージ)にも侵入することはできるが、非食細胞への侵入のためのインターナリンのみを必要とする。
細菌は細胞内に移行後、リソソームに取り込まれる前に液胞やファゴソームから逃れなければならない。この回避を可能にするのは主に3つの病原性毒性因子であり、リステリオリシンO(LLO、hly遺伝子にコードされる)、ホスホリパーゼA(plcA遺伝子にコードされる)、ホスホリパーゼB(plcB遺伝子にコードされる)である[43][44]。LLOとPlcAの分泌は、液胞膜を破壊し、細菌が細胞質に逃げることを可能にする。
細胞質に入ってからリステリア・モノサイトゲネスは宿主のアクチンを2回利用する。ActAタンパク質は古い方の細胞極(リステリア・モノサイトゲネスには細胞の中央に中隔があり、したがって1つの細胞に古い細胞極と新しい細胞極がある)と関連し、Arp2/3複合体に結合し、それによって細菌細胞表面の特定領域にアクチン核形成を誘導する。そして、アクチン重合は細菌細胞を宿主細胞膜中へと一方向的に推進させる。形成された突出部は隣接細胞の内部に取り込まれ、二重膜液胞を形成する。この液胞からは前述のようにLLOとPlcBを使用して脱出する。この直接的な細胞間拡散の様式には、paracytophagyとして知られる細胞機構が関与する[45]。
病原性の制御
リステリア・モノサイトゲネスが病原菌あるいは腐生菌として振舞うかどうかは環境によって決まる。宿主体内に存在する時、クオラムセンシングがいくつかの病原遺伝子は上方制御するよう働く。宿主生物内での位置に依存して、上方制御をする活性化因子は変わる。腸内ではシグマ因子の1つSigBが、血液内ではPrfAがVir 遺伝子を上方制御する[46][47][48][49]。病原菌となるか腐生菌となるかを切り替える機構についてはあまり明らかになっていないが、切り替えにはいくつかの非翻訳RNAが必要である。
系統
リステリア・モノサイトゲネスには3つの系統があり、それぞれ進化の過程や病原性が異なる[50]。系統I株にはヒト由来の臨床分離株の大部分と、ヒトへの流行性クローンの全てが含まれているが、ヒト以外の動物由来の臨床分離株は多くない[50]。系統II株ではヒト以外の動物の臨床分離株が大きな比率を占め、ヒトの臨床分離株は少なく、環境中や食品にはより一般的に存在する[51]。系統III株は非常に稀であり、ヒト以外の動物由来のものが多い[50]。
規制
国際食品規格委員会は2007年から、食べる前に加熱を要さない生食用食品(Ready-to-eat食品:RTE食品)についてリステリア・モノサイトゲネスの基準値を設定した。日本では2014年12月25日から厚生労働省が非加熱食肉製品及びナチュラルチーズについて成分規格として基準値100 (cfu/g)以下を設定した[34]。
検出方法

リステリア・モノサイトゲネスの検出検出にはアントン試験(Anton test)が用いられる。ウサギかモルモットの結膜嚢に培養液を滴下すると、24時間以内に角結膜炎が観察される[52][53]。
リステリア種はミューラー・ヒントン寒天培地などの培地で生育する。 培地に羊血液を混ぜて初代培養を行うと、溶血によりコロニーの下か周囲に特徴的な外観変化が現れるため同定の精度が向上する。培地を植菌の数日前から4 °Cの環境に置くことは分離に役立つ。リステリア属は様々な有機酸を産生するが、ガスは発生させない[54]。リステリア属の溶血素産生性や室温での運動性はリステリア属とコリネ型細菌を区別するのに重要である。
食品からの検出には時間を要する。1990年9月に改訂された米国食品医薬品局(FDA)の方法では分析の前に24時間と48時間の濃縮を必要とする。同定までの総時間は5日から7日を要するが、特定の株に特異的な非放射性ラベルDNAプローブを用いればより簡便かつ迅速にその株かどうか確認することができる[55]。
治療
リステリアによる髄膜炎に罹患すると、全体の死亡率は70%、敗血症なら50%、周産期/新生児での感染なら80%以上に達することがある。 妊娠中の感染症では、母親の症状は軽いことが多く、通常は生存する。静脈注射によるペニシリンまたはアンピシリンによる治療成功の報告がある[56]。ペニシリンにアレルギーのある患者にはトリメトプリム-スルファメトキサゾールが有効である[56]。
感染制御
バクテリオファージのリステリアファージP100は、リステリア・モノサイトゲネスを制御するための食品添加物として提案されている[57]。バクテリオファージによる治療法は複数の会社で開発されている。米国食品医薬品局(FDA)は、Intralytix社のバクテリオファージ6種の混合物と、EBI Food Safety社がリステリア・モノサイトゲネスを殺すよう設計したファージ製品を承認した。用途には、スライスしたハムのような、販売形態のまま即席で食べることができる肉や果物にスプレーすることが想定されている[58]。
遺伝子導入ベクターとしての利用
いくつかの研究ではリステリア・モノサイトゲネスを、in vitroで遺伝子導入用のベクターとして利用することを検討している。成功例の1つとして、遺伝子導入による嚢胞性線維症の遺伝子治療がある[59]。
がん治療
リステリア・モノサイトゲネスをいくつかのタイプのがんの免疫療法に利用することが研究されている[60][61]。
生きた弱毒化リステリア・モノサイトゲネスを使った癌ワクチンADXS11-001は、子宮頸癌の治療薬として開発中である[62]。
脚注
- ^ 光山, 正雄「リステリアのエスケープ機構と感染宿主応答」『日本細菌学雑誌』第52巻第3号、1997年、593-600頁、doi:10.3412/jsb.52.593。
- ^ Farber, J. M.; Peterkin, P. I. (September 1991). “Listeria monocytogenes, a food-borne pathogen”. Microbiology and Molecular Biology Reviews 55 (3): 476–511. PMC 372831. PMID 1943998.
- ^ Todar, K. (2008). "Listeria monocytogenes". Todar's Online Textbook of Bacteriology. Retrieved January 28, 2009.
- ^ Gründling A.; Burrack L.S.; Bouwer H.G.A.; Higgins D.E. (2004). “Listeria monocytogenes regulates flagellar motility gene expression through MogR, a transcriptional repressor required for virulence”. Proc. Natl. Acad. Sci. U.S.A. 101 (33): 12316–12323. Bibcode: 2004PNAS..10112318G. doi:10.1073/pnas.0404924101. PMC 514476. PMID 15302931.
- ^ a b c d e “リステリアによる食中毒”. 厚生労働省. 2018年8月19日閲覧。
- ^ a b Ramaswamy V; Cresence VM; Rejitha JS; Lekshmi MU; Dharsana KS; Prasad SP; Vijila HM. (February 2007). “Journal of microbiology, immunology, and infection.” (PDF). J. Microbiol. Immunol. Infect. 40 (1): 4–13. PMID 17332901 2010年9月5日閲覧。.
- ^ M. D. Collins, S. Wallbanks, D. J. Lane, J. Shah, R. Nietupskin, J. Smida, M. Dorsch and E. Stackebrandt (April 1991). “Phylogenetic Analysis of the Genus Listeria Based on Reverse Transcriptase Sequencing of 16S rRNA”. International Journal of Systematic and Evolutionary Microbiology. 41 (2): 240–246. doi:10.1099/00207713-41-2-240. PMID 1713054.
- ^ Seafood HACCP Alliance (2007). "Compendium of Fish and Fishery Product Processes, Hazards, and Controls, Chapter 15: Listeria monocytogenes". Archived 2009-06-23 at the Wayback Machine. Seafood Network Information Center. Retrieved January 28, 2009.
- ^ Ward, T. J.; Gorski, L.; Borucki, M. K.; Mandrell, R. E.; Hutchins, J.; Pupedis, K. (2004). “Intraspecific Phylogeny and Lineage Group Identification Based on the prfA Virulence Gene Cluster of Listeria monocytogenes”. Journal of Bacteriology 186 (15): 4994–5002. doi:10.1128/JB.186.15.4994-5002.2004. PMC 451661. PMID 15262937.
- ^ Murray E.G.D.; Webb R.E.; Swann M.B.R. (1926). “A disease of rabbits characterized by a large mononuclear leucocytosis, caused by a hitherto undescribed bacillus Bacterium monocytogenes (n. sp.)”. J. Pathol. Bacteriol. 29: 407–439. doi:10.1002/path.1700290409.
- ^ Harvey P.J.H. (1940). “Listeria: change of name for a genus of bacteria”. Nature 145 (3668): 264. Bibcode: 1940Natur.145..264P. doi:10.1038/145264a0.
- ^ Potel, J. 1952. Zur Granulomatosis infantiseptica. Zentr. Bakteriol. I. Orig. 158: 329-331
- ^ Schlech W.F. III; Acheson, D. (2001). “Foodborne listeriosis”. Clin. Infect. Dis. 31 (3): 770–775. doi:10.1086/314008. PMID 11017828.
- ^ a b “Epidemic listeriosis--evidence for transmission by food”. N. Engl. J. Med. 308 (4): 203–6. (January 1983). doi:10.1056/NEJM198301273080407. PMID 6401354.
- ^ Ryser, E.T., Marth, E.H. (Eds.) 1999. Listeria, Listeriosis, and Food. Safety, 2nd edn. Marcel Dekker, New York.
- ^ “Campylobacter and Listeria infections still rising in the EU – say EFSA and ECDC - European Food Safety Authority”. www.efsa.europa.eu (2017年5月31日). 2018年7月31日閲覧。
- ^ https://efsa.onlinelibrary.wiley.com/doi/abs/10.2903/j.efsa.2015.4329
- ^ Genigeorgis C.; Carniciu M.; Dutulescu D.; Farver T.B. (1991). “Growth and survival of Listeria monocytogenes in market cheeses stored at 4 to 30 degrees C”. Journal of food protection 54 (9): 662–668. doi:10.4315/0362-028X-54.9.662.
- ^ “Listeriosis (Listeria infection)”. www.health.ny.gov. 2015年11月16日閲覧。
- ^ “CDC - Sources - Listeriosis”. www.cdc.gov. 2015年11月16日閲覧。
- ^ a b Gray M. L.; Killinger A. H. (1966). “Listeria monocytogenes and listeric infection”. Bacteriol. Rev. 30: 309–382. PMC 440999. PMID 4956900.
- ^ Armstrong R. W.; Fung P. C. (1993). “Brainstem encephalitis (Rhombencephalitis) due to Listeria monocytogenes: case report and review”. Clin. Infect. Dis. 16 (5): 689–702. doi:10.1093/clind/16.5.689. PMID 8507761.
- ^ Holland S.; Alfonso E.; Heidegger D.; Mendelsohn A.; Ullman S.; Miller D. (1987). “Corneal ulcer due to Listeria monocytogenes”. Cornea 6 (2): 144–146. doi:10.1097/00003226-198706020-00008. PMID 3608514.
- ^ Whitelock-Jones L.; Carswell J.; Rassmussen K. C. (1989). “Listeria pneumonia. A case report”. South African Medical Journal 75 (4): 188–189. PMID 2919343.
- ^ Wexler H.; Oppenheim J. D. (1979). “Isolation, characterization, and biological properties of an endotoxin-like material from the gram-positive organism Listeria monocytogenes”. Infection and Immunity 23 (3): 845–857. PMC 414241. PMID 110684.
- ^ Fiedler, F (1988). “Biochemistry of the cell surface of Listeria strains: a locating general view”. Infection 16 Suppl 2 (S2): S92–7. doi:10.1007/BF01639729. PMID 3417357.
- ^ Farber, JM; Peterkin, PI (1991). “Listeria monocytogenes, a food-borne pathogen”. Microbiological Reviews 55 (3): 476–511. PMC 372831. PMID 1943998.
- ^ Dramsi, Shaynoor; Cossart, Pascale (2002-03-18). “Listeriolysin O”. The Journal of Cell Biology 156 (6): 943–946. doi:10.1083/jcb.200202121. ISSN 0021-9525. PMC 2173465. PMID 11901162.
- ^ Fleming D. W.; Cochi S. L.; MacDonald K. L.; Brondum J.; Hayes P. S.; Plikaytis B. D.; Holmes M. B.; Audurier A. et al. (1985). “Pasteurized milk as a vehicle of infection in an outbreak of listeriosis”. N. Engl. J. Med. 312 (7): 404–407. doi:10.1056/NEJM198502143120704. PMID 3918263.
- ^ Dykes G. A.; Dworaczek M. (2002). “Influence of interactions between temperature, ferric ammonium citrate and glycine betaine on the growth of Listeria monocytogenes in a defined medium”. Lett Appl Microbiol 35 (6): 538–42. doi:10.1046/j.1472-765x.2002.01237.x.
- ^ “リステリアによる食中毒について”. 食品安全委員会. 2018年8月19日閲覧。
- ^ “リステリア菌食中毒を確認/国内初、北海道で3年半前”. 四国新聞社. (2004年9月13日). 2004-09-13 2018年8月19日閲覧。
- ^ 五十君靜信 (2003). “食品由来のリステリア菌の健康被害に関する研究(総括研究報告書)”. 厚生労働省研究報告書.
- ^ a b 難波, 豊彦 (2015年4月3日). “新たに制定されたリステリア・モノサイトゲネスの成分規格”. 一般財団法人東京顕微鏡院 食と環境の科学センター. 2018年8月19日閲覧。
- ^ Domann E、Chakraborty T (1989-08-11). “Nucleotide sequence of the listeriolysin gene from a Listeria monocytogenes serotype 1/2a strain”. Nucleic acids research 17 (15): 6406. PMC 318305. PMID 2505236.
- ^ Portnoy DA, Chakraborty T, Goebel W, Cossart P (4 1992). “Molecular determinants of Listeria monocytogenes pathogenesis”. Infection and immunity 60: 1263-7. PMC 256991. PMID 1312514.
- ^ Leimeister-Wächter M, Domann E, Chakraborty T「Detection of a gene encoding a phosphatidylinositol-specific phospholipase C that is co-ordinately expressed with listeriolysin in Listeria monocytogenes」『Molecular microbiology』第5巻第2号、1991年、361-366頁、PMID 1645838。
- ^ T Nishibori, H Xiong, I Kawamura, M Arakawa, and M Mitsuyama (8 1996). “Induction of cytokine gene expression by listeriolysin O and roles of macrophages and NK cells”. Infection and Immunity 64 (8): 3188–3195. PMC 174206.
- ^ Lasa I, David V, Gouin E, Marchand JB, Cossart P. (11 1995). “The amino-terminal part of ActA is critical for the actin-based motility of Listeria monocytogenes; the central proline-rich region acts as a stimulator”. Molecular microbiology 18 (3): 425-436. PMID 8748027.
- ^ Dramsi, S., Dehoux, P., Lebrun, M., Goossens, P. L., & Cossart, P. (5 1997). “Identification of four new members of the internalin multigene family of Listeria monocytogenes EGD”. Infection and immunity 65 (5): 1615-1625. PMC 175184. PMID 9125538.
- ^ Sujata Vijh & Eric G. Pamer (4 1997). “Immunodominant and subdominant CTL responses to Listeria monocytogenes infection”. The Journal of Immunology 158 (7): 3366-3371. PMID 9120295.
- ^ 光山 正雄 (3 1997). “リステリアのエスケープ機構と感染宿主応答”. 日本細菌学雑誌 52 (3): 593-600. doi:10.3412/jsb.52.593.
- ^ Schmid M. W.; Ng E. Y. W.; Lampidis R.; Emmerth M.; Walcher M.; Kreft J.; Goebel W. (2005). “Evolutionary history of the genus Listeria and its virulence genes”. Systematic and Applied Microbiology 28 (1): 1–18. doi:10.1016/j.syapm.2004.09.005. PMID 15709360.
- ^ Zhang C.; Zhang M.; Ju J.; Nietfeldt J.; Wise J.; Terry P. M.; Olson M. (2003). “Genome Diversification in Phylogenetic Lineages I and II of Listeria monocytogenes: Identification of Segments Unique to Lineage II Populations”. Journal of Bacteriology 185 (18): 5573–5584. doi:10.1128/JB.185.18.5573-5584.2003. PMC 193770. PMID 12949110.
- ^ Robbins JR, Barth AI, Marquis H, de Hostos EL, Nelson WJ, Theriot JA; Barth; Marquis; De Hostos; Nelson; Theriot (1999). “Listeria monocytogenes Exploits Normal Host Cell Processes to Spread from Cell to Cell”. J. Cell Biol. 146 (6): 1333–50. doi:10.1083/jcb.146.6.1333. PMC 1785326. PMID 10491395.
- ^ Mengaud, J.; Dramsi, S.; Gouin, E.; Vazquez-Boland, J. A.; Milon, G.; Cossart, P. (1991). “Pleiotropic control of Listeria monocytogenes virulence factors by a gene that is autoregulated”. Molecular Microbiology 5 (9): 2273–83. doi:10.1111/j.1365-2958.1991.tb02158.x. PMID 1662763.
- ^ Leimeister-Wachter, M.; Haffner, C; Domann, E; Goebel, W; Chakraborty, T (1990). “Identification of a gene that positively regulates expression of listeriolysin, the major virulence factor of listeria monocytogenes”. Proceedings of the National Academy of Sciences 87 (21): 8336–40. Bibcode: 1990PNAS...87.8336L. doi:10.1073/pnas.87.21.8336. PMC 54950. PMID 2122460.
- ^ Garner, M. R.; Njaa, B. L.; Wiedmann, M.; Boor, K. J. (2006). “Sigma B Contributes to Listeria monocytogenes Gastrointestinal Infection but Not to Systemic Spread in the Guinea Pig Infection Model”. Infection and Immunity 74 (2): 876–86. doi:10.1128/IAI.74.2.876-886.2006. PMC 1360341. PMID 16428730.
- ^ Mandin, Pierre; Fsihi, Hafida; Dussurget, Olivier; Vergassola, Massimo; Milohanic, Eliane; Toledo-Arana, Alejandro; Lasa, Iñigo; Johansson, JöRgen et al. (2005). “VirR, a response regulator critical for Listeria monocytogenes virulence”. Molecular Microbiology 57 (5): 1367–80. doi:10.1111/j.1365-2958.2005.04776.x. PMID 16102006.
- ^ a b c Jeffers G. T.; Bruce J. L.; McDonough P. L.; Scarlett J.; Boor K. J.; Wiedmann M. (2001). “Comparative genetic characterization of Listeria monocytogenes isolates from human and animal listeriosis cases”. Microbiology 147 (Pt 5): 1095–1104. doi:10.1099/00221287-147-5-1095. PMID 11320113.
- ^ Gray M. J.; Zadoks R. N.; Fortes E. D.; Dogan B.; Cai S.; Chen Y.; Scott V. N. (2004). “Listeria monocytogenes Isolates from Foods and Humans Form Distinct but Overlapping Populations”. Applied and Environmental Microbiology 70 (10): 5833–5841. doi:10.1128/AEM.70.10.5833-5841.2004. PMC 522108. PMID 15466521.
- ^ “Anton test - definition of Anton test in the Medical dictionary - by the Free Online Medical Dictionary, Thesaurus and Encyclopedia”. Medical-dictionary.thefreedictionary.com. 2013年8月5日閲覧。
- ^ “Anton's eye test”. Whonamedit. 2013年8月5日閲覧。
- ^ Chapter 13. Non-Spore-Forming Gram-Positive Bacilli: Corynebacterium, Propionibacterium, Listeria, Erysipelothrix, Actinomycetes, & Related Pathogens ,Jawetz, Melnick, & Adelberg's Medical Microbiology, 24th Edition ,The McGraw-Hill Companies
- ^ “103051F-EN-RevC”. Hologic. 2016年6月16日閲覧。
- ^ a b Temple, ME; Nahata, MC (May 2000). “Treatment of listeriosis.”. The Annals of Pharmacotherapy 34 (5): 656–61. doi:10.1345/aph.19315. PMID 10852095.
- ^ Carlton, RM; Noordman, WH; Biswas, B; De Meester, ED; Loessner, MJ (2005). “Bacteriophage P100 for control of Listeria monocytogenes in foods: Genome sequence, bioinformatic analyses, oral toxicity study, and application”. Regulatory Toxicology and Pharmacology 43 (3): 301–12. doi:10.1016/j.yrtph.2005.08.005. PMID 16188359.
- ^ U.S. FDA/CFSAN: Agency Response Letter, GRAS Notice No. 000198
- ^ Krusch, S; Domann, E; Frings, M; Zelmer, A; Diener, M; Chakraborty, T; Weiss, S (2002). “Listeria monocytogenes mediated CFTR transgene transfer to mammalian cells”. The Journal of Gene Medicine 4 (6): 655–67. doi:10.1002/jgm.313. PMID 12439857.
- ^ Chu, Nina J.; Armstrong, Todd D.; Jaffee, Elizabeth M. (2015-04-01). “Nonviral oncogenic antigens and the inflammatory signals driving early cancer development as targets for cancer immunoprevention”. Clinical Cancer Research 21 (7): 1549–1557. doi:10.1158/1078-0432.CCR-14-1186. ISSN 1078-0432. PMC 4383709. PMID 25623216.
- ^ Singh, Reshma; Wallecha, Anu (2011-05-01). “Cancer immunotherapy using recombinant Listeria monocytogenes: transition from bench to clinic”. Human Vaccines 7 (5): 497–505. doi:10.4161/hv.7.5.15132. ISSN 1554-8619. PMID 21422819.
- ^ Fran Lowry (2008-05-15). “Live Listeria Vaccine Proves Safe Against End-Stage Cervical Ca in Human Trial”. Ob. Gyn. News 43 (10): 2. doi:10.1016/S0029-7437(08)70329-X.
