組換えDNA
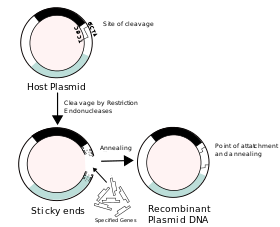
組換えDNA(くみかえDNA、英: recombinant DNA、略称: rDNA)は、複数種に由来する遺伝物質を結合することで形成されたDNA分子のことである。分子クローニングなどの実験室的な遺伝子組換えの手法が用いられ、その結果ゲノムには存在しない配列が作り出される。
すべての生物のDNA分子は共通の化学構造を持っており、異なるのはそのヌクレオチドの並びだけである。そのため、このような組換えDNAを作り出すことができる。組換えDNAは、2つの異なる生物種に由来する物質から作製することもできるため、ギリシア神話のキマイラ(キメラ)からキメラDNA(chimeric DNA)と呼ばれることもある。組換えDNA技術では、回文配列を利用して粘着末端や平滑末端を形成する。
組換えDNA分子の構築に利用されるDNA配列は、どの生物種に由来するものであってもよい。例えば、植物のDNAを細菌のDNAと連結させたり、ヒトのDNAを菌類のDNAと連結させることも可能である。加えて、自然界には存在しないDNA配列を化学合成(オリゴヌクレオチド合成)によって作製し、組換えDNA分子に組み込むこともできる。組換えDNA技術と合成DNAを用いることで、いかなるDNA配列であっても作製可能であり、きわめて多様な生物種へ導入することができる。
生細胞内での組換えDNAの発現によって生じたタンパク質は、組換えタンパク質(recombinant protein)と呼ばれている。タンパク質をコードする組換えDNAが宿主生物へ導入されたとしても、必ずしも組換えタンパク質が産生されるとは限らない[1]。外来タンパク質の発現には、専用の発現用ベクターを用いることが必要であり、多くの場合コーディング配列を大きく再構築する必要がある[2]。
組換えDNAと遺伝的組換えには異なる点が存在する。前者は試験管内で行われる人工的手法によって形成されるのに対し、後者は既存のDNA配列が再混合される正常な生物学過程であり、基本的にすべての生物種で行われる過程である。
作製
[編集]
分子クローニングは、組換えDNAの作製のために用いられる実験室的手法である[3][4][5][6]。ポリメラーゼ連鎖反応(PCR)ともに、特定のDNA配列を複製するために最も広く用いられている実験手法の1つである。分子クローニングとPCRには、2つの基本的な差異が存在する。1つは、分子クローニングは生細胞内でDNAの複製を行うのに対し、PCRは試験管内で行うという点である。もう1つは、分子クローニングはDNA配列の切り貼りを伴うのに対し、PCRは既存配列をコピーのみで増幅を行うという点である。
組換えDNAの形成には、生細胞内で複製を行うDNA分子であるクローニングベクターを必要とする。ベクターは一般的にプラスミドやウイルスに由来し、複製に必要な遺伝的シグナルを含む比較小さなDNA断片が存在する。その他に、外来DNAの挿入や、細胞が組換えDNAを含んでいるかどうかの同定、外来DNAの発現を行う際に便利なエレメントなどが含まれている場合がある。分子クローニングの際のベクターの選択は、宿主生物の選択、クローニングするDNAのサイズ、外来DNAの発現を行うかどうか、どのように行うかに依存する[7]。DNA断片の結合は、制限酵素とリガーゼによるクローニングやギブソン・アセンブリなど、さまざまな手法で行われる。
標準的なクローニングのプロトコルでは、DNA断片のクローニングは次の7つの段階で行われる[6]。
- 宿主生物とクローニングベクターの選択
- ベクターDNAの調製
- クローニングするDNAの調製
- 組換えDNAの作製
- 組換えDNAの宿主生物への導入
- 組換えDNAを含む個体の選択
- 目的のDNA挿入と生物学的性質を有するクローンのスクリーニング
発現
[編集]宿主生物への導入の後、組換えDNAコンストラクトに含まれる外来DNAの発現を行う場合と行わない場合がある。すなわち、DNAの発現は行わず複製のみを行う場合と、転写と翻訳を行って組換えタンパク質の生産を行う場合とがある。一般的に外来遺伝子の発現には、宿主生物の転写・翻訳装置を利用するために必要な配列(プロモーター、ターミネーター、翻訳開始シグナルなど)を遺伝子に組み込んでおくことが必要である[8]。このような遺伝子の発現を改善するために、宿主側に特定の変更が施されることもある。さらに、翻訳の最適化、タンパク質の可溶化、組換えタンパク質の細胞内外の適切な部位への輸送、タンパク質の分解を防ぐ安定化などを目的とした変更をコーディング配列に施す必要がある場合もある[9][10]。
組換えDNAを含む生物の性質
[編集]多くの場合、組換えDNAを含む生物は見かけ上正常な表現型を示す。すなわち、その外見、行動、代謝には通常変化がみられない。組換え配列の存在を示す唯一の方法はDNA自身の調査であり、一般的にはPCR検査が行われる[11]。重要な例外も存在し、後述する。
組換えDNA配列から遺伝子の発現が行われている場合、組換え遺伝子のRNAまたはタンパク質産物から組換え配列の存在を検出することもできる。一般的にはRT-PCRやウェスタンブロッティングが行われる[11]。宿主生物で生物学的活性が生じるような組換え遺伝子の選択と修正が行われていない場合には、表現型変化の観察は標準的手法ではない[12]。組換え遺伝子産物によって宿主生物に毒性がもたらされることで付加的な表現型が生じることがあり、特に過剰発現が行われている場合や、不適当な細胞や組織で発現が行われている場合に生じやすい。
組換えDNAは発現していない場合でも宿主生物に有害な影響を与えることがある。1つの機構としては挿入による不活性化があり、組換えDNAが宿主細胞の遺伝子へ挿入された場合に生じる。この現象は、遺伝子を「ノックアウト」してその生物学的機能や重要性を明らかにするためにも利用される[13]。他の機構としては、染色体への組換えDNAの挿入によって、宿主細胞でこれまで発現していなかった遺伝子が不適切な形で活性化される場合がある。例えば、組換えDNA断片に活性の高いプロモーターが存在し、それによって隣接する抑制されていた遺伝子が活性化されてしまう場合や、遺伝子発現の抑制機能を持つ宿主細胞の遺伝子が組換えDNAによる挿入不活性化を受ける場合がある。
利用
[編集]組換えDNAはバイオテクノロジー、医療、研究で広く利用されている。今日、DNA技術を利用した組換えタンパク質や他の製品は、ほぼすべての薬局、病院、動物病院、臨床検査室や生物学の研究室に置かれている。加えて、組換えDNA技術によって改変された生物やそうした生物に由来する製品は、多くの農場、スーパーマーケット、家庭の常備薬庫にも進出しており、ペットショップでもGloFishなどの遺伝子組換え生物が売られている。
組換えDNAが最も一般的に利用されているのは基礎研究においてであり、現在の生物学や生物医学研究の大部分で重要な役割を果たしている[11]。組換えDNAは遺伝子の同定、マッピング、シーケンシングや、その遺伝子の機能を決定するために利用される。組換えDNAによるプローブは、個々の細胞や生物の組織全体での遺伝子発現の解析に利用される。組換えタンパク質は研究室での実験試薬として広く利用されており、細胞内や生体内でのタンパク質合成を調べる抗体プローブを作り出すためにも利用されている[4]。
組換えDNAは、工業、食品生産、医学や獣医学、農業、生物工学といった分野で多くの実用化がなされている[4]。一部の例を下に挙げる。
組換えキモシン
[編集]レンネットに含まれるキモシンは、チーズの製造に必要な酵素である。キモシンは遺伝子操作が行われた食品添加物として初めて商業的に利用された。伝統的に、加工業者は哺乳期間中の仔牛の第4胃から調製したレンネットからキモシンを得ていた。科学者は実験室での大規模な酵素生産を行うために大腸菌Escherichia coliの非病原性株(K-12)を操作した。この微生物によって産生された組換え酵素は、仔牛由来の酵素と構造的に同一であり、低コストで大量に生産を行うことができた。今日アメリカ合衆国のハードチーズの約60%は遺伝子組換えキモシンを用いて製造されている。1990年、FDAは酵素の安全性を示すデータに基づいてキモシンを「一般に安全と認められる」と評価した[14]。
組換えヒトインスリン
[編集]インスリン依存型糖尿病の治療に用いられるインスリンは、ブタやウシなどの動物由来のものから遺伝子組換えのものへほぼ完全に置き換えられており、さまざまな組換えインスリン製剤が広く利用されている[15]。組換えインスリンはヒトのインスリン遺伝子を大腸菌E. coliや出芽酵母Saccharomyces cerevisiaeへ挿入することによって合成されている[16]。
組換えヒト成長ホルモン(HGH、ソマトトロピン)
[編集]脳下垂体で十分な量の成長ホルモンが産生されない患者には、正常な成長と発達をサポートするために組換えヒト成長ホルモンが投与される。組換えヒト成長ホルモンが利用できるようになる前は、治療目的の成長ホルモンは死体の脳下垂体から得られていた。この安全性に欠ける手法によって、一部の患者はクロイツフェルト・ヤコブ病を発症した。組換え成長ホルモンによってこの問題は解消され、現在では治療目的で広く利用されている[17]。また、アスリートなどによってパフォーマンス向上薬としての誤った利用もなされている[18]。 DrugBank entry
組換え血液凝固第VIII因子
[編集]血液凝固タンパク質は、正常な血液凝固に十分な量の第VIII因子を産生することができない血友病など、出血障害の患者に投与されている[19]。組換え第VIII因子が開発される前は、第VIII因子は複数のドナーからの大量の血液を処理することによって得られており、HIVやB型肝炎など血液感染を行う疾患の伝染リスクが非常に高かった。DrugBank entry
組換えB型肝炎ワクチン
[編集]B型肝炎の感染は、組換えB型肝炎ワクチンの利用によってコントロールされている。 組換えB型肝炎ワクチンには、酵母細胞で産生されたB型肝炎ウイルスの表面抗原の一種が含まれている。B型肝炎ウイルスはポリオウイルスなどの他の一般的なウイルスのようにin vitroでの生育を行うことができないため、組換えサブユニットを含むワクチンの開発は、重要かつ必要なものであった。Vaccine information from Hepatitis B Foundation
HIV感染の検査
[編集]HIV/AIDSの検査で広く用いられている3つの手法は、組換えDNAを利用して開発されたものである。抗体検査(ELISAまたはウェスタンブロッティングによるもの)は、HIVの感染に応答して体内で産生された抗体を検出するために組換えHIVタンパク質を利用する。DNA検査は、RT-PCRによってHIVに由来する遺伝物質の存在を検査する。RT-PCR試験の開発は、HIVのゲノムの分子クローニングと配列解析によって可能となった。 HIV testing page from US Centers for Disease Control (CDC)
ゴールデンライス
[編集]ゴールデンライスは、β-カロテンの生合成を担う酵素を発現するよう遺伝子操作がなされたコメの品種である[12]。この品種は、世界中でビタミンA欠乏症の発生数を減少させることが大きく期待されている[20]。ゴールデンライスは現在利用されておらず、規制や知的財産権[21]の問題の解決が待たれる。
除草剤耐性作物
[編集]重要な農作物(ダイズ、トウモロコシ、モロコシ、ナタネ、アルファルファ、ワタなど)において、除草剤グリホサート(商品名: ラウンドアップ)に対する耐性をもたらす遺伝子を組み込み、グリホサートによる雑草管理を容易にした品種が開発されている[22]。このような作物は、いくつかの国では一般的に商業利用されている。
害虫耐性作物
[編集]バチルス・チューリンゲンシスBacillus thuringeiensisは、殺虫作用をもつタンパク質(Bt毒素)を天然産生する微生物である[20]。この微生物は作物の害虫管理に長年利用されており、農業や園芸で広く利用されている。近年、この細菌タンパク質を組換え発現する植物が開発され、一部の害虫に対する効率的な対策となる可能性がある。これらの遺伝子組換え作物の利用に関係する環境問題は、完全には解決されていない[23]。
歴史
[編集]組換えDNAの概念は、スタンフォード大学医学部の生化学部門の教授デール・カイザーの大学院生であったPeter Lobbanによって初めて提唱された[24]。組換えDNAの作製と細胞内での複製の成功を記載した最初の論文は、1972年と1973年にスタンフォード大学とカリフォルニア大学サンフランシスコ校(UCSF)から発表された[25][26][27][28]。最初の論文[25]の著者の1人であったスタンフォード大学医学部生化学部門の教授ポール・バーグは、組換えDNAに関する核酸研究についての業績で1980年にノーベル化学賞を受賞した。ヴェルナー・アーバー、ハミルトン・スミス、ダニエル・ネイサンズは、組換えDNA技術の向上をもたらした制限酵素の発見によって、1978年にノーベル生理学・医学賞を受賞した。
スタンフォード大学は、UCSFの教授ハーバート・ボイヤー、スタンフォード大学の教授スタンリー・N・コーエンを発明者として、1974年に組換えDNAに関するアメリカ合衆国での特許を申請し、1980年に取得した[29]。組換えDNA技術を利用して作られた最初の認可薬は、ジェネンテックによる開発とイーライリリー・アンド・カンパニーの提携によるヒトインスリンである[30]。
論争
[編集]初期の組換えDNA手法の開発に関係していた科学者らは、組換えDNAを含む生物に望ましくないまたは危険な性質が存在する可能性を認識していた。1975年のアシロマ会議ではこれらの懸念についての議論がなされ、組換えDNA研究に関し、特に危険性が高いと見なされた実験の自主的な停止が行われた。この実験停止は、アメリカ国立衛生研究所から組換えDNA実験に関する公式なガイドラインが作成・発行されるまで広く順守されていた。今日、組換えDNA分子や組換えタンパク質は一般的には危険なものとはみなされていない。しかし、組換えDNAを発現する一部の生物、特にそれらが実験室を離れて環境や食物連鎖へ持ち込まれた際の懸念は残されている。さらに、バイオ医薬品生産、特に組換えDNAから特定のタンパク質を産生した際の副産物に関する懸念も存在する。宿主細胞由来タンパク質と呼ばれる、宿主の発現系に由来する主要な副産物は、患者の健康や環境全体に対する脅威となる可能性がある[31][32]。
出典
[編集]- ^ Rosano, Germán L.; Ceccarelli, Eduardo A. (2014-04-17). “Recombinant protein expression in Escherichia coli: advances and challenges”. Frontiers in Microbiology 5: 172. doi:10.3389/fmicb.2014.00172. ISSN 1664-302X. PMC 4029002. PMID 24860555.
- ^ “Promoters used to regulate gene expression”. www.cambia.org. 16 February 2018閲覧。
- ^ Campbell, Neil A. & Reece, Jane B.. (2002). Biology (6th ed.). San Francisco: Addison Wesley. pp. 375–401. ISBN 978-0-201-75054-6
- ^ a b c Peter Walter; Alberts, Bruce; Johnson, Alexander S.; Lewis, Julian; Raff, Martin C.; Roberts, Keith (2008). Molecular Biology of the Cell (5th edition, Extended version). New York: Garland Science. ISBN 978-0-8153-4111-6. Fourth edition is available online through the NCBI Bookshelf: link
- ^ Berg, Jeremy Mark; Tymoczko, John L.; Stryer, Lubert (2010). Biochemistry, 7th ed. (Biochemistry (Berg)). W.H. Freeman & Company. ISBN 978-1-4292-2936-4 Fifth edition available online through the NCBI Bookshelf: link
- ^ a b Watson, James D. (2007). Recombinant DNA: Genes and Genomes: A Short Course. San Francisco: W.H. Freeman. ISBN 978-0-7167-2866-5
- ^ Russell, David W.; Sambrook, Joseph (2001). Molecular cloning: a laboratory manual. Cold Spring Harbor, N.Y: Cold Spring Harbor Laboratory. ISBN 978-0-87969-576-7
- ^ Hannig, G.; Makrides, S. (1998). “Strategies for optimizing heterologous protein expression in Escherichia coli”. Trends in Biotechnology 16 (2): 54–60. doi:10.1016/S0167-7799(97)01155-4. PMID 9487731.
- ^ Brondyk, W. H. (2009). “Chapter 11 Selecting an Appropriate Method for Expressing a Recombinant Protein”. Guide to Protein Purification, 2nd Edition. Methods in Enzymology. 463. pp. 131–147. doi:10.1016/S0076-6879(09)63011-1. ISBN 9780123745361. PMID 19892171
- ^ Ortega, Claudia; Prieto, Daniel; Abreu, Cecilia; Oppezzo, Pablo Javier; Correa, Agustin (2018). “Multi-compartment and multi-host vector suite for recombinant protein expression and purification.” (English). Frontiers in Microbiology 9: 1384. doi:10.3389/fmicb.2018.01384. ISSN 1664-302X. PMC 6030378. PMID 29997597.
- ^ a b c Brown, Terry (2006). Gene Cloning and DNA Analysis: an Introduction. Cambridge, MA: Blackwell Pub. ISBN 978-1-4051-1121-8
- ^ a b Ye, X.; Al-Babili, S.; Klöti, A.; Zhang, J.; Lucca, P.; Beyer, P.; Potrykus, I. (2000). “Engineering the provitamin A (beta-carotene) biosynthetic pathway into (carotenoid-free) rice endosperm”. Science 287 (5451): 303–305. doi:10.1126/science.287.5451.303. PMID 10634784.
- ^ Koller, B. H.; Smithies, O. (1992). “Altering Genes in Animals by Gene Targeting”. Annual Review of Immunology 10: 705–730. doi:10.1146/annurev.iy.10.040192.003421. PMID 1591000.
- ^ Donna U. Vogt and Mickey Parish. (1999) Food Biotechnology in the United States: Science, Regulation, and Issues
- ^ Gualandi-Signorini, A.; Giorgi, G. (2001). “Insulin formulations--a review”. European Review for Medical and Pharmacological Sciences 5 (3): 73–83. PMID 12004916.
- ^ DrugBank: Insulin Regular (DB00030)
- ^ Von Fange, T.; McDiarmid, T.; MacKler, L.; Zolotor, A. (2008). “Clinical inquiries: Can recombinant growth hormone effectively treat idiopathic short stature?”. The Journal of Family Practice 57 (9): 611–612. PMID 18786336.
- ^ Fernandez, M.; Hosey, R. (2009). “Performance-enhancing drugs snare nonathletes, too”. The Journal of Family Practice 58 (1): 16–23. PMID 19141266.
- ^ Manco-Johnson, M. J. (2010). “Advances in the Care and Treatment of Children with Hemophilia”. Advances in Pediatrics 57 (1): 287–294. doi:10.1016/j.yapd.2010.08.007. PMID 21056743.
- ^ a b Paine, J. A.; Shipton, C. A.; Chaggar, S.; Howells, R. M.; Kennedy, M. J.; Vernon, G.; Wright, S. Y.; Hinchliffe, E. et al. (2005). “Improving the nutritional value of Golden Rice through increased pro-vitamin a content”. Nature Biotechnology 23 (4): 482–487. doi:10.1038/nbt1082. PMID 15793573.
- ^ Deccan Herald, " Foreign group roots for 'golden rice' in India", March 18, 2015 http://www.deccanherald.com/content/466247/foreign-group-roots-golden-rice.html
- ^ Funke, T.; Han, H.; Healy-Fried, M.; Fischer, M.; Schönbrunn, E. (2006). “Molecular basis for the herbicide resistance of Roundup Ready crops”. Proceedings of the National Academy of Sciences 103 (35): 13010–13015. doi:10.1073/pnas.0603638103. PMC 1559744. PMID 16916934.
- ^ Mendelsohn, M.; Kough, J.; Vaituzis, Z.; Matthews, K. (2003). “Are Bt crops safe?”. Nature Biotechnology 21 (9): 1003–1009. doi:10.1038/nbt0903-1003. PMID 12949561.
- ^ Lear, J. (1978). Recombinant DNA: The Untold Story. New York: Crown Publishers. p. 43.
- ^ a b Jackson, D.; Symons, R.; Berg, P. (1972). “Biochemical method for inserting new genetic information into DNA of Simian Virus 40: Circular SV40 DNA molecules containing lambda phage genes and the galactose operon of Escherichia coli”. Proceedings of the National Academy of Sciences of the United States of America 69 (10): 2904–2909. doi:10.1073/pnas.69.10.2904. PMC 389671. PMID 4342968.
- ^ Mertz, J. E.; Davis, R. W. (1972). “Cleavage of DNA by R 1 restriction endonuclease generates cohesive ends”. Proceedings of the National Academy of Sciences of the United States of America 69 (11): 3370–4. doi:10.1073/pnas.69.11.3370. PMC 389773. PMID 4343968.
- ^ Lobban, P.; Kaiser, A. (1973). “Enzymatic end-to end joining of DNA molecules”. Journal of Molecular Biology 78 (3): 453–471. doi:10.1016/0022-2836(73)90468-3. PMID 4754844.
- ^ Cohen, S.; Chang, A.; Boyer, H.; Helling, R. (1973). “Construction of biologically functional bacterial plasmids in vitro”. Proceedings of the National Academy of Sciences of the United States of America 70 (11): 3240–3244. doi:10.1073/pnas.70.11.3240. PMC 427208. PMID 4594039.
- ^ Hughes, S. (2001). “Making dollars out of DNA. The first major patent in biotechnology and the commercialization of molecular biology, 1974-1980”. Isis; an International Review Devoted to the History of Science and Its Cultural Influences 92 (3): 541–575. doi:10.1086/385281. hdl:10161/8125. PMID 11810894.
- ^ Johnson, I. S. (1983). “Human insulin from recombinant DNA technology”. Science 219 (4585): 632–637. doi:10.1126/science.6337396. PMID 6337396.
- ^ Wang, Xing; Hunter, Alan K.; Mozier, Ned M. (2009-06-15). “Host cell proteins in biologics development: Identification, quantitation and risk assessment” (英語). Biotechnology and Bioengineering 103 (3): 446–458. doi:10.1002/bit.22304. ISSN 0006-3592. PMID 19388135.
- ^ Bracewell, Daniel G.; Francis, Richard; Smales, C. Mark (2015-07-14). “The future of host cell protein (HCP) identification during process development and manufacturing linked to a risk-based management for their control” (英語). Biotechnology and Bioengineering 112 (9): 1727–1737. doi:10.1002/bit.25628. ISSN 0006-3592. PMC 4973824. PMID 25998019.
関連文献
[編集]- The Eighth Day of Creation: Makers of the Revolution in Biology. Touchstone Books, ISBN 0-671-22540-5. 2nd edition: Cold Spring Harbor Laboratory Press, 1996 paperback: ISBN 0-87969-478-5.
- Micklas, David. 2003. DNA Science: A First Course. Cold Spring Harbor Press: ISBN 978-0-87969-636-8.
- Rasmussen, Nicolas, Gene Jockeys: Life Science and the rise of Biotech Enterprise, Johns Hopkins University Press, (Baltimore), 2014. ISBN 978-1-42141-340-2.
- Rosenfeld, Israel. 2010. DNA: A Graphic Guide to the Molecule that Shook the World. Columbia University Press: ISBN 978-0-231-14271-7.
- Schultz, Mark and Zander Cannon. 2009. The Stuff of Life: A Graphic Guide to Genetics and DNA. Hill and Wang: ISBN 0-8090-8947-5.
- Watson, James. 2004. DNA: The Secret of Life. Random House: ISBN 978-0-09-945184-6.
関連項目
[編集]外部リンク
[編集]- Recombinant DNA fact sheet (from University of New Hampshire)
- Plasmids in Yeasts (Fact sheet from San Diego State University)
- Animation illustrating construction of recombinant DNA and foreign protein production by recombinant bacteria
- Recombinant DNA research at UCSF and commercial application at Genentech Edited transcript of 1994 interview with Herbert W. Boyer, Living history project. Oral history.
- Recombinant Protein Purification Principles and Methods Handbook
