胃腸炎
| 胃腸炎 | |
|---|---|
 | |
| 胃腸炎ウイルス: A = ロタウイルス, B = アデノウイルス, C = ノロウイルス D = アストロウイルス サイズ比較のため、各ウイルスは同じ拡大率で示してある。 | |
| 概要 | |
| 診療科 | 消化器学 |
| 分類および外部参照情報 | |
| ICD-10 | A02.0, A08, A09, J10.8,J11.8, K52 |
| ICD-9-CM | 008.8 009.0, 009.1, 558 |
| DiseasesDB | 30726 |
| MedlinePlus | 000252 000254 |
| eMedicine | emerg/213 |
| MeSH | D005759 |
胃腸炎(いちょうえん、英語: gastroenteritis)とは、感染性下痢(infectious diarrhea)、ガストロとも知られ、消化管 胃 ("gastro"-)および小腸 ("entero"-)の炎症を特徴とする疾患であり、発熱、下痢、嘔吐、腹痛および腹部痙攣などの症状を呈する[1]。食物によって生じるものは食中毒とも称される。山陰地方では、感染性胃腸炎の事を腸感冒とも呼ぶ[2]。
世界的にみて小児の発症例のほとんどがロタウイルスによるものである[3]。成人ではノロウイルス[4]およびカンピロバクター[5]に起因するものが最も多い。次いでその他の細菌 (またはその毒素)や寄生虫を原因とするものがよくみられる。調理が不適切な食品や汚染された水を摂取したり、感染者との密接な接触などによって感染する。
治療の基本は十分な水分補給である。軽度または中等度の症例では経口補水液の補給が効果的である。重症例になると静脈内輸液が必要となる場合がある。
症状および徴候
[編集]胃腸炎では通常下痢と嘔吐の双方がみられることが多く[6]、また頻度は下がるものの、そのいずれかのみがみられることもある[1]。腹部痙攣を生じる場合もある[1]。症状および徴候は通常、感染から12〜72時間で発現しはじめる[7]。
ウイルス性胃腸炎の場合、症状は通常1週間以内に軽快し[6]、発熱、倦怠感、頭痛、筋肉痛を伴うことがある[6]。血便がみられる場合、ウイルス性である可能性は低く[6]、細菌感染が疑われる[8]。一部の細菌感染では重度の腹痛を伴い、数週間続くことがある[8]。
ロタウイルスに感染した小児は通常3〜8日以内に全快する[9]。ただし貧困国では重度の感染に対する治療が行き届かないことが多く、下痢が長引くことが多い[10]。下痢の合併症として脱水が頻繁にみられる。[11]脱水の程度が顕著な小児例では毛細血管再充満時間が長く、皮膚の張りの低下、呼吸異常などがみられる[12]。衛生状態が悪く栄養失調のみられる地域では感染を繰り返すことも多く[7]発育不全や長期的な認知機能の発達遅延をもたらす場合がある[13]。
カンピロバクター属細菌感染者の1%が反応性関節炎を、0.1%がギラン・バレー症候群を発症する[8]。志賀毒素(ベロ毒素)を産生する腸管出血性大腸菌や赤痢菌に感染すると、血小板減少や腎不全、溶血性貧血の結果、溶血性尿毒症症候群 (HUS)を発症することがある。[14]小児の方が成人よりもHUSを発症しやすい[13]。ウイルス感染では良性小児てんかんを来たすこともある[1]。
原因
[編集]ウイルスおよび大腸菌や カンピロバクター属菌などの細菌が胃腸炎の主な原因である[15][7]。感染リスクは小児の方が高くなっており、これは免疫が不十分であったり不衛生になりやすいためである[1]。
ウイルス性
[編集]急性胃腸炎の原因として知られるウイルスにはロタウイルス、ノロウイルス、アストロウイルス、アデノウイルス[16]などがある[6][17]。ウイルス性胃腸炎の中で、臨床的な意義が確立されているのはロタウイルス、ノロウイルス、サポウイルス、アデノウイルス、アストロウイルスの5種類である[18]。
小児の胃腸炎ではロタウイルスがもっとも多く[15]、先進国でも発展途上国でも発症率は同程度である[9]。小児の感染性下痢の70%がウイルスによるものである。[19]成人は獲得免疫を有するため、ロタウイルス感染はあまりみられない[20]。
アメリカではノロウイルスが成人の胃腸炎の主要な原因となっており、集団発生の90%以上がこのウイルスによるものである[6]。このような限局性の流行は、クルーズ客船 [6]や病院、レストランなど、人々が密接した空間で過ごしている時に発生しやすい[1]。下痢が治まった後も保菌者の感染性は持続しており[6]1ヶ月程度ウイルスを排出し続ける[21][6]。小児の感染例の約10%はノロウイルスによるものである[1]。
細菌性
[編集]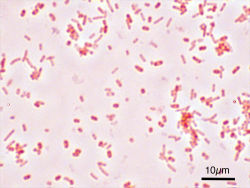
先進国ではカンピロバクター・ジェジュニが細菌性胃腸炎の主な原因となっており、その半数は家禽との接触によるものである[8]。小児では細菌が感染例の15%の原因となっており、最もよくみられるものに大腸菌、サルモネラ菌、赤痢菌、カンピロバクター属などがある[19]。細菌に汚染された食品を常温で数時間放置すると細菌が増殖し、その食品を食べた場合の感染リスクが上昇する[13]。なかでも食中毒の原因としてよくみられるものに、生肉や過熱が不十分な食肉、家禽、海鮮類、卵、生のスプラウト、低温殺菌されていない牛乳、ソフトチーズ、果物や野菜のジュースなどがある[22]。発展途上国(特にサハラ以南アフリカやアジア)では、コレラが胃腸炎の原因としてよくみられ、多くは汚染された水や食品による感染である[23]。
高齢者では、毒素産生型クロストリディオイデス・ディフィシルもまた下痢の原因として重要である[13]。乳幼児も無症候でこの細菌を保菌していることがある[13]。入院患者の下痢の原因としてよくみられ、抗生物質の使用が誘発していることが多い[24]。黄色ブドウ球菌 感染による下痢もまた、抗生物質を使用している患者に発生することがある[25]。旅行者下痢の多くは細菌性胃腸炎の一種である。胃酸分泌抑制剤の使用もまた、クロストリディオイデス・ディフィシル、サルモネラ菌、カンピロバクター属など多数の微生物への曝露から感染につながるリスクを上昇させるようである[26]。このリスクはヒスタミンH2受容体拮抗薬よりもプロトンポンプ阻害薬を摂取している患者の方が高くなっている[26]。
寄生虫性
[編集]さまざまな原生動物が胃腸炎の原因となりうる。特によくみられるのがランブル鞭毛虫であるが、赤痢アメーバやクリプトスポリジウム もまた原因となりうる[19]。このような病原体によるものが小児発症例の10%を占める[14]。ジアルジア症は発展途上国によくみられるが、ランブル鞭毛虫によるこのタイプの疾患は世界中ほぼどこでも起こりうる[27]。この疾患は、有病率の高い地域への旅行者や保育所に通う小児、男性間の性交、災害時などに発生しやすくなる[27]。
伝染
[編集]汚染水の摂取や身の回り品の共用などによって伝染する[7]。雨季と乾季のある地域では乾季に水質が悪化するため、集団発生につながりやすい[7]。四季のある地域では冬に感染が増える[13]。世界的にみて哺乳瓶の不衛生な管理が大きな原因となっている[7]。感染率は不衛生にも相関しており、特に小児[6]や大所帯[28]、栄養状態の悪い集団にはその影響が顕著である[13]。耐性がつくため、成人の場合何ら症状を呈さずに病原体を保菌していることがある(自然宿主)[13]。赤痢菌など、一部の病原体の感染はサル目に限られる一方、多岐にわたる動物に感染するものもある(ランブル鞭毛虫等)[13]。
非感染性
[編集]消化管の炎症を惹き起こす原因には、非感染性のものも数多く存在する[1]。よくみられるものには、医薬品 (NSAIDs等)、ラクトース (不耐性者の場合)やグルテン (セリアック病患者の場合)を含む食品などが挙げられる。クローン病もまた非感染性の胃腸炎を惹き起こし、その症状の多くは重度である[1]。また毒素によるものもある。食品が原因となって吐き気や嘔吐、下痢を惹き起こすものには、捕食によって汚染された魚類を摂取することによるシガテラ中毒、腐敗した魚の摂取によるヒスタミン中毒、フグによるテトドロドキシン中毒、保存状態の悪い食品が原因となることの多いボツリヌス中毒などが挙げられる[29]。
病態
[編集]胃腸炎は小腸や大腸の感染による嘔吐、下痢を特徴とする[13]。小腸にみられる変化は非炎症性であることが多いが、大腸では炎症性である[13]。感染を惹き起こす病原体数はクリプトスポリジウムの1株からコレラ菌の108株までさまざまである[13]。
診断
[編集]胃腸炎は患者の徴候および症状をもとに臨床診断される[6]。直接的な原因を判別することは治療法を左右するものではないため、通常必要とされない[7]。ただし、糞便中に潜血がある場合や食中毒が疑われる場合、最近発展途上国に滞在歴のある患者の場合には検便を実施する必要がある[19]。また、監視のため診断試験を実施することがある[6]。乳児および小児の約10%に低血糖がみられるため、この年齢層の患者には血清グルコース濃度の測定が推奨される[12]。重度の脱水が疑われる場合は電解液および腎機能を確認する必要がある[19]。
脱水
[編集]診断の上では患者が脱水を来たしているかどうかの判断が重要となる。脱水の程度は通常、軽度 (3〜5%)、中等度 (6〜9%)および重度 (≥10%)に分けられる[1]小児の場合、中等度または重度の脱水を示す最も正確な徴候は毛細血管再充満時間の延長、皮膚弾力の低下、呼吸異常である[12][30]。この他併用するのに有用な所見として眼のくぼみ、活動性の低下、眼や口の渇きなどが挙げられる[1]。正常な排尿と飲水がみられれば危険度は少ない[12]。脱水の程度を明らかにする上で、臨床検査はあまり有益ではない[1]。
鑑別診断
[編集]胃腸炎でなくとも似た徴候および症状を呈することのあるものに虫垂炎、腸捻転、炎症性腸疾患、尿路感染症および糖尿病などがあり、鑑別が必要である[19]。このほか膵不全、短腸症候群、ウィップル病、セリアック病、瀉下薬中毒も考慮する必要がある[31]。鑑別診断は嘔吐または下痢のいずれかのみを呈する患者の方が、双方の症状を呈する患者よりもいくぶん複雑化する[1]。
虫垂炎の場合、全例の33%に嘔吐、腹痛、少量の下痢がみられる[1]。胃腸炎の下痢は通常多量であるという点で対比している[1]。小児の場合、肺や尿路に感染がある場合も嘔吐や下痢を惹き起こすことがある[1]。糖尿病性ケトアシドーシス (DKA)も腹痛、吐き気、嘔吐などの症状を呈するが、下痢はみられない[1]。ある試験によれば、DKAの小児の17%が最初は胃腸炎と診断されている[1]。
予防
[編集]
生活習慣
[編集]汚染されていない水を容易に利用できるようにし、習慣的に良い衛生状態を保つことが、感染や臨床的に有意な胃腸炎の発生率を減少させる上で重要である[13]。各個人の手洗い等の実践が、途上国でも先進国でも胃腸炎の有病率を30%も減少させることがわかっている[12]。消毒用アルコールジェルも効果的である[12]。衛生状態の悪い地域では特に、全体的な衛生状態の改善と並んで授乳が重要な役割を果たす[7]。母乳は感染の頻度と感染期間のいずれも減少させる[1]。汚染された食品や飲料を避けることもまた効果的である[32]。
ワクチン投与
[編集]世界保健機関は2009年に性双方の点で、全世界的に小児へのロタウイルスワクチン投与を推奨している[33][15]。市場には2種のロタウイルスワクチンが既に存在し、さらに数種が開発中である[33]。アフリカおよびアジアではこのワクチンが小児の重度の胃腸炎を減少させており[33]、国家予防接種プログラムを実施している国々では疾患の発症率と重症度が低下している[34][35]。このワクチンはほかにも、感染循環を減少させることによってワクチン未投与の小児にも予防効果がみられる[36]。2000年から実施されたアメリカ合衆国でのロタウイルスワクチン投与プログラムによって、下痢の症例数が実に80%も減少している[37][38][39]。ワクチンの初回投与は生後6週から15週の間に投与することが望ましい[15]。経口コレラワクチンは2年以上にわたって50〜60%の有効性が確認されている[40]。
治療
[編集]胃腸炎は通常急性の自己制限疾患であり、投薬は必要としない[11]。軽度ないし中等度の脱水には経口補水液による治療(ORT)がよく用いられる[14]。ただし、小児にはメトクロプラミドやオンダンセトロンが治療の助けとなることがある[41]。腹痛の治療にはブチルスコポラミンが有用である[42]。
水分補給
[編集]小児、成人ともに、胃腸炎の一次治療は水分補給である。経口補水液による水分補給が適しているが、意識レベルの低下がみられる場合や脱水が重度である場合、点滴静脈注射による輸液が必要となることがある[43][44]。経口補水液は単糖類を含むものより複合炭水化物から作られたもの(麦や米を原料とするものなど)の方が好ましい[45]。ソフトドリンクやフルーツジュースなどの単糖類を特に多く含む飲料は、下痢を増悪させることがあるため推奨されない[11]。経口補水液が手に入らない場合や患者が好まない場合、これよりも効果は落ちるが純粋な水を用いることもある[11]。必要性がある場合、小児には経鼻カテーテルを使用することもある[19]。一方、小児の軽症胃腸炎患者に対しては、2倍希釈のリンゴジュースを用いると治療失敗が少ないとの報告がある[46]。
食事
[編集]母乳で育てている乳児には普段通り母乳を与えることが望ましく、乳児用流動食を与えている乳児には、ORTによる水分補給後すみやかに同じ乳児用流動食を与えることが推奨されている[47]。無乳糖または低乳糖の流動食を与える必要はない[47]。小児には下痢が続く間も通常の食事を続けさせることが望ましいが、例外として単糖を多く含む食品は避けるようにする[47]。 BRATダイエット (バナナ、米、アップルソース、トースト、お茶)は、栄養分が不足しており通常の食事と比べて便益性が高いわけでもないため、現在では推奨されていない[47]。一部のプロバイオティックスは、回復までの時間と下痢の頻度をいずれも減少させる効果があることが示されている[48]。また、抗生物質によって惹き起こされる下痢の予防と治療にも有用である[49]。発酵乳製品(ヨーグルト等)も同じく有益である[50]。発展途上国では亜鉛の補給が小児の下痢の治療および予防いずれにも効果的であると考えられている[51]。
制吐薬
[編集]制吐薬の投与は小児の嘔吐の治療の一助となる。オンダンセトロンには一定の有益性があり、単回投与によって静脈内輸液や入院の必要性を低下させ、嘔吐回数を減少させる[52][53][54]。メトクロプラミドもまた場合によっては有用である[54]。ただし、オンダンセトロンの使用が小児の再入院率を上昇させる可能性がある[55]。オンダンセトロンの静脈内投与が臨床的に難しい場合は経口投与も可能である[56]。ジメンヒドリナートは嘔吐を減少させはするものの、臨床的に有意な便益性は認められない[1]。
抗生物質
[編集]抗生物質は通常胃腸炎の治療には用いられないが、症状が特に重度の場合[57]や、細菌性の原因が特定されるか疑われる場合に限り推奨されることがある[58]。抗生物質を用いる必要がある場合、キノロン系よりマクロライド系抗生物質 (アジスロマイシン等)の方が抵抗率が高いため好ましい[8]。通常抗生物質の使用によって惹き起こされる偽膜性大腸炎は、原因となった抗生物質の投与を中止し、メトロニダゾールまたはバンコマイシンを用いて治療する[59]。治療の効果があらわれやすい細菌および原生動物は赤痢菌[60]、腸チフス、[61]ジアルジア属である[27]。ジアルジア属や赤痢アメーバを原因とするものは、チニダゾールによる治療が推奨されており、メトロニダゾールよりも優れている[62][27]。世界保健機関 (WHO)は、血性下痢および発熱いずれもみられる乳幼児には抗生物質の使用を推奨している[1]。
腸管運動抑制剤
[編集]腸管運動抑制剤の投与は理論上合併症を惹き起こすリスクが高いとされており、臨床経験からはその可能性は高くないと示されているものの[31]、やはり血性下痢や発熱を伴う下痢のある患者には使用を控えるべきである[63]。オピオイド作動薬のひとつであるロペラミドは、下痢の対症療法としてよく用いられる[64]が、小児に対しては未成熟な血液脳関門を通過して毒性を持ちうるため推奨されていない。三価ビスマスとサルチル酸塩の非溶解性複合体である次サリチル酸ビスマスは、軽度ないし中等度の症例に用いることができるが[31]、理論上サルチル酸中毒を来たす可能性がある[1]。
疫学
[編集]
| no data ≤less 500 500–1000 1000–1500 1500–2000 2000–2500 2500–3000 | 3000–3500 3500–4000 4000–4500 4500–5000 5000–6000 ≥6000 |
胃腸炎は年間ベースで全世界的に30億〜50億例が発症しており、そのうち140万例が死亡していると見積もられており[65]、なかでも小児および発展途上国の住人の感染例が中心となっている[7]。2011年現在、5歳未満の小児17億例中70万例が死亡しており[66]、そのほとんどが貧困国で起こっている[13]。死亡例のうち450,000例以上が5歳未満の小児のロタウイルス感染によるものである[67][68]。コレラの年間発症数は300〜500万例であり、約100,000人が死亡している[23]。発展途上国では2歳未満の小児が毎年6回以上の頻度で臨床的に重大な胃腸炎を発症している[13]。成人は獲得免疫を有するため小児ほど頻度は高くない[6]。
1980年には、何らかの胃腸炎によって460万例の小児が死亡しており、過半数が発展途上国で発生している[59]。しかし2000年までには死亡率が著明に減少している(年間死亡例約150万人)。これは経口補水液の導入と普及によるところが大きい[69]。アメリカ合衆国では胃腸炎感染が風邪に次いで2番目に多い感染症であり、2億〜3億7500万例が急性下痢を来たし[6][13]、年間約1万人が死亡している[13]そのうち150〜300例が5歳未満の小児である[1]。
| 病原体 | 腸炎ビブリオ | サルモネラ | カンピロバクター | O157などの腸管出血性大腸菌(EHEC) | 病原性大腸菌(腸管出血性大腸菌を除く) | 赤痢菌 | コレラ菌 | ノロウイルス | ロタウイルス |
|---|---|---|---|---|---|---|---|---|---|
| 病原因子 | 耐熱性溶血毒(TDH) | 腸管上皮細胞侵入 | 腸管上皮細胞侵入 | ベロ毒素(志賀毒素) | 腸管病原性大腸菌(EPEC)と腸管侵入性大腸菌(EIEC)は腸管上皮細胞侵入。毒素原性大腸菌(ETEC)はコレラトキシンに似た毒素を産生。 | 腸管上皮細胞侵入、ベロ毒素(志賀毒素) | コレラ毒素(コレラトキシン) | 腸管上皮細胞侵入 | 腸管上皮細胞侵入 |
| 感染源 | 魚介類 | ネズミ、家畜、鳥 | 鳥、家畜 | 家畜、ネズミ、感染者の糞便 | 感染者の糞便 | 飲料水、感染者の糞便、サル | 魚介類、飲料水、感染者の糞便 | 飲食物、感染者の糞便 | 感染者の糞便、おむつ |
| 原因食品 | 生の魚、貝類など | 生肉、鶏卵、サラダ | 鶏肉、豚肉、牛肉 | 種々の食品。特に生の牛肉が原因となることが多い。 | 種々の食品 | 飲料水、種々の食品 | 魚介類、種々の食品 | 種々の食品 | 食品からの感染は少ない。 |
| 潜伏期間 | 12〜24時間 | 1〜2日 | 2〜11日 | 3〜8日 | 12〜72時間 | 1〜5日 | 12時間〜5日 | 24〜48時間 | 1〜3日 |
| 主な症状 | 上腹部痛、下痢、嘔吐 | 発熱、腹痛、下痢、嘔吐 | 頭痛、腹痛、下痢、嘔吐 | 出血性大腸炎(下腹部痛、下痢、血便、風邪様症状) | 腹痛、下痢、嘔吐、発熱 | 下腹部痛、下痢、血便、発熱 | 水様性下痢、嘔吐、脱水症状 | 上腹部痛、嘔気、嘔吐、下痢 | 水様性下痢、嘔吐、発熱、脱水症状 |
| 腹痛 | 上腹部で強い | へそ周辺で強い | へそ周辺で強い | 下腹部で強い | EPECはへそ周辺で強い。EIECは下腹部で強い。ETECでは軽い。 | 下腹部で強い。ときに渋り腹(テネスムス)もあり。 | 軽い | 上腹部で強い | 上腹部で強い |
| 下痢便の性状 | 水様便、重症例では粘血便 | 水様便または粘血便 | 水様便または粘血便 | はじめ水様便、のちに血便 | EPECでは水様便が多い。EIECでは粘血便となることが多い。ETECでは真っ白い水様便が大量に出ることも。 | はじめ水様便、のちに膿粘血便 | 「米のとぎ汁」と形容されるほどの真っ白な水様便 | 水様便 | 水様便。重症例では真っ白い水様便が大量に出ることも。 |
| 血便(下血) | 重症例ではあり | あり | あり | 特に顕著に現れる。典型例では「糞便成分がほとんどなく、真っ赤な血液そのもの」といった状態で出てくる。 | EIECでは多い。EPECでも重症例ではあり。 | 顕著。血液だけでなく膿や粘液も混じる。典型例では糞便成分がほとんどなく、血液、膿、粘液のみを頻回に排泄するようになる。 | 胃腸炎自体ではなし。合併症として腸重積症を起こした場合はあり。 | ||
| 嘔吐 | 多い | あり | あり | 稀 | あり | 稀 | 多い | 激しい | 多い |
| 発熱 | ない、または軽度(37℃台) | 多い、ときに38℃以上の高熱になることも | あり | 軽度(37℃台)であることが多い | EPEC、EIECでは多い。ETECでは稀。 | あり | 稀 | ない、または軽度(37℃台) | 多い |
| 合併症 | 稀に心臓障害を起こすことがある | 敗血症、髄膜炎 | 敗血症、ギラン・バレー症候群 | 溶血性尿毒症症候群(HUS)、血栓性血小板減少性紫斑病(TTP) | 溶血性尿毒症症候群(HUS)、ライター症候群 | 脱水症状 | 脱水症状、腸重積症、肝炎、心筋炎、脳炎、ウイルス性急性脳症、腎不全 | ||
| 二次感染(ヒトからヒトへの伝染) | 稀 | あり | あり | あり | あり | 多い | あり | 多い | 多い |
| 予防法 | 魚介類の生食を避ける、食前加熱 | ネズミの駆除、鶏卵の生食を避ける、食前加熱、冷蔵冷凍、食前の手洗い | 肉類の生食を避ける、食前加熱、冷蔵冷凍、食前の手洗い | 肉類の生食を避ける、食前加熱、冷蔵冷凍、食前の手洗い、二次感染の防止 | ネズミの駆除、加熱殺菌 | 生ものや生水を避ける、加熱殺菌、冷凍冷蔵 | 生ものや生水を避ける、加熱殺菌、冷凍冷蔵 | 食前加熱、手洗い、うがい、二次感染の防止 | ロタウイルスワクチン接種 |
| 感染症法での扱い | 五類感染症 | 五類感染症。一部の菌株は三類感染症(腸チフス、パラチフス)。 | 五類感染症 | 三類感染症(腸管出血性大腸菌感染症) | 五類感染症 | 三類感染症(細菌性赤痢) | 三類感染症(コレラ | 五類感染症 | 五類感染症、基幹定点 |
| 備考 | コレラ菌と同じビブリオ属に分類される細菌である。 | 腸チフスおよびパラチフスを起こす菌株は感染症法で三類感染症に指定される。 | 合併症のHUSは致死率が高く、後遺症が残ることもある。 | 感染力が非常に強く、ごく少量の菌数でも感染が成立する。 | 腸炎ビブリオと同じビブリオ属に分類される細菌である。 | 乳幼児の重症胃腸炎の原因として重要な病原体。 |
研究
[編集]胃腸炎に対するワクチンが多数開発中である。細菌性胃腸炎の二大原因菌である赤痢菌や毒素原性大腸菌(ETEC)に対するワクチンが開発中である[70][71]。
ヒト以外の胃腸炎
[編集]ネコやイヌも病原体によって胃腸炎を発症する。特に頻繁にみられるのがカンピロバクター、クロストリジウム・ディフィシル、クロストリジウム・パーフリンジェンス、サルモネラ菌である[72]。また、有毒植物も胃腸炎の原因となる[73]。伝染性胃腸炎コロナウイルス (TGEV)はブタに感染する[74]。感染源は野鳥であると考えられており、特定の治療法はない[75]。ただし、ヒトへの感染性はない[76]。
脚注
[編集]- ^ a b c d e f g h i j k l m n o p q r s t u v w Singh, Amandeep (July 2010). “Pediatric Emergency Medicine Practice Acute Gastroenteritis — An Update”. Emergency Medicine Practice 7 (7).
- ^ 感染性胃腸炎(ノロウィルス等)│暮らしのガイド|島根県松江市
- ^ Tate JE, Burton AH, Boschi-Pinto C, Steele AD, Duque J, Parashar UD (February 2012). “2008 estimate of worldwide rotavirus-associated mortality in children younger than 5 years before the introduction of universal rotavirus vaccination programmes: a systematic review and meta-analysis”. The Lancet Infectious Diseases 12 (2): 136–41. doi:10.1016/S1473-3099(11)70253-5. PMID 22030330.
- ^ Marshall JA, Bruggink LD (April 2011). “The dynamics of norovirus outbreak epidemics: recent insights”. International Journal of Environmental Research and Public Health 8 (4): 1141–9. doi:10.3390/ijerph8041141. PMC 3118882. PMID 21695033.
- ^ Man SM (December 2011). “The clinical importance of emerging Campylobacter species”. Nature Reviews. Gastroenterology & Hepatology 8 (12): 669–85. doi:10.1038/nrgastro.2011.191. PMID 22025030.
- ^ a b c d e f g h i j k l m n Eckardt AJ, Baumgart DC (January 2011). “Viral gastroenteritis in adults”. Recent Patents on Anti-infective Drug Discovery 6 (1): 54–63. PMID 21210762.
- ^ a b c d e f g h i Webber, Roger (2009). Communicable disease epidemiology and control : a global perspective (3rd ed.). Wallingford, Oxfordshire: Cabi. p. 79. ISBN 978-1-84593-504-7
- ^ a b c d e Galanis, E (2007 Sep 11). “Campylobacter and 細菌性 gastroenteritis.”. CMAJ : Canadian Medical Association 177 (6): 570–1. doi:10.1503/cmaj.070660. PMC 1963361. PMID 17846438.
- ^ a b Meloni, A; Locci, D, Frau, G, Masia, G, Nurchi, AM, Coppola, RC (2011 Oct). “Epidemiology and prevention of rotavirus infection: an underestimated issue?”. The journal of maternal-fetal & neonatal medicine : the official journal of the European Association of Perinatal Medicine, the Federation of Asia and Oceania Perinatal Societies, the International Society of Perinatal Obstetricians 24 Suppl 2: 48–51. doi:10.3109/14767058.2011.601920. PMID 21749188.
- ^ “Toolkit”. DefeatDD. 2012年4月27日時点のオリジナルよりアーカイブ。2012年5月3日閲覧。
- ^ a b c d “Management of acute diarrhoea and vomiting due to gastoenteritis in children under 5”. National Institute of Clinical Excellence (2009年4月). 2009年6月11日閲覧。
- ^ a b c d e f Tintinalli, Judith E. (2010). Emergency Medicine: A Comprehensive Study Guide (Emergency Medicine (Tintinalli)). New York: McGraw-Hill Companies. pp. 830–839. ISBN 0-07-148480-9
- ^ a b c d e f g h i j k l m n o p q Mandell 2010 Chp. 93
- ^ a b c Elliott, EJ (2007 Jan 6). “Acute gastroenteritis in children.”. BMJ (Clinical research ed.) 334 (7583): 35–40. doi:10.1136/bmj.39036.406169.80. PMC 1764079. PMID 17204802.
- ^ a b c d Szajewska, H; Dziechciarz, P (2010 Jan). “Gastrointestinal infections in the pediatric population.”. Current opinion in gastroenterology 26 (1): 36–44. doi:10.1097/MOG.0b013e328333d799. PMID 19887936.
- ^ 山下育孝、服部昌志、大瀬戸光明 ほか、小児における腸管アデノウイルス胃腸炎の疫学 感染症学雑誌 69巻 (1995) 4号 p.377-382, doi:10.11150/kansenshogakuzasshi1970.69.377
- ^ Dennehy PH (January 2011). “Viral gastroenteritis in children”. The Pediatric Infectious Disease Journal 30 (1): 63–4. doi:10.1097/INF.0b013e3182059102. PMID 21173676.
- ^ 医学書院、今日の小児治療指針 第16版第11章「感染症,寄生虫症」-ウイルス性胃腸炎。20150901発行
- ^ a b c d e f g Webb, A; Starr, M (2005 Apr). “Acute gastroenteritis in children.”. Australian family physician 34 (4): 227–31. PMID 15861741.
- ^ Desselberger U, Huppertz HI (January 2011). “Immune responses to rotavirus infection and vaccination and associated correlates of protection”. The Journal of Infectious Diseases 203 (2): 188–95. doi:10.1093/infdis/jiq031. PMC 3071058. PMID 21288818.
- ^ 西尾治、秋山美穂、愛木智香子 ほか、ノロウイルスによる食中毒について 食品衛生学雑誌, 46, 235-245 (2005), doi:10.3358/shokueishi.46.235
- ^ Nyachuba, DG (2010 May). “Foodborne illness: is it on the rise?”. Nutrition Reviews 68 (5): 257-69. doi:10.1111/j.1753-4887.2010.00286.x. PMID 20500787.
- ^ a b Charles, RC; Ryan, ET (2011 Oct). “Cholera in the 21st century.”. Current opinion in infectious diseases 24 (5): 472-7. doi:10.1097/QCO.0b013e32834a88af. PMID 21799407.
- ^ Moudgal, V; Sobel, JD (2012 Feb). “Clostridium difficile colitis: a review.”. Hospital practice (1995) 40 (1): 139-48. doi:10.3810/hp.2012.02.954. PMID 22406889.
- ^ Lin, Z; Kotler, DP; Schlievert, PM; Sordillo, EM (2010 May). “Staphylococcal enterocolitis: forgotten but not gone?”. Digestive diseases and sciences 55 (5): 1200-7. PMID 19609675.
- ^ a b Leonard, J; Marshall, JK, Moayyedi, P (2007 Sep). “Systematic review of the risk of enteric infection in patients taking acid suppression.”. The American journal of gastroenterology 102 (9): 2047–56; quiz 2057. doi:10.1111/j.1572-0241.2007.01275.x. PMID 17509031.
- ^ a b c d Escobedo, AA; Almirall, P, Robertson, LJ, Franco, RM, Hanevik, K, Mørch, K, Cimerman, S (2010 Oct). “Giardiasis: the ever-present threat of a neglected disease.”. Infectious disorders drug targets 10 (5): 329–48. PMID 20701575.
- ^ Grimwood, K; Forbes, DA (2009 Dec). “Acute and persistent diarrhea.”. Pediatric clinics of North America 56 (6): 1343–61. doi:10.1016/j.pcl.2009.09.004. PMID 19962025.
- ^ Lawrence, DT; Dobmeier, SG; Bechtel, LK; Holstege, CP (2007 May). “Food poisoning.”. Emergency medicine clinics of North America 25 (2): 357-73; abstract ix. doi:10.1016/j.emc.2007.02.014. PMID 17482025.
- ^ Steiner, MJ; DeWalt, DA, Byerley, JS (2004 Jun 9). “Is this child dehydrated?”. JAMA : the Journal of the American Medical Association 291 (22): 2746–54. doi:10.1001/jama.291.22.2746. PMID 15187057.
- ^ a b c Warrell D.A., Cox T.M., Firth J.D., Benz E.J., ed (2003). The Oxford Textbook of Medicine (4th ed.). Oxford University Press. ISBN 0-19-262922-0. オリジナルの2012年3月21日時点におけるアーカイブ。
- ^ “Viral Gastroenteritis”. Center for Disease Control and Prevention (2011年2月). 2012年4月24日時点のオリジナルよりアーカイブ。2012年4月16日閲覧。
- ^ a b c World Health Organization (December 2009). “Rotavirus vaccines: an update”. Weekly epidemiological record 51–52 (84): 533–540 10 May 2012閲覧。.
- ^ Giaquinto, C; Dominiak-Felden G, Van Damme P, Myint TT, Maldonado YA, Spoulou V, Mast TC, Staat MA (2011 July). “Summary of effectiveness and impact of rotavirus vaccination with the oral pentavalent rotavirus vaccine: a systematic review of the experience in industrialized countries”. Human Vaccines. 7 7: 734–748. doi:10.4161/hv.7.7.15511. PMID 21734466 10 May 2012閲覧。.
- ^ Jiang, V; Jiang B, Tate J, Parashar UD, Patel MM (July 2010). “Performance of rotavirus vaccines in developed and developing countries”. Human Vaccines 6 (7): 532–542. PMID 20622508 10 May 2012閲覧。.
- ^ Patel, MM; Steele, D, Gentsch, JR, Wecker, J, Glass, RI, Parashar, UD (2011 Jan). “Real-world impact of rotavirus vaccination.”. The Pediatric Infectious Disease Journal 30 (1 Suppl): S1-5. doi:10.1097/INF.0b013e3181fefa1f. PMID 21183833.
- ^ US Center for Disease Control and Prevention (2008). “Delayed onset and diminished magnitude of rotavirus activity—United States, November 2007 – May 2008”. Morbidity and Mortality Weekly Report 57 (25): 697–700 3 May 2012閲覧。.
- ^ “Reduction in rotavirus after vaccine introduction—United States, 2000–2009”. MMWR Morb. Mortal. Wkly. Rep. 58 (41): 1146–9. (October 2009). PMID 19847149.
- ^ Tate, JE; Cortese, MM, Payne, DC, Curns, AT, Yen, C, Esposito, DH, Cortes, JE, Lopman, BA, Patel, MM, Gentsch, JR, Parashar, UD (2011 Jan). “Uptake, impact, and effectiveness of rotavirus vaccination in the United States: review of the first 3 years of postlicensure data.”. The Pediatric Infectious Disease Journal 30 (1 Suppl): S56-60. doi:10.1097/INF.0b013e3181fefdc0. PMID 21183842.
- ^ Sinclair, D; Abba, K, Zaman, K, Qadri, F, Graves, PM (2011 Mar 16). “Oral vaccines for preventing cholera.”. Cochrane database of systematic reviews (Online) (3): CD008603. doi:10.1002/14651858.CD008603.pub2. PMID 21412922.
- ^ Alhashimi D, Al-Hashimi H, Fedorowicz Z (2009). Alhashimi, Dunia. ed. “Antiemetics for reducing vomiting related to acute gastroenteritis in children and adolescents”. Cochrane Database Syst Rev (2): CD005506. doi:10.1002/14651858.CD005506.pub4. PMID 19370620.
- ^ Tytgat GN (2007). “Hyoscine butylbromide: a review of its use in the treatment of abdominal cramping and pain”. Drugs 67 (9): 1343–57. PMID 17547475.
- ^ “BestBets: Fluid Treatment of Gastroenteritis in Adults”. 2008年12月20日閲覧。
- ^ Canavan A, Arant BS (October 2009). “Diagnosis and management of dehydration in children”. Am Fam Physician 80 (7): 692–6. PMID 19817339.
- ^ Gregorio GV, Gonzales ML, Dans LF, Martinez EG (2009). Gregorio, Germana V. ed. “Polymer-based oral rehydration solution for treating acute watery diarrhoea”. Cochrane Database Syst Rev (2): CD006519. doi:10.1002/14651858.CD006519.pub2. PMID 19370638.
- ^ 軽症胃腸炎の小児には希釈したリンゴジュース 電解質入りの経口補水液より治療失敗が少ない 日経メディカルオンライン 2016/5/30
- ^ a b c d King CK, Glass R, Bresee JS, Duggan C (November 2003). “Managing acute gastroenteritis among children: oral rehydration, maintenance, and nutritional therapy”. MMWR Recomm Rep 52 (RR-16): 1–16. PMID 14627948.
- ^ Allen SJ, Martinez EG, Gregorio GV, Dans LF (2010). Allen, Stephen J. ed. “Probiotics for treating acute infectious diarrhoea”. Cochrane Database Syst Rev 11 (11): CD003048. doi:10.1002/14651858.CD003048.pub3. PMID 21069673.
- ^ Hempel, S; Newberry, SJ; Maher, AR; Wang, Z; Miles, JN; Shanman, R; Johnsen, B; Shekelle, PG (2012 May 9). “Probiotics for the prevention and treatment of antibiotic-associated diarrhea: a systematic review and meta-analysis.”. JAMA: the Journal of the American Medical Association 307 (18): 1959-69. PMID 22570464.
- ^ Mackway-Jones, Kevin (2007年6月). “Does yogurt decrease acute diarrhoeal symptoms in children with acute gastroenteritis?”. BestBets. 2008年12月18日閲覧。
- ^ Telmesani, AM (2010 May). “Oral rehydration salts, zinc supplement and rota virus vaccine in the management of childhood acute diarrhea.”. Journal of family and community medicine 17 (2): 79–82. doi:10.4103/1319-1683.71988. PMC 3045093. PMID 21359029.
- ^ DeCamp LR, Byerley JS, Doshi N, Steiner MJ (September 2008). “Use of antiemetic agents in acute gastroenteritis: a systematic review and meta-analysis”. Arch Pediatr Adolesc Med 162 (9): 858–65. doi:10.1001/archpedi.162.9.858. PMID 18762604.
- ^ Mehta S, Goldman RD (2006). “Ondansetron for acute gastroenteritis in children”. Can Fam Physician 52 (11): 1397–8. PMC 1783696. PMID 17279195.
- ^ a b Fedorowicz, Z; Jagannath, VA, Carter, B (2011 Sep 7). “Antiemetics for reducing vomiting related to acute gastroenteritis in children and adolescents.”. Cochrane database of systematic reviews (Online) 9 (9): CD005506. doi:10.1002/14651858.CD005506.pub5. PMID 21901699.
- ^ Sturm JJ, Hirsh DA, Schweickert A, Massey R, Simon HK (May 2010). “Ondansetron use in the pediatric emergency department and effects on hospitalization and return rates: are we masking alternative diagnoses?”. Ann Emerg Med 55 (5): 415–22. doi:10.1016/j.annemergmed.2009.11.011. PMID 20031265.
- ^ “Ondansetron”. Lexi-Comp (2011年5月). 2012年4月16日閲覧。
- ^ Traa BS, Walker CL, Munos M, Black RE (April 2010). “Antibiotics for the treatment of dysentery in children”. Int J Epidemiol 39 (Suppl 1): i70–4. doi:10.1093/ije/dyq024. PMC 2845863. PMID 20348130.
- ^ Grimwood K, Forbes DA (December 2009). “Acute and persistent diarrhea”. Pediatr. Clin. North Am. 56 (6): 1343–61. doi:10.1016/j.pcl.2009.09.004. PMID 19962025.
- ^ a b Mandell, Gerald L.; Bennett, John E.; Dolin, Raphael (2004). Mandell's Principles and Practices of Infection Diseases (6th ed.). Churchill Livingstone. ISBN 0-443-06643-4
- ^ Christopher, PR; David, KV, John, SM, Sankarapandian, V (2010 Aug 4). “Antibiotic therapy for Shigella dysentery.”. Cochrane database of systematic reviews (Online) (8): CD006784. doi:10.1002/14651858.CD006784.pub4. PMID 20687081.
- ^ Effa, EE; Lassi, ZS, Critchley, JA, Garner, P, Sinclair, D, Olliaro, PL, Bhutta, ZA (2011 Oct 5). “Fluoroquinolones for treating typhoid and paratyphoid fever (enteric fever).”. Cochrane database of systematic reviews (Online) (10): CD004530. doi:10.1002/14651858.CD004530.pub4. PMID 21975746.
- ^ Gonzales, ML; Dans, LF, Martinez, EG (2009 Apr 15). “Antiamoebic drugs for treating amoebic colitis.”. Cochrane database of systematic reviews (Online) (2): CD006085. doi:10.1002/14651858.CD006085.pub2. PMID 19370624.
- ^ Harrison's Principles of Internal Medicine (16th ed.). McGraw-Hill. ISBN 0-07-140235-7. オリジナルの2012年8月4日時点におけるアーカイブ。
- ^ Feldman, Mark; Friedman, Lawrence S.; Sleisenger, Marvin H. (2002). Sleisenger & Fordtran's Gastrointestinal and Liver Disease (7th ed.). Saunders. ISBN 0-7216-8973-6
- ^ Elliott, EJ (2007 Jan 6). “Acute gastroenteritis in children.”. BMJ (Clinical research ed.) 334 (7583): 35–40. doi:10.1136/bmj.39036.406169.80. PMC 1764079. PMID 17204802.
- ^ Black, RE; Cousens, S, Johnson, HL, Lawn, JE, Rudan, I, Bassani, DG, Jha, P, Campbell, H, Walker, CF, Cibulskis, R, Eisele, T, Liu, L, Mathers, C, Child Health Epidemiology Reference Group of WHO and, UNICEF (2010 Jun 5). “Global, regional, and national causes of child mortality in 2008: a systematic analysis.”. Lancet 375 (9730): 1969–87. doi:10.1016/S0140-6736(10)60549-1. PMID 20466419.
- ^ Tate, JE; Burton, AH, Boschi-Pinto, C, Steele, AD, Duque, J, Parashar, UD, WHO-coordinated Global Rotavirus Surveillance, Network (2012 Feb). “2008 estimate of worldwide rotavirus-associated mortality in children younger than 5 years before the introduction of universal rotavirus vaccination programmes: a systematic review and meta-analysis.”. The Lancet infectious diseases 12 (2): 136–41. doi:10.1016/S1473-3099(11)70253-5. PMID 22030330.
- ^ World Health Organization (November 2008). “Global networks for surveillance of rotavirus gastroenteritis, 2001–2008”. Weekly Epidemiological Record 47 (83): 421–428 10 May 2012閲覧。.
- ^ Victora CG, Bryce J, Fontaine O, Monasch R (2000). “Reducing deaths from diarrhoea through oral rehydration therapy”. Bull. World Health Organ. 78 (10): 1246–55. PMC 2560623. PMID 11100619.
- ^ World Health Organization. “Enterotoxigenic Escherichia coli (ETEC)”. Diarrhoeal Diseases. 3 May 2012閲覧。
- ^ World Health Organization. “Shigellosis”. Diarrhoeal Diseases. 3 May 2012閲覧。
- ^ Weese, JS (2011 Mar). “細菌性 enteritis in dogs and cats: diagnosis, therapy, and zoonotic potential.”. The Veterinary clinics of North America. Small animal practice 41 (2): 287-309. doi:10.1016/j.cvsm.2010.12.005. PMID 21486637.
- ^ Rousseaux, Wanda Haschek, Matthew Wallig, Colin (2009). Fundamentals of toxicologic pathology (2nd ed. ed.). London: Academic. pp. 182. ISBN 9780123704696
- ^ MacLachlan, edited by N. James; Dubovi, Edward J. (2009). Fenner's veterinary virology (4th ed. ed.). Amsterdam: Elsevier Academic Press. p. 399. ISBN 9780123751584
- ^ al.], edited by James G. Fox ... [et (2002). Laboratory animal medicine (2nd ed. ed.). Amsterdam: Academic Press. pp. 649. ISBN 9780122639517
- ^ al.], edited by Jeffrey J. Zimmerman ... [et. Diseases of swine (10th ed. ed.). Chichester, West Sussex: Wiley-Blackwell. pp. 504. ISBN 9780813822679
- Notes
- Dolin, [edited by] Gerald L. Mandell, John E. Bennett, Raphael (2010). Mandell, Douglas, and Bennett's principles and practice of infectious diseases (7th ed. ed.). Philadelphia, PA: Churchill Livingstone/Elsevier. ISBN 0-443-06839-9
参考文献
[編集]- 冬季に流行する胃腸カゼ(感染性胃腸炎) - 愛知県衛生研究所
関連項目
[編集]外部リンク
[編集]- 感染性胃腸炎(ノロウイルスを中心に) 東京都感染症情報センター
