ジボラン(4)
表示
| ジボラン(4) | |
|---|---|
| |
| 識別情報 | |
| CAS登録番号 | 18099-45-1 |
| PubChem | 29529 |
| ChEBI | |
| Gmelin参照 | 24760 |
| |
| |
| 特性 | |
| 化学式 | H4B2 |
| モル質量 | 25.65 g mol−1 |
| 関連する物質 | |
| 関連物質 | ビス(ピナコラート)ジボロン 四フッ化ジボロン テラヒドロキシジボロン |
| 特記なき場合、データは常温 (25 °C)・常圧 (100 kPa) におけるものである。 | |
ジボラン(4)(系統名: di-μH-catena-diborane(4)、di-μ-hydrido-bis(hydridoboron)(B—B))は、化学式B2H4を持つ無機化合物である[1][2]。
構造と結合
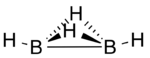
[編集]計算化学研究はホウ素-ホウ素結合を含む2つの構造を予測する。基底状態では、それぞれのホウ素原子に付いた一つの「末端」水素原子に加えて、三中心二電子結合を介して2つのホウ素原子を繋ぐ2つの水素原子が存在する。ホウ素–ホウ素結合の電子はこれら2つの原子間の領域に異常に局在化しており、水素原子のブリッジから離れたB–B軸の側に著しい負電荷を作り出している。この非核吸引子が電子供与体として他分子との相互作用に関与しているかもしれない[2]。

励起状態では、2つの水素原子がより伝統的な(二中心二電子)共有結合によってそれぞれのホウ素原子に付いている。ホウ素–ホウ素結合のみが2つのホウ素原子を繋ぎ、1つのホウ素上の水素原子はもう一方と比べてねじれている[2]。
生成
[編集]ジボラン(4) を作り出す唯一既知の方法は、原子状フッ素を用いたジボラン(6)からの水素の連続的引き抜きである[1]。ジボラン(4) の構造は確認されていないが、光イオン化質量分析によって得られた結果は二重に橋渡しさえれた構造と一致している[1]。
複数のジボラン(4) の置換誘導体が観測されている[3][4]。
脚注
[編集]- ^ a b c Ruščic, B.; Schwarz, M.; Berkowitz, J. (1989). “Molecular structure and thermal stability of B2H4 and B2H+
4 species”. J. Chem. Phys. (AIP Publishing) 91 (8): 4576–4581. doi:10.1063/1.456745. - ^ a b c Alkorta, Ibon; Soteras, Ignacio; Elguero, José; Del Beneb, Janet E. (2011). “The boron–boron single bond in diborane(4) as a non-classical electron donor for hydrogen bonding”. Phys. Chem. Chem. Phys. 13 (31): 14026–14032. doi:10.1039/C1CP20560A.
- ^ Xie, Xiaochen; Haddow, Mairi F.; Mansell, Stephen M.; Norman, Nicholas C.; Russell, Christopher A. (2012). “Diborane(4) compounds with bidentate diamino groups”. Dalton Transactions 41 (7): 2140–7. doi:10.1039/C2DT11936F. PMID 22187045.
- ^ Wagner, Arne; Kaifer, Elisabeth; Himmel, Hans-Jörg (2012). “Diborane(4)–metal bonding: Between hydrogen bridges and frustrated oxidative addition”. Chem. Commun. 48 (43): 5277–9. doi:10.1039/C2CC31671D. PMID 22526934.
