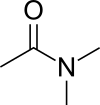
ジメチルアセトアミド
表示
| ジメチルアセトアミド | |
|---|---|
| |

| |
N,N-Dimethylacetamide | |
| 識別情報 | |
| 略称 | DMA, DMAC, DMAc[1] |
| CAS登録番号 | 127-19-5 |
| PubChem | 31374 |
| ChemSpider | 29107 |
| UNII | JCV5VDB3HY |
| EC番号 | 204-826-4 |
| MeSH | dimethylacetamide |
| ChEBI | |
| ChEMBL | CHEMBL11873 |
| RTECS番号 | AB7700000 |
| バイルシュタイン | 1737614 |
| |
| 特性 | |
| 化学式 | C4H9NO |
| モル質量 | 87.12 g mol−1 |
| 外観 | 無色の液体 |
| 匂い | アンモニア臭 |
| 密度 | 0.937 g/mL |
| 融点 |
−20 °C |
| 沸点 |
165 °C |
| 水への溶解度 | 混和 |
| log POW | −0.253 |
| 蒸気圧 | 300 Pa |
| λmax | 270 nm |
| 屈折率 (nD) | 1.4375 |
| 粘度 | 0.945 mPa·s [2] |
| 熱化学 | |
| 標準生成熱 ΔfH |
−300.1 kJ/mol |
| 標準燃焼熱 ΔcH |
−2.5835–−2.5805 MJ/mol |
| 標準定圧モル比熱, Cp |
178.2 J/(K·mol) |
| 危険性 | |
| GHSピクトグラム |  
|
| GHSシグナルワード | DANGER |
| Hフレーズ | H312, H319, H332, H360 |
| Pフレーズ | P280, P308+313 |
| NFPA 704 | |
| 引火点 | 63 °C (145 °F; 336 K) |
| 発火点 | 490 °C (914 °F; 763 K) |
| 爆発限界 | 1.8–11.5% |
| 許容曝露限界 | TWA 10 ppm (35 mg/m3) [皮膚][4] |
| 半数致死量 LD50 | 2.24 g/kg (皮膚, ウサギ) 4.3 g/kg (経口, ラット) 4.8 g/kg (経口, ラット) 4.62 g/kg (経口, マウス)[3] |
| 半数致死濃度 LC50 | 2475 ppm (ラット, 1時間)[3] |
| 関連する物質 | |
| 関連物質 | |
| 特記なき場合、データは常温 (25 °C)・常圧 (100 kPa) におけるものである。 | |
ジメチルアセトアミドは化学式C4H9NOで表される有機化合物である。N,N-ジメチルアセトアミドとも呼ばれ、DMAやDMAcと略されることがある。 無色で水に可溶であり、吸湿性を持つ。高沸点の極性溶媒として、有機合成化学において広く用いられる。アルコールやエーテル、ケトン、ハロゲン化物や芳香族などの他の溶媒とも容易に混ざる。しかし、脂肪族炭化水素とはほとんど混ざらない。
- CH3CON(CH3)2 + H2O + HCl → CH3COOH + (CH3)2NH·HCl
またナトリウムメトキシドなど強塩基を用いる反応の溶媒にしばしば用いられる[5]。
工業的にもよく用いられる溶媒であるが、人体に有害であり、吸入や皮膚の接触は避けなければならない。発がん性や催奇性があると疑われている。日本では消防法により危険物第4類に指定されている。
出典
[編集]- ^ Munro, D. D.; Stoughton, R. B. (1965). “Dimethylacetamide (DMAC) and Dimethylformamide (DMFA). Effect on Percutaneous Absorption”. Archives of Dermatology 92 (5): 585–586. doi:10.1001/archderm.1965.01600170101020. PMID 5844405.
- ^ Iloukhani, H., K. Khanlarzadeh. "Densities, viscosities, and refractive indices for binary and ternary mixtures of N, N-dimethylacetamide (1)+ 2-methylbutan-2-ol (2)+ ethyl acetate (3) at 298.15 K for m liquid region and at ambient pressure". Journal of Chemical & Engineering Data, 51.4 (2006): 1226–1231. doi:10.1021/je050538q.
- ^ a b “Dimethyl acetamide”. 生活や健康に直接的な危険性がある. アメリカ国立労働安全衛生研究所(NIOSH). 2025年1月5日閲覧。
- ^ NIOSH Pocket Guide to Chemical Hazards 0218
- ^ S. Zen, E. Kaji, Organic Syntheses, Coll. Vol. 6, p.503, 1988 (Vol. 57, p.60, 1977). (オンライン版)

