パゴダン
この項目「パゴダン」は翻訳されたばかりのものです。不自然あるいは曖昧な表現などが含まれる可能性があり、このままでは読みづらいかもしれません。(原文:en:Pagodane) 修正、加筆に協力し、現在の表現をより自然な表現にして下さる方を求めています。ノートページや履歴も参照してください。(2016年7月) |
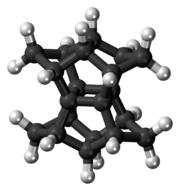
| [1.1.1.1]パゴダン | |
|---|---|

| |
| |
| 識別情報 | |
| CAS登録番号 | 89683-62-5 |
| PubChem | 145202 |
| ChemSpider | 128087 |
| |
| 特性 | |
| 化学式 | C20H20 |
| モル質量 | 260.37 g mol−1 |
| 密度 | 1.629 g/ml |
| 構造 | |
| 双極子モーメント | 0 D |
| 特記なき場合、データは常温 (25 °C)・常圧 (100 kPa) におけるものである。 | |
パゴダン (Pagodane) は、分子式 C20H20 の有機化合物である。パゴダに似た炭素骨格に因んで名付けられた[2]。D2h の分子対称性をもつ多環式炭化水素である。結晶性の高い固体で、243 °C の融点を示す。ほとんどの有機溶媒にほぼ溶けないが、ベンゼンとクロロホルムには若干溶ける。低圧下においては昇華する[3]。
パゴダンという名前は、広義には同様の16炭素中心かご型分子骨格を持つ一連の化合物群の基礎化合物として用いられる。各化合物は、このかごの8つの原子が4つのアルカン鎖によって繋がれたものと見ることができる。広義のパゴダン型化合物は、m, n, p, q をそれぞれ4つの鎖に含まれる炭素原子の数として、[m.n.p.q]パゴダンのように名付けられる。一般分子式は s= m+n+p+q として、C16+sH12+2s と表わすことができる。具体的には、基礎化合物 C20H20 においては4つのメチレン基 (m=n=p=q=1) によって繋がれているため、広義のパゴダンとしての名前は [1.1.1.1]パゴダンとなる[3]。
合成と構造
[編集]1987年、プリンツバッハらにより、イソドリンを出発物質とする14段合成法により始めて合成された[3]。この合成法では、[2.2.1.1]パゴダン C22H24 やその他の派生物も合成される。
プリンツバッハと共同研究者は、パゴダンという慣用名の必要は、ウンデカシクロ[9.9.0.01,5.02,12.02,18.03,7.06,10.08,12.011,15.013,17.016,20]イコサンというIUPAC名を見れば一目瞭然だろうと述べている[3]。
パゴダンの炭素骨格中には、多数のプロペラン型部分構造が見られる[3]。
 |
この図に描かれた合成法は、全体収率 24% の14段ワンポット合成法に短縮することができる。しかし、その方法では初期段に二回使用されているテトラクロロジメトキシシクロペンタジエンの代わりにテトラクロロチオフェンジオキシドを使う必要がある。より段数が短く収率も高いように見えるが、ジオキシドの高いコストと入手性の悪さから用いられなくなった[3]。
誘導体
[編集]ジケトン C20H16O2 (融点 ~322 °C)など、いくつかの誘導体が知られている[3]。
[1.1.1.1]パゴダンと[2.2.1.1]パゴダンの両者ともに、 SbF5/SO2ClF 中で二価のカチオンを形成する。これらのカチオンにおいては、電子欠乏は中心のシクロブタン環上に拡がっている[5] [6]。これらのジカチオンは、後にプリンツバッハらが長年にわたり研究することとなる、σ-ビスホモ芳香族の最初の例となった[7]。
パゴダンはドデカヘドランの異性体であり、化学的に異性化させることができる[8] [9]。
出典
[編集]- ^ “Pagodane | C20H20”. ChemSpider. 2016年7月19日閲覧。
- ^ Elegant Solutions: Ten Beautiful Experiments in Chemistry Philip Ball RSC 2005
- ^ a b c d e f g h Wolf-Dieter Fessner, Gottfried Sedelmeier, Paul R. Spurr, Grety Rihs, H. Prinzbach (1987), "Pagodane": the efficient synthesis of a novel, versatile molecular framework. J. Am. Chem. Soc., volume 109 issue 15, pp. 4626–42 doi:10.1021/ja00249a029
- ^ H. Prinzbach, F. Wahl, A. Weiler, P. Landenberger, J. Woerth, L.T. Scott, M. Gelmont, D. Olevano, F. Sommer, B. von Issendorff: C20 Carbon Clusters: Fullerene - Boat - Sheet Generation, Mass Selection, PE Characterization. Chem. Eur. J. 2006, 12, 6268-6280 | doi:10.1002/chem.200501611
- ^ G. K. Surya Prakash (1998), Investigations on intriguing long lived carbodications. Pure & Appl. Chem., volume 70 issue 10, pp. 2001–06. Online version at iupac.org accessed on 2010-01-14. doi:10.1351/pac199870102001
- ^ Stable carbocations. Part 267. Pagodane dication, a unique 2.pi.-aromatic cyclobutanoid system G. K. Prakash, V. V. Krishnamurthy, Rainer. Herges, Robert. Bau, Hanna. Yuan, George A. Olah, Wolf Dieter. Fessner, and Horst. Prinzbach Journal of the American Chemical Society 1986 108 (4), 836-838 doi:10.1021/ja00264a046
- ^ G.K.S. Prakash, V.V. Krishnamurthy, R. Herges, R. Bau, H. Yuan, G.A Olah, W.-D. Fessner, H. Prinzbach: [1.1.1.1]- and [2.2.1.1]Pagodane Dications: Frozen Two-Electron Woodward-Hoffmann Transition State Models. J. Am. Chem. Soc. 1988, 110, 7764-7772
- ^ Wolf-Dieter Fessner, Bulusu A. R. C. Murty, Horst Prinzbach (1987), The Pagodane Route to Dodecahedranes – Thermal, Reductive, and Oxidative Transformations of Pagodanes Angewandte Chemie International Edition in English Volume 26, Issue 5, pp. 451–52 doi:10.1002/anie.198704511
- ^ Wolf-Dieter Fessner, Bulusu A. R. C. Murty, Jürgen Wörth, Dieter Hunkler, Hans Fritz, Horst Prinzbach, Wolfgang D. Roth, Paul von Ragué Schleyer, Alan B. McEwen, Wilhelm F. Maier (1987), Dodecahedranes from [1.1.1.1]Pagodanes. Angewandte Chemie International Edition in English, Volume 26, Issue 5, pp. 452–54 doi:10.1002/anie.198704521
