モネリン
| Monellin Chain A and B | |
|---|---|
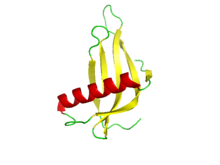 一本鎖モネリンのリボンモデル[1] | |
| 識別子 | |
| 略号 | MNEI |
| PDB | 2O9U (RCSB PDB PDBe PDBj) |
| UniProt | P02882 |
モネリン(Monellin)は甘味を持つタンパク質の一種。1969年に、西アフリカ原産のツヅラフジ科のつる植物であるディオスコレオフィルム・ヴォルケンシー(Dioscoreophyllum volkensii)の果実から発見された。当初は糖の一種と考えられていたが[2]、1972年に米国フィラデルフィアのモネル研究所 (Monell Chemical Senses Center) で単離され、タンパク質と同定された。モネリンの名はこの研究所にちなむ[3]。
タンパク質組成
[編集]モネリンの分子量は10.7kDaである。非共有結合である2本ポリペプチド鎖、44のアミノ酸残基であるA鎖と50のアミノ酸残基であるB鎖より成る[3][4]。
A鎖
REIKGYEYQL YVYASDKLFR ADISEDYKTR GRKLLRFNGP VPPP
B鎖
GEWEIIDIGP FTQNLGKFAV DEENKIGQYG RLTFNKVIRP CMKKTIYEEN
モネリンは二次構造として、逆平行βシート構造を構成する5本のβストランドと、17のアミノ酸残基よりなるαヘリックスを持つ[1]。未変性の状態ではモネリンは前述の二本鎖より成るが、この二本鎖構造は高温や極端なpH条件に対して不安定である[1]。安定性を高めるため、二本鎖をグリシン-フェニルアラニンのジペプチドで結合した一本鎖モネリンも作成されている[1]。このタンパク質(MNEI)はNMRやX線回折による分析が行われている。冒頭のリボンモデルは、1.15Åの解像度で得られたX線回折像を元に作成されたものである[1]。
二次構造に加え、モネリン分子の表面には安定的に結合した4つの硫酸イオンが存在している。うち3つは凹部に、残りの一つはタンパク質分子の凸部に結合している[1]。この凸部にある一つは、負に帯電した甘味受容体T1R2/T1R3と静電気的な相互作用をするとされているモネリン分子の正の帯電部分近傍に位置しているため、特に注目されている[1]。
甘味特性
[編集]モネリンはヒトおよび一部のオナガザル科の霊長類に対しては甘みを感じさせるが、その他の哺乳類には好まれない[1]。砂糖の主成分であるスクロースに比べ800倍から2000倍(甘味の評価法により異なる)の甘さを持ち、重量ベースでは5%のショ糖溶液の800倍[7]、7%ショ糖溶液の1500倍から2000倍の甘みを持つとの報告がある[8][9]。甘みの発現は遅く、長時間にわたり後味が生じる。モネリンの甘さはミラクリンと同様にpHに依存し、pHが2未満もしくは9以上の場合は無味である。モネリンとその他の強い甘味料を併用することにより、後味を軽減させ、甘みの相乗効果を得ることができる[10]。低pH条件下で50℃以上に加熱すると、モネリンは変性し甘味を喪失する[10]。
甘味料としての利用
[編集]モネリンは親水性・水溶性のタンパク質であるため、一部の食品や飲み物の甘味料としては有用である。しかし高温で変性するため、加工食品への用途は限られる。糖尿病などにより糖分の摂取を制限されている患者向けの卓上用の甘味料としては、有用である可能性がある[1]。D. volkensii は栽培が難しいため、モネリンを果実から抽出すると高価になってしまう。従って代替として化学合成や微生物を用いた製造法が研究されている。例えば酵母の一種である Candida utilis ではモネリンの発現に成功しており[11]、また固相法を用いた合成も行われている[12]。酵母によって産生された合成モネリンは、砂糖の0.6%溶液に比べ4000倍甘いことが判明している。モネリン普及の障壁となっているものは主に法律上の制限であり、EUやアメリカでは認可されていない。
関連項目
[編集]強い甘みを持つタンパク質として、モネリン(1969年発見)のほか ソーマチン (thaumatin) (1972年)、ペンタジン (pentadin) (1989年)、マビンリン (mabinlin) (1983年)、ブラゼイン (brazzein) (1994年)が発見されている[13]。
脚注
[編集]- ^ a b c d e f g h i PDB: 2O9U; Hobbs JR, Munger SD, Conn GL (March 2007). “Monellin (MNEI) at 1.15 A resolution”. Acta Crystallogr. Sect. F Struct. Biol. Cryst. Commun. 63 (Pt 3): 162–7. doi:10.1107/S1744309107005271. PMC 2330190. PMID 17329805.
- ^ GE Inglett, JF May. Serendipity berries - Source of a new intense sweetener. J Food Sci 1969, 34:408-411.
- ^ a b Morris JA, Martenson R, Deibler G, Cagan RH (January 1973). “Characterization of monellin, a protein that tastes sweet”. J. Biol. Chem. 248 (2): 534–9. PMID 4684691.
- ^ Ogata C, Hatada M, Tomlinson G, Shin WC, Kim SH (1987). “Crystal structure of the intensely sweet protein monellin”. Nature 328 (6132): 739–42. doi:10.1038/328739a0. PMID 3614382.
- ^ UniProtKB/Swiss-Prot database entry #P02881
- ^ UniProtKB/Swiss-Prot database entry #P02882
- ^ US patent 4122205, Burge MLE, Nechutny Z, "Sweetening compositions containing protein sweeteners", issued 1978-10-24
- ^ Kim NC, Kinghorn AD (December 2002). “Highly sweet compounds of plant origin”. Arch. Pharm. Res. 25 (6): 725–46. doi:10.1007/BF02976987. PMID 12510821.
- ^ Gelardi, Robert C.; Nabors, Lyn O'Brien (1991). Alternative sweeteners. New York: M. Dekker. ISBN 0-8247-8475-8
- ^ a b Nabors, Lyn O'Brien; Lyn O'Brien-Nabors (2001). Alternative sweeteners / edited by Lyn O'Brien Nabors. New York, N.Y: Marcel Dekker. ISBN 0-8247-0437-1
- ^ XL Zhang, T Ito, K Kondo, T Kobayashi and H Honda. Production of single chain recombinant monellin by high cell density culture of genetically engineered Candida utilis using limited feeding of sodium ions. Journal of Chemical Engineering of Japan 2002. 35: 654-659.
- ^ M Kohmura, T Mizukoshi, N Nio, EI Suzuki and Y Ariyoshi. Structure–taste relationships of the sweet protein monellin. Pure Appl. Chem., Vol. 74, 1235-1242, 2002.
- ^ Biopolymers. Volume 8. Polyamides and Complex Proteinaceous Materials II. Sweet-tasting Proteins. I Faus and H Sisniega. p203-209. 2004. Eds. Wiley-VCH. ISBN 3-527-30223-9.
