共役系


化学における共役系(きょうやくけい、英: conjugated system)は、化合物中に交互に位置する単結合および多重結合に非局在化電子を持つ結合p軌道系である。共役系は一般的に、分子全体のエネルギーを低下させ、安定性を高める。非共有電子対やラジカル、カルベニウムイオンなども共役系の一部となりうる。化合物は環状、非環状、線状あるいはこれらの混合物である。
共役は、間に存在するσ結合を越えたp軌道同士の重なり合いである(重原子ではd軌道も関与できる)[1]。
共役系は、間の単結合により橋渡しされた、p軌道が重なり合った領域である。共役系によって、全ての隣接し整列したp軌道に渡ってπ電子が非局在化している[2]。π電子は、単一の結合あるいは原子ではなく、原子のグループに属している。
「最大」の共役系はグラファイトや導電性高分子、カーボンナノチューブ(バックミンスターフラーレンに由来する)で見られる。
機構
[編集]
共役は、交互の単結合および二重結合によって起こり得るが、他の方法でも起こる。鎖中のそれぞれの近接した原子が利用可能なp軌道を有していれば、その系は共役していると考えることができる。例えば、フラン(図)は2つの交互の二重結合と1位に一つの酸素原子を持つ五員環である。酸素原子は2つの孤立電子対を持ち、そのうち1つがその位置におけるp軌道を占有していることによって、五員環の共役を維持している。環上の窒素原子あるいは環のα位に位置するカルボニル基 (C=O) 、イミノ基 (C=N)、ビニル基 (C=C) 、アニオンの様な官能基の存在もまた、共役の維持に寄与するp軌道の供与体として十分である。
共役環式化合物
[編集]
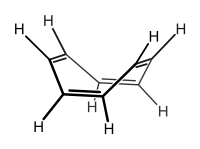
環式化合物は、部分的あるいは完全に共役することができる。完全に共役した単環性炭化水素であるアヌレンは、芳香族性、非芳香族性、反芳香族性を示す。
芳香族化合物
[編集]ヒュッケル則を満たす共役、平面、環式化合物は芳香族であり、並外れた安定性を示す。古典的な例であるベンゼンは、6個の電子が平面の環の上下に存在する系である。
非芳香族化合物
[編集]交互に存在する二重結合および単結合を持つ全ての化合物が芳香族性を示す訳ではない。例えば、シクロオクタテトラエンは交互の単結合および二重結合を有しており、通常「桶」型の配座をとっている。このような非平面上分子ではp軌道がよく整列しないため、炭素原子環で電子を容易に共有することができない。分子は共役していると考えられるが、芳香族でも反芳香族でもない(分子が平面でないため)。
色素における共役系
[編集]共役系は強い色を呈する特色がある。多くの色素は共役系を利用している。例えばβ-カロテン中の共役長炭化水素は強いオレンジ色を呈する。共役系中の電子が適切な波長の光の光子を吸収すると、高エネルギーレベルに励起する(井戸型ポテンシャルを参照)。これらの電子遷移のほとんどは、偶対称性を持つ一つの共役π系分子軌道 (molecular orbital, MO) から奇対称性を持つもう一つの共役π系分子軌道への遷移(π → π*)である。しかし電荷移動錯体でしばしば起こるように、他の状態の電子もまたπ系分子軌道に働きかけることができる(n → π*)。電磁遷移の選択律で許容される場合は電子のHOMOからLUMOへの遷移がしばしば起こる。共役二重結合が8本よりも少ない共役系は紫外領域しか吸収せず、人間の眼には無色に見える。二重結合が増えるにつれ、共役系は長波長(低エネルギー)の光子を吸収し、化合物は黄色から赤色を呈する。青色や緑色の化合物は通常共役二重結合のみには頼っていない。
紫外から可視スペクトルの光の吸収は、紫外・可視分光法によって定量することができ、光化学の全領域の基礎を形成している。
合成顔料および染料に広く使われている共役系は、ジアゾおよびアゾ化合物、フタロシアニン化合物である。
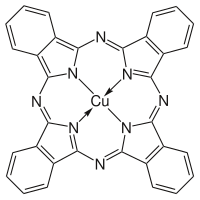
フタロシアニン化合物
[編集]共役系は可視領域の低エネルギー励起だけでなく、容易に電子を受容あるいは供与することができる。遷移金属イオンをしばしば含むフタロシアニンブルーやフタロシアニングリーンの様なフタロシアニン類は、酸化状態を容易に変化させる遷移金属イオンと電子を交換する。これらの様な顔料および染料は電荷移動錯体である。
ポルフィリンおよび類似化合物
[編集]ポルフィリンは、共役分子環系(大員環化合物)を持ち、生物系の多くの酵素で見られる。配位子として、ポルフィリンは濃い赤色を呈するヘモグロビンの鉄の様な金属イオンと数多くの錯体を形成する。ヘモグロビンは人体の細胞に酸素を輸送する。ポルフィリン-金属錯体は、しばしば強い色を呈する。クロリンと呼ばれる同様の分子構造環ユニットは、鉄の代わりにマグネシウムと同様の錯体を形成し、緑色を呈する最も一般的なクロロフィル分子の部分構造となる。もう一つの同様の大員環ユニットはコリンであり、コバラミン分子の部分構造としてコバルトと錯体を形成する。コバラミン類のビタミンB12は非常に強い赤色である。コリンユニットは6つの共役二重結合を持つが、大員環全てに渡っては共役していない。
 |
 |

|
| ヘモグロビン中のヘム基 | クロロフィルa分子のクロリン部位。緑色の四角はクロロフィルの種類によって異なる官能基を示している。 | コリン環を含むコバラミンの構造。 |
発色団
[編集]共役系は、化合物が呈色する分子中の光吸収部位である発色団の基礎を形作る。色を示すあるいは暗闇で光を放つ発色団は様々な有機化合物中にしばしば存在し、高分子でも時々存在する。発色団は、しばしば一連の共役した結合と環の両方あるいはどちらか一方の系から構成されており、一般的に芳香族で、C-C、C=C、C=O、N=N結合を含んでいる。

共役発色団はアゾ色素(人工食品添加物)、果物および野菜中の化合物(リコペンおよびアントシアニジン類)、眼の光受容体、以下のいくつかの医薬化合物含む多くの有機化合物でしばしば見られる。

共役系を含む化合物
[編集]脚注
[編集]- ^ conjugated system (conjugation) IUPAC. Compendium of Chemical Terminology, 2nd ed. (the "Gold Book"). Compiled by A. D. McNaught and A. Wilkinson. Blackwell Scientific Publications, Oxford (1997). XML on-line corrected version: http://goldbook.iupac.org (2006-) created by M. Nic, J. Jirat, B. Kosata; updates compiled by A. Jenkins. ISBN 0-9678550-9-8. doi:10.1351/goldbook.C01267.
- ^ March Jerry; (1985). Advanced Organic Chemistry reactions, mechanisms and structure (3rd ed.). New York: John Wiley & Sons, inc. ISBN 0-471-85472-7
