利用者:Wingless reindeer/物理有機化学
Physical organic chemistry, a term coined by Louis Hammett in 1940, refers to a discipline of organic chemistry that focuses on the relationship between chemical structures and reactivity, in particular, applying experimental tools of physical chemistry to the study of organic molecules. Specific focal points of study include the rates of organic reactions, the relative chemical stabilities of the starting materials, reactive intermediates, transition states, and products of chemical reactions, and non-covalent aspects of solvation and molecular interactions that influence chemical reactivity. Such studies provide theoretical and practical frameworks to understand how changes in structure in solution or solid-state contexts impact reaction mechanism and rate for each organic reaction of interest.
同位体の速度論的な影響
[編集]速度定数式からは遷移状態構造である分子の化学量の情報は得られるが、結合の切断や形成に関する情報はない。.[1][要ページ番号] 反応性の高い位置の近くである原子をその同位体に置換すると、反応速度が変化することが多い。同位体の置換は反応中間体や遷移状態のポテンシャルエネルギーを変化させるが、これは同位体が重いほど他の原子とより強い結合を形成するためである。原子の質量は関連する分子のゼロポイント振動準位に影響を与え、より重い同位体を含む分子では短く強い結合が形成され、より軽い同位体を含む分子では長く弱い結合が形成される。[2][要ページ番号] 反応過程では、結合が形成されたり切断されたりすることにより、振動の動きが変化することがあるため、振動数にも影響が及ぶ。これを観測することで、同位体置換により反応機構と速度定数に関する見識が得られる。
置換基の影響
[編集]置換基が分子の反応性や反応速度に与える影響は、化学界の大きな研究対象である。置換基は立体障害および電子的相互作用を介して影響を及ぼすことがあり、後者には共鳴や誘起効果などがある。分子の分極率も影響を受ける可能性がある。多くの置換基の影響は線形自由エネルギー関係(LFER)により分析される。その中で最も一般的なものはハメット則プロット分析である。[1][要ページ番号] この分析では、さまざまな置換基が安息香酸のイオン化に及ぼす影響を、さまざまな化学系において比較するものである。ハメット則プロットのパラメータにはシグマ(σ)とロー(ρ)がある。σの値は、無置換の安息香酸に対する置換安息香酸の酸性度を示す。正のσ値は置換安息香酸の酸性度がより強いことを示し、負の値は置換安息香酸の酸性度がより弱いことを示す。ρ値は置換基の変化に対する反応性の高さを示す尺度であるが、誘起効果のみの尺度である。したがって、共鳴による局所的な電荷の安定化を評価するためにσ+とσ−という2つの新しい尺度が生まれた。σ+は共鳴を介して正の電荷を安定化させる置換基に関連し、σ−は共鳴を介して負の電荷を安定化させる置換基に関連する。ハメット則分析は、起きうる反応機構の解明に役立つことがある。たとえば、遷移状態の分子構造が基底状態の構造に比べて負の電荷が蓄積すると予測される場合、電子供与基が反応速度を増加させていると推測される。 [1][要ページ番号]
他のLFER尺度も研究が進んでいる。立体障害や極性の効果はタフトパラメータにより分析される。反応物ではなく溶媒を変更することで、反応中の電荷の変化に対する見識が得られる。グルンワルド-ウィンシュタインプロットを行うと、これらの効果に対する量的な見解が得られる。[1][要ページ番号] [3]
溶媒の影響
[編集]溶媒は溶解度、安定性、反応速度に大きく影響することがある。溶媒を変更することで、化学反応の熱力学的制御と速度論的制御に影響を与えられる可能性がある。化学物質の転換中に電荷分布が変化するため、異なる溶媒中では反応が異なる速度で進行する可能性がある。溶媒効果は基底状態・遷移状態の分子構造に作用することがある。[1][要ページ番号]
有機反応における溶媒効果の一例は、 SN1 反応と SN2 反応の比較で見られる。[4][further explanation needed][要実例]
溶媒は系の熱力学的平衡にも大きく影響する可能性がある。たとえば、ケト-エノール平衡状態などである。非プロトン性の非極性溶媒では、分子内水素結合の形成によりエノールの割合が大きく増加する。一方、ジクロロメタンなどの極性非プロトン性溶媒では、極性溶媒と極性ジケトンとの相互作用のためエノールの形態が減少する。[example needed] プロトン性溶媒では、分子内水素結合が溶媒由来の水素結合と競合するため、平衡はケトの形態に傾く。[5][要非一次資料] [6][要非一次資料][7][要非一次資料]
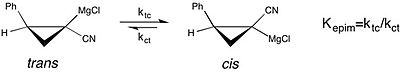
化学平衡の溶媒効果研究における現代の例として、キラルのシクロプロピルニトリルグリニャール試薬のエピメリ化研究が挙げられる。[8][要非一次資料] この研究によればグリニャール試薬のシス–トランス異性化の平衡定数は、THFが反応溶媒であるとき非常に大きく(cis型に平衡が傾き)、ジエチルエーテルが溶媒のときよりも優位である。しかし、THF中でのシス–トランス異性化の速度が速いため、立体化学的な純度を保つことはできない。このケースでは、不斉合成で観測される選択性に関し、反応溶媒が試薬の立体配置の安定性に与える影響を理解することが重要である。
Vibrational spectroscopy
[編集]振動分光法、または赤外線(IR)分光法は、官能基の同定を可能にする他、低コストで堅牢な分析法であるため教育機関の実験室や高圧、高温、気相、相境界などの厳しい環境での反応進行のリアルタイムモニタリングに使用されることが多い。分子の振動準位は電子波動関数と同様に量子化されており、振動数の整数値が増加するほど高いエネルギー準位となる。振動状態間のエネルギー差はほぼ一定であり、通常の温度では分子の振動は調和振動子と非常によく似ているため、これらのエネルギー差は赤外線の光子が持つ範囲のエネルギーに相当する。このIR分光法による有機化合物の官能基の同定は大まかには可能であるが、複合分子の場合、分子内で近傍の官能基間の振動が合わさるためスペクトルが複雑になる。したがって通常、単純な分子のみがIR分光法で分子構造を決定できる。また、スペクトルが複雑になる別の理由として、振動によっては分子の双極子モーメントを変化させないため、標準のIR吸収分光法では観測できないものがあることが挙げられる。これらは代わりにラマン分光法を通じて観測できるが、ラマン分光法はより細密な装置が必要であるためIR分光法ほど実施が容易ではない。ただし、ラマン分光法は光散乱に依存するため、異相触媒の表面、相境界、大きな液体容積内の1マイクロリットル(µL)の副試料など、微小な資料で実施できる。[9][要ページ番号] 振動分光法は、天文分野では分子ガス雲、太陽系外惑星の大気、および惑星の表面の組成を研究するためによく応用される。
Electronic excitation spectroscopy
[編集]電子励起(紫外可視近赤外)分光法、または紫外可視(UV-vis)分光法は、電磁スペクトルの可視光および紫外線領域で実行され、最高エネルギー被占軌道(HOMO)と最低エネルギー空軌道(LUMO)の分子軌道間のエネルギー差測定に利用される。このスペクトル情報は有機化合物がさまざまな可視光波長を吸収することによるものであり、有機光化学や染料の設計を行う物理有機化学者が利用する。電子構造を詳細に把握すれば電子の励起を説明できる。分子構造を綿密に制御することでHOMO-LUMOのエネルギー差を調整できれば、そのエネルギーに相当する望ましい色の波長と励起状態の特性を得ることができる。 [10]
Mass spectrometry
[編集]質量分析法は分子量を測定する手法であり、他の手法である分光法と併用してデータを補完することで分子構造が特定される。質量分析の典型的な実験を示す。有機材料の気相サンプルをイオン化すると、生成した各種のイオンが電場によって加速され、さらに磁場で向きを変える。磁場がかかるとイオンによって向きの変わる程度が異なることを利用し、分子が検出器に到達するまでの時間も併せて分子量を算出する。大きな分子はサンプルイオン化の過程で分裂しやすく、得られるデータには親イオンの質量といくつかの小さなフラグメント(分子の断片)の質量が含まれる。このようにフラグメント化することでタンパク質や核酸ポリマーの配列に対する豊富な情報が得られる。分子やそのフラグメントの質量だけでなく、同位体の分布も測定でき、ある元素の定性的な存在をその元素に固有な天然同位体分布によって識別することができる。フラグメント質量の分布と親イオンの分布の比率はこれまでの実験例を集めたライブラリ中のフラグメントデータと比較することで、既知の分子構造と一致するかどうかを調べることができる。[11] ガスクロマトグラフィーと–質量分析法の組み合わせにより、分子の定性と濃度の定量測定が高い精度で行われ、血液中の微量の生体分子や違法薬物を検出するために広く使用されている。合成有機化学の分野では、新しい化合物や反応生成物の特性評価に有用なツールである。
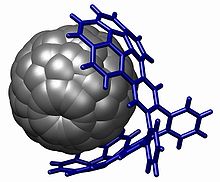
X線結晶構造解析は分光法と違って常に明確な構造決定が可能であり、また分光法では得られない結合角と結合長が精度よく得られる。物理有機化学では絶対的な分子構造を得るため使用されることが多く、純度の高い光学異性体物質の合成を改善するためにも重要なツールである。また、NMR活性な核を持たない酸素などの元素に対し、位置と結合を特定する唯一の方法でもある。実際、20世紀初頭にX線結晶構造決定法が利用可能になるまで、有機分子の構造は推測することしかできなかった。例えば四面体形分子構造の炭素は、ダイヤモンドの結晶構造でしか確証できず[12]、ベンゼンの非局在構造は、ヘキサメチルベンゼンの結晶構造でしか確証できなかった。[13] 結晶学は有機化学の分野で非常に満足のいくデータを提供するが、対象化合物の完全な単結晶を育てる必要があるため、有機化学で日常的に使われる手法ではない。NMRデータで一義的に解釈できない複雑な分子のみにこの技術が適応される。例として、図のホスト-ゲスト複合体は、単結晶構造解析を使用しなければ構造の解明は困難であった(フラーレンにはプロトンがなく、有機複合体の二つの半分に共有結合がないため、分光法だけでは仮説された構造を証明することができなかった)。[要出典] [[Category:有機化学]]
- ^ a b c d e Dougherty, Dennis A.; Anslyn, Eric V. (2006). Modern Physical Organic Chemistry. Sausalito, CA, USA: University Science Books. ISBN 9781891389313[要ページ番号] 引用エラー: 無効な
<ref>タグ; name "Anslyn"が異なる内容で複数回定義されています - ^ Isaacs, Neil S. (1995). Physical Organic Chemistry (2nd ed.). Harlow, ESS, ENG: Longman Scientific & Technical. ISBN 978-0582218635[要ページ番号]
- ^ Kevill, Dennis N.; D'Souza, Malcolm J. (1 June 1992). “Concerning the development of scales of solvent ionizing power based on solvolyses of benzylic substrates”. Journal of Physical Organic Chemistry 5 (6): 287–294. doi:10.1002/poc.610050602.
- ^ Reichardt, Christian; Welton, Thomas (2011). Solvents and solvent effects in organic chemistry. (4th, updated and enl. ed.). Weinheim, Germany: Wiley-VCH. ISBN 978-3-527-32473-6
- ^ Mills, Sander G.; Beak, Peter (1 April 1985). “Solvent effects on keto-enol equilibria: tests of quantitative models”. The Journal of Organic Chemistry 50 (8): 1216–1224. doi:10.1021/jo00208a014.
- ^ Emsley, John; Freeman, Neville J. (1 October 1987). “β-diketone interactions”. Journal of Molecular Structure 161 (1–2): 193–204. Bibcode: 1987JMoSt.161..193E. doi:10.1016/0022-2860(87)85074-3.
- ^ Schlund, Sebastian; Basílio Janke, Eline M.; Weisz, Klaus; Engels, Bernd (1 January 2009). “Predicting the tautomeric equilibrium of acetylacetone in solution. I. The right answer for the wrong reason?”. Journal of Computational Chemistry 31 (4): 665–70. doi:10.1002/jcc.21354. PMID 19557765.
- ^ a b Gao, Ming; Patwardhan, Neeraj N.; Carlier, Paul R. (2013). “Stereochemical Inversion of a Cyano-Stabilized Grignard Reagent: Remarkable Effects of the Ethereal Solvent Structure and Concentration”. J. Am. Chem. Soc. 135 (38): 14390–14400. doi:10.1021/ja407348s. PMID 23978216.
- ^ Drago, Russell S. (1992). Physical Methods for Chemists (2nd ed.). Ft. Worth, TX, USA: Saunders. ISBN 9780030970375 22 June 2014閲覧。[要ページ番号]
- ^ Reusch. “Visible and Ultraviolet Spectroscopy”. Michigan State University Website. Michigan State University. 26 October 2013閲覧。
- ^ Adlard, edited by Alan J. Handley, Edward R. (2000). Gas chromatographic techniques and applications. Boca Raton, FL: CRC Press. p. 168. ISBN 978-0-8493-0514-6
- ^ Bragg, W. H.; Bragg, W. L. (July 1913). “The Structure of the Diamond”. Nature 91 (2283): 557. Bibcode: 1913Natur..91..557B. doi:10.1038/091557a0.
- ^ Lonsdale, K. (November 1928). “The Structure of the Benzene Ring”. Nature 122 (3082): 810. Bibcode: 1928Natur.122..810L. doi:10.1038/122810c0.
