白血球

白血球(はっけっきゅう、英: white blood cellあるいは英: leukocyte)とは、生体防御に際した免疫を担当する細胞である単球(マクロファージ)、リンパ球、好中球、好塩基球、好酸球の5種類を含んだ総称的物質を指す。
この細胞成分は、外部から体内に侵入した細菌・ウイルスなどの異物の排除や、腫瘍細胞・役目を終えた細胞の排除及び分解殺失などを役割とする造血幹細胞由来の細胞である。
血液検査などではWBCと表されることが多い。
大きさは6から30µm(マクロファージはそれ以上)。数は、男女差はなく、正常血液3,500~9,500/μL(1 µLあたり、3,500から9,500個)程度である。
白血球の種類
[編集]末梢血内には顆粒球・リンパ球・単球があり、顆粒球はギムザ染色による染色のされ方の違いによって好中球、好酸球、好塩基球の3つに分類される[1]。
したがって末梢血内の白血球は通常、好中球・好酸球・好塩基球・リンパ球・単球の5種類とされる。
顆粒球は骨髄で産出され、末梢血内の白血球の半分から3/4程度を占める[2]。細胞質には殺菌作用を持つ顆粒が存在する。リンパ球は末梢血内の20から40%を占め、単球は3から6%ほどを占める[2]。
組織内には単球の分化が進み組織ごとに適応し、異物の呑食・不要になった体細胞の処理、体液性免疫細胞への抗原提示、サイトカインの放出などさまざまな役割を果たすマクロファージが存在する。
白血球数の基準値
[編集]内科学の代表的な教科書では白血球の基準値は3,500〜9,500/µLとされている[1]。しかし末梢血内の白血球数は個人差が大きく、また一個人内でも短時間で変動する。そのために検査機関ごとに、あるいは成書ごとに基準値の設定には差があり、成人では基準下限値は3,300〜4,000/µL、基準上限値は8,000〜11,000/µLと幅がある[2]。新生児および乳幼児は成人より数が多く、新生児では20,000/µLを超えることも珍しくない。また、新生児から乳児期にはリンパ球の割合が高く、70%程度になる[2]。
- 50,000/µL以上
- 白血病、骨髄増殖性疾患、栗粒結核、敗血症、悪性腫瘍
- 10,000〜50,000/µL
- 感染症、自己免疫疾患、代謝障害、薬物中毒、白血病、骨髄増殖性疾患、ステロイド剤の影響、ストレス、喫煙、妊娠
- 1,000〜3,000/µL
- 再生不良性貧血、抗ガン剤・放射線治療の副作用、薬剤アレルギー、ガンの骨髄転移、骨髄異形成症候群、悪性貧血、脾機能亢進、腸チフス、ウイルス感染症、骨髄線維症、粘液水腫、AIDS、無顆粒球症
- 1,000/µL以下
- 1,000〜3,000/µLと同じ
上記の疾患などは白血球数の増減があるが、白血球数だけでは確定診断できない[4]。
好中球
[編集]
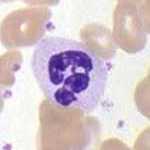
好中球(好中性白血球)(Neutrophil)は末梢血内では白血球全体の50から70%を占め[2]、顆粒球では約90から95%を占める。細菌や真菌などの感染には好中球が最初に集結し、かつ主に好中球が対処するが、好中球は体液性免疫細胞への抗原提示は行わない。好中球が処理し切れなかった細菌などの異物をマクロファージなどが貪食し、抗原提示を行い、体液性免疫を獲得する。怪我などをした後に傷口から発生する膿は、細菌との戦いで死んだ好中球の死体を主としている。
形状
[編集]無色半透明のおおむね球状であるが、偽足を出し、盛んにアメーバ様運動をするので、形は定まっていない。標準の血液細胞染色であるギムザ染色で中性色素に染まる殺菌性特殊顆粒を持ち、成熟すると核が分かれる(分葉)ので多核白血球といわれることもある。最終完成形の好中球は分葉核球と呼ばれ、核は分かれるが、核の間は核糸で繋がっている。分葉核球になる前には核が大きく曲がったジェリービーンズ様の桿状である段階がある(桿状核球)。殺菌性顆粒はリソソームの一種であり、ゴルジ体(内網装置)で作られる。直径は12〜15µmであり[5]、白血球の中ではリンパ球より大きく、単球・マクロファージより小さい。
数量・寿命
[編集]末梢血内には1マイクロリットル当たり2,000から7,500個程度の好中球が含まれ[2]、成人の末梢血内には概ね10の10乗個のオーダー(桁)の好中球が存在する。体重50kgの場合でおおよそ80億個から300億個程度の数量である。
しかしながら好中球は血管壁や組織、脾臓・肝臓などにも末梢血内に匹敵する量の好中球が辺縁プールとして存在する。さらに骨髄には末梢血内の10から30倍もの量の貯留プールが存在し、生体内すべてでは10の11乗のオーダー、数千億個の桁の好中球が存在する。
大きな貯留プールがあるため、細菌感染時などには貯留プール内の好中球が動員され、末梢血内の好中球数は速やかに増加する。また、食事や運動、ストレスなどのわずかな体の変化でも、その血流量の変化によって血管壁に滞留などで辺縁プールに存在していた好中球が末梢血内に移動するので、好中球数は変化しやすい。細菌感染時には、炎症性のサイトカインの働きで骨髄内での生産も亢進される。
感染がない時でも、一部の好中球は血管から組織内に移動し存在する。
血液内での好中球の寿命は1日以内、概ね10時間程とされる。組織内では数日である。
好中球は骨髄内で生産されるが、1日当たり10の11乗個(1000億個)程度作られる[2]。
好中球の生体防御のしくみ
[編集]生体に細菌などが感染すると、好中球は感染した炎症部位に遊走して集まり、細菌を貪食殺菌する。
遊走
[編集]
細菌や真菌類が侵入した組織では、組織内のマクロファージや肥満細胞がただちに反応し、インターロイキン-1(IL-1)などのサイトカインを放出し、それらのサイトカインにより、組織内の細胞は炎症性変化を起こす。また、それ以外の過程を含め、炎症性変化を起こした組織はインターロイキン-8(IL-8)を代表とする多種類のケモカイン(サイトカイン)や、その他の多種類の好中球遊走刺激因子を放出する。それらの刺激因子や細菌自身が産出する物質、活性化された補体を表面のレセプターで感じ取った好中球は遊走運動を活発化させる。速度は最大40µm/minになる。好中球は表面に多数あるレセプターで刺激因子の濃度の濃い薄いを感じ取り、因子の濃度の濃い方向に遊走し、感染巣に集結する。多くの場合、感染巣は血管外であり、好中球は血管壁を通過しなければならない。炎症箇所に近い毛細血管壁で好中球は血管上皮に粘着し、血管上皮細胞と好中球それぞれが各種因子によって変化を起こし、好中球は血管上皮細胞の間をすり抜ける。血管外に出た好中球は組織内を遊走し、感染巣に到達する。
炎症組織からの遊走刺激因子により、骨髄内の貯留プールなどに存在する好中球も刺激を受け、遊走運動を開始し、また骨髄では好中球の生産が亢進される。それらによって、細菌類の感染には大量の好中球が動員されることになる。
このように炎症によって生じる白血球遊走刺激因子(ロイコエグレシン、ロイコカイン、リンフォカイン、細菌毒素、補体の分解産物)によって移動する性質を化学走性(chemotaxis)という。
貪食・殺菌
[編集]感染巣に到達した好中球は、細菌類への接触から貪食を行い、飲み込んだ細菌類を殺菌する。
好中球は細菌類に接触すると表面のレセプターを介して異物と認識し、接着結合する。結合した異物を好中球形質膜がこれを包むようにして、好中球内に取り込む。
好中球内に取り込まれた細菌類は、3つの手段で殺菌される。一つは、酸素系の働きで活性酸素や過酸化水素、次亜塩素酸を発生させて殺菌する。もう一つは、顆粒から放出される加水分解酵素などで殺菌する。さらに近年NETs(neutrophil extracellular traps)と呼ばれるクロマチンの網を形成して微生物をとらえることが知られている[6][7]。
細菌を飲み込んだ好中球はやがて死亡し、死体は膿になって体外に放出されるか、組織内のマクロファージなどにより処理される。
生体防御の過程について、より詳しくは好中球項目を参照のこと。

分化過程
[編集]好中球を含め、全ての血球は骨髄の中に存在する造血幹細胞に由来する。骨髄中において造血幹細胞は赤血球・各種の白血球・血小板に分化するが、最終的に好中球に分化する場合は造血幹細胞、骨髄系幹細胞(骨髄系前駆細胞)、顆粒球・単球系前駆細胞、顆粒球前駆細胞、骨髄芽球、前骨髄球、骨髄球、後骨髄球の順に分化成熟する。さらに桿状核球を経て分葉核球へと分化するが、この最後の2つをもって好中球と呼ぶ。
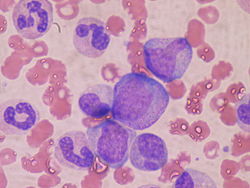
造血幹細胞から分裂し分化し始めた細胞は盛んに分裂し数を増やしながら少しずつ分化の方向を進めていく。幹細胞から前駆細胞、骨髄芽球の段階までは、顕微鏡による形態学的観察では最終的に好中球などの顆粒球系に分化する細胞であるか識別は困難であるが、骨髄芽球の段階からは顆粒が生じ始め、顆粒球系の細胞と形態学的にも判断できるようになる。前骨髄球の段階になると、好中球への分化傾向が明らかになる。
骨髄芽球の段階から一次顆粒(アズール顆粒)が生じ始め、前骨髄球では豊富な一次顆粒(アズール顆粒)を持つようになる。骨髄球の段階では一次顆粒は見えなくなり(見えないが存在はする)、代わりに二次顆粒(特殊顆粒)が発現する。さらに三次顆粒など、好中球には各種の殺菌性顆粒が存在するようになる。
顆粒球系と判断できるようになった段階以降も、骨髄芽球で1回、前骨髄球で2回、骨髄球で2回ほどの細胞分裂を起こし、数を増す。後骨髄球の段階になると、細胞分裂する能力は失われる。通常時には、骨髄芽球以降の段階でおよそ11日の時間をかけ、成熟する。
骨髄芽球や前骨髄球など幼若な段階では、細胞の核は大きく丸く、核内構造(クロマチン構造)は繊細であるが、分化・成熟が進むほど核は小さくいびつになり、構造は粗くなる。核が歪んだジェリービーンズ形である「桿状核球」と呼ばれる段階になると、完成した好中球と認識されるが、さらに成熟が進み、核の形が複数に分かれた分葉核球となる。分葉核球が好中球の分化の最終成熟段階となる。
末梢血に見られる好中球の大多数は分葉核球であるが、炎症時など好中球の大量の動員が必要な時などには桿状核球の割合が増える。
白血球の核形の左方推移
[編集]好中球は、正常な状態では末梢血中に分葉核球(2〜3葉が多い)が多く認められる。
感染症等の場合、免疫応答による好中球増加が見られるが、その初期の段階では桿状核球が増加し、さらに幼若な後骨髄球や骨髄球が末梢血に出現することがある。出血性貧血や、医療行為による骨髄抑制などによる汎血球減少からの回復期にも同様のことが起きる。このような一核細胞の増加を、核の左方推移と呼ぶ。好中球を急速に動員しなければならない事態のために、最終成熟形態でない好中球も動員されるためと思われる。
上記は炎症や「造血の立ち上がり」に見られる一過性の左方推移の例であるが、骨髄異形成症候群や慢性骨髄性白血病などの場合は骨髄球-顆粒球系細胞の分化成熟能力自体に異常を生じているため、左方推移状態が持続する。
なお、逆に分葉核球の比率が増えた状態=右方推移は、悪性貧血などのときに起こる。
好酸球
[編集]好酸球(好酸性白血球)(Eosinophil,Acidophil)は、末梢血内の白血球の2から5%を占める[2]。普通染色でエオジン親和性のピンクから橙黄色に染まる均質・粗大な顆粒(好酸性顆粒)が細胞質に充満し、核は多くは2分葉で細いクロマチン糸でつながれ、細胞周縁に偏在する[1]。
好酸球も弱い遊走・貪食能力を持つが、主な役割では寄生虫・寄生虫卵の傷害あるいはアレルギー反応の制御を行う。
I型アレルギー、寄生虫の感染などで増殖する。
また、ストレスや副腎皮質ホルモン分泌時に減少する。
好塩基球
[編集]好塩基球(好塩基性白血球)(Basophil)は、末梢血内の白血球の1%以下である[2]。
普通染色の塩基性色素により、暗紫色に染まる大型の顆粒(好塩基性顆粒)を持つ。
肝臓の肥満細胞と似ており、細胞表面にIgEに対するレセプターをもち、抗原刺激によって脱顆粒反応を起こし、血管作動性タンパク質であるヒスタミンを遊離し、凝固阻止因子であるヘパリンを分泌することにより血液の血管内凝固を防止している。
生体の免疫機能に関与していると考えられるが、はっきりとした存在意義は不明である[8]。
リンパ球
[編集]リンパ球(Lymphocyte)は、末梢血の白血球のうち20〜40%ほどを占める[2]、比較的小さく(6〜15µm)[9]、細胞質の少ない白血球。その大きさから小リンパ球(6〜9µm)と大リンパ球(9〜15µm)とに分類されることがあるが、この分類に絶対的な基準はない。抗体(免疫グロブリン)などを使ってあらゆる異物に対して攻撃するが、特にウイルスなどの小さな異物や腫瘍細胞に対しては、顆粒球ではなくリンパ球が中心となって対応する。NK細胞、B細胞(Bリンパ球)、T細胞(Tリンパ球)などの種類がある。体液性免疫、抗体産生に携わるのはB細胞とそれをサポートするヘルパーT細胞で、腫瘍細胞やウイルス感染細胞の破壊など細胞性免疫に携わるのはキラーT細胞やNK細胞である。寿命は数日から数箇月、時には年単位である。骨髄で未熟な状態で産出された後、胸腺(T細胞)や骨髄など(B細胞)で成熟し、さらにはリンパ節に移動し、そこでも増生・成熟が行われるなど、複雑な経過をたどる。
単球
[編集]単球(Monocyte)は骨髄で産出され、末梢血の白血球のうち3〜6%を占める[2]。白血球細胞の中で最も大きく(20〜30µm)[10]、切れ込みの入った核を持つことが多い。単核白血球ともいう。単球は、感染に対する免疫の開始に重要であり、アメーバ様運動を行って移動することができ、細菌などの異物を細胞内に取り込み、細胞内酵素を使って消化する。断片化した異物を、もともと細胞質内に持っていたクラスII MHC分子と結合させ、細胞表面に提示し、これをヘルパーT細胞が認識する。こうして免疫反応が開始される。また単球は血管外の組織や体腔に遊走し、そこで組織固有のマクロファージ(大食細胞)、樹状細胞、破骨細胞に分化する。あるいは、単球とは血管内に存在しているマクロファージ/樹状細胞と考えることもできる。マクロファージ/樹状細胞は存在する組織ごとに適応し、異物の呑食、体液性免疫細胞への抗原提示の他に、不要になった体細胞の処理、各種サイトカインの放出、骨髄において赤血球の育成などさまざまな役割を果たす。寿命は血液中では1日以下から数日、組織中では数日から数か月、時には数年である。
付録
[編集]別表
[編集]| 種類 | 顕微鏡像 | イメージ図 | 存在割合[2] | 直径 | 主な役割 | 核型 | 顆粒 | 寿命 |
|---|---|---|---|---|---|---|---|---|
| 好中球 |  |
50〜70% | 12〜15µm[5] |
|
桿状から分葉 | 中性色素でピンクに染まる殺菌性顆粒 | 血液中で1日以内、組織内で数日 | |
| 好酸球 | 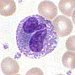 |
2〜5% | 13〜17µm[5] |
|
2分葉 | エオジン親和性の橙黄色に染まる均質・粗大な顆粒 | 好中球より少し長い | |
| 好塩基球 | 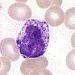 |
1%以下 | 10〜15µm[5] |
|
不定形 | 塩基性色素により暗紫色に染まる大型の顆粒 | ||
| リンパ球 |  |
 |
20〜40% | 6〜15µm[9] |
B細胞: 抗体(免疫グロブリン)産出
|
球型 | ないものが多い、大型の顆粒を持つ細胞はNK細胞に多い | 週〜年 |
| 単球 |  |
3–6% | 20〜30µm[10] | 単球は血液内に存在し、組織内に移動するとマクロファージか樹状細胞・破骨細胞に変化する | そら豆型 | なし | 数時間から数日 | |
| マクロファージ |  |
 |
20〜50µm[5] | 寿命を迎えた赤血球・白血球・血小板や裸核・各種細胞などの細胞残屑と病原体の食作用(抱き込みと消化)、およびリンパ球に対する抗原提示、リンパ球の刺激、骨髄において幼若な赤血球の育成など | 数日〜数箇月、ときには数年 | |||
| 樹状細胞 |  |
 |
Tリンパ球(T細胞)を動かす抗原提示 | マクロファージと同じ単球系細胞 |
注、画像の色および顆粒の色の説明はギムザ染色したものでの説明である、実際の血液中の白血球は無色半透明である。
好中球の異物貪食動画像
[編集][1] Neutrophils display highly directional amoeboid motility in infected footpad and phalanges. Intravital imaging was performed in the footpad path of LysM-eGFP mice 20 min after infection with LM.[11]
脚注
[編集]注釈
[編集]出典
[編集]- ^ a b c 小川『内科学書』p.15
- ^ a b c d e f g h i j k l 日本検査血液学会編、スタンダード検査血液学第2版、医歯薬出版、2008、p.50
- ^ 高久史麿監修『臨床検査データブック 2003-2004』(医学書院、2003)、 p.307
- ^ 『臨床検査データブック 2003-2004』p.307
- ^ a b c d e 小川 哲平、大島 年照、浅野 茂隆編著、血液学、内外医学社、1991
- ^ Brinkmann V, et al. Neutrophil extracellular traps kill bacteria. Science 2004: 303; 1532-1535.
- ^ Zawrotniak M, et al. Neutrophil extracellular traps (NETs)-frmation and implications. Acta Biochim Pol 2013: 60; 277-284.
- ^ 小川『内科学書』p.18
- ^ a b 日本検査血液学会編、スタンダード検査血液学第2版、医歯薬出版、2008、p.48
- ^ a b 日本検査血液学会編、スタンダード検査血液学第2版、医歯薬出版、2008、p.47
- ^ Public Library of Science
参考文献
[編集]- 笹月 健彦 監訳『免疫生物学 原書第5版』南江堂 2003年 ISBN 9784524235223
- 浅野茂隆、池田康夫、内山卓 監修 『三輪血液病学』文光堂、2006年、ISBN 4-8306-1419-6
- 小川聡 総編集 『内科学書』Vol.6 改訂第7版、中山書店、2009年、ISBN 978-4-521-73173-5
- 小川 哲平、大島 年照、浅野 茂隆編著、『血液学』、中外医学社、1991年
- 日本検査血液学会 編集『スタンダード検査血液学』初版、医歯薬出版、2003年、ISBN 4-263-22271-7
関連項目
[編集]外部リンク
[編集]- 『白血球』 - コトバンク
- 『炎症とライソゾーム』(1974年) - 鳥居薬品の企画の下でヨネ・プロダクションが制作。『科学映像館』より。白血球は生体に侵入した異物を食胞の中に捕らえると、これをライソゾームで消化。一方で、細胞外に放出されたライソゾームは生体の組織を破壊することもある。これらの観察で、ライソゾームと炎症の関係を明らかにするのが、この短編映画の趣旨。

