塩化スズ(II)
| 塩化スズ(II) | |
|---|---|

| |
塩化スズ(II) | |
別称 塩化スズ 塩化第一スズ | |
| 識別情報 | |
| CAS登録番号 | 7772-99-8 |
| PubChem | 24479 |
| ChemSpider | 22887 |
| E番号 | E512 (pH調整剤、固化防止剤) |
| 国連/北米番号 | 3260 |
| ChEBI | |
| RTECS番号 | XP8700000 (無水物) XP8850000 (二水和物) |
| |
| |
| 特性 | |
| 化学式 | SnCl2 |
| モル質量 | 189.60 g/mol (無水物) 225.63 g/mol (二水和物) |
| 外観 | 無色または白色の結晶性粉末(無水物) 白色結晶(二水和物) |
| 匂い | 無臭 |
| 密度 | 3.95 g/cm3 (無水物) 2.71 g/cm3 (二水和物) |
| 融点 |
247 °C, 520 K, 477 °F (無水物) |
| 沸点 |
623 °C, 896 K, 1153 °F (分解) |
| 水への溶解度 | 83.9 g/100 ml (0 ℃) 熱水中で加水分解 |
| 溶解度 | エタノール、アセトン、エーテル、テトラヒドロフランに可溶 キシレンに不溶。 |
| 構造 | |
| 結晶構造 | 層状 (SnCl3の集合体) |
| 配位構造 | 三角錐形 (無水物) 二水和物は配位数が3 |
| 分子の形 | 折れ線形(気体状態) |
| 危険性 | |
| 安全データシート(外部リンク) | ICSC 0955 (無水物) ICSC 0783 (二水和物) |
| 主な危険性 | 刺激性、水生生物には危険 |
| NFPA 704 | |
| 半数致死量 LD50 | 700 mg/kg (ラット、経口) 10,000 mg/kg (ウサギ、経口) 250 mg/kg (マウス、経口)[1] |
| 関連する物質 | |
| その他の陰イオン | フッ化スズ(II) 臭化スズ(II) ヨウ化スズ(II) |
| その他の陽イオン | 二塩化ゲルマニウム 塩化スズ(IV) 塩化鉛(II) |
| 特記なき場合、データは常温 (25 °C)・常圧 (100 kPa) におけるものである。 | |
塩化スズ(II)(えんかスズ、tin(II) chloride または stannous chloride)は、化学式 SnCl2 で表される+2価のスズの塩化物で、無水物、2水和物がある。無水物は常温常圧において無色〜白色の結晶性粉末で、潮解性がある。2水和物は常圧において融点 37.7 ℃ の白色結晶で強力な還元剤であり、酸化剤や強塩基と激しく反応する。硝酸塩とは非常に激しく反応し、爆発の危険がある。空気中の酸素と反応して不溶性のオキシ塩化物を生じる。水、メタノール、エタノール、酢酸、酒石酸などに可溶。
構造
[編集]塩化スズ(II)は非共有電子対を持つため、気体状態では折れ線形分子として存在する。固体状態では、1つの塩化物イオンが2つのスズイオンによって共有され、鎖型の結晶構造となっている。2水和物は1つの水分子がスズイオンに配位結合し、その水分子にもう1つの水分子が配位結合して構成されている。2水和物の結晶格子は、層をなした塩化スズ(II)の間に水分子を挟み込む形になっている。

性質
[編集]物理的性質
[編集]生成熱は-325kJ/mol、結合の長さは気体状態で242pm、結合がなす角度は気体状態で95°、固体状態で80°である。磁化率はCGS単位系で−69.0である。
化学的性質
[編集]塩化スズ(II)は見た目上水に分解することなく溶解するが、溶液を希釈すると加水分解がおこり、白色沈殿の塩基性塩が生成する。この時、次の式の平衡が成立している。

ゆえに、透明な塩化スズ(II)の溶液を長時間保持する場合、ルシャトリエの原理より溶媒は塩酸とする必要がある。また、塩化スズ(II)は空気に触れることで空気中の酸素と反応して酸化され、次の反応を起こす。
スズでできた缶に保存すれば、この反応の進行を抑えることができる[3]。
スズは様々な状況で還元剤として用いられる。銀や金のイオンと反応して銀や金の単体を析出させるほか、鉄(III)イオンを還元して鉄(II)イオンを生じさせる。
また、塩化スズ(II)の溶液はスズ(II)イオンの沈殿反応にも利用することができる。例えば、硫化ナトリウムとの反応では、黒色沈殿の硫化スズ(II)が生成する。
強塩基を塩化スズ(II)の溶液に少量加えた場合、酸化スズ(II)1水和物の白色沈殿が生成する。しかし過剰に加えると、スズは両性元素であるため、トリスヒドロキソスズ(II)酸イオンなどの錯体を作って溶ける。
無水塩化スズ(II)は水以外の溶媒中において、様々な化合物に変化する。例えば、ジブチルヒドロキシトルエンと塩化スズ(II)をテトラヒドロフラン(THF)中で反応させると、2分子が配位結合した黄色い直線状の分子Sn(OAr)2ができる[4]。
塩化スズ(II)はルイス酸としても働き、塩化物イオンなどを配位子として錯体を形成する。
これらの錯体のうち多くは三角錐形である。またトリクロロスズ(II)酸イオン([SnCl3]-)などの錯体はオクテット則を満たすため安定であり、これらの錯体に配位子が増えることは少ない。よって、これらの錯体の孤立電子対は結合に使われる。ゆえに、これらの錯体はルイス塩基や配位子として働く。これはフェロセンの関連物質との反応において見られる現象である。
また、塩化スズ(II)は金属同士の間に結合を作る反応にも用いられる。例えば、オクタカルボニル二コバルトとは以下のように反応する。
調製
[編集]無水塩化スズ(II)は金属スズに乾燥した塩化水素を吹き付けて得られる。同様に塩化スズ(II)2水和物は、スズを塩酸に溶かし、できた溶液の水を蒸発させれば得られる。
用途
[編集]塩酸を少量含む塩化スズ(II)の水溶液は、鉄のスズめっき(ブリキの缶)の製造に用いられる。陽極に鉄を用い、溶液に電圧をかけて、電気分解すると、鉄の極板上にスズが析出する。
染色において塩化スズ(II)はコチニール色素などで染めた布の色を明るくするので、媒染剤として用いられる。また、絹の重量を増すために単独で使われることもある。また、生分解性プラスチックであるポリ乳酸(PLA)の製造時に触媒として用いられる。さらに、アセトンと過酸化水素を反応させて過酸化アセトンの四量体を作る際の触媒にも用いられることがある。
塩化スズ(II)には還元剤として多くの用途がある。銀鏡反応にも用いられる。
同様の還元反応がHg2+の検出にも用いられる。塩化スズ(II)の溶液を塩化水銀(II)の溶液に少量たらすと、塩化水銀(I)の白色沈殿が生成する。さらに塩化スズ(II)を加えていくと、金属の水銀が生成し、溶液が黒くなる。また、塩化スズ(II)は金の存在下でカシウス紫を生成し、紫色となるため、金の検出にも使われる。また、同様に水溶液中の白金族元素の検出にも用いられる[6]。
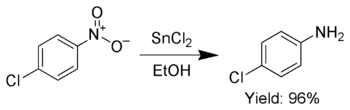
原子吸光を用いて水銀を分析する場合、必ず冷蒸気原子吸光分析法が用いられるが、この時塩化スズ(II)が還元剤としてよく用いられる。また、有機合成化学では還元剤として用いられる。例えばニトロ基をアミノ基に還元して芳香族アミンを合成する際に用いられる[7]。
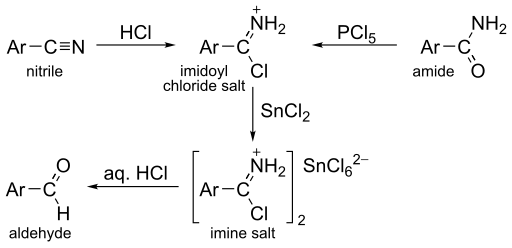
この他に、ニトリルから塩化イミドイル(英語版)を経由してイミンを合成し、それを加水分解させて芳香族アルデヒドに変換するスチーブン合成などに用いられる[8]。
この反応は芳香族ニトリル(Aryl-CN)においてよく進行する。関連する反応として、アミドを五塩化リンで処理して塩化イミドイルに変換するソン・ミューラー(Sonn-Müller)法がある。
スチーブン合成は、現在は水素化ジイソブチルアルミニウムの還元に取って代わられたため、あまり行われていない。
また、塩化スズ(II)にはキノンをヒドロキノンに還元するはたらきもある。
EUでは、塩化スズ(II)はE番号E512として食品添加物に認定されている。缶詰や瓶詰の食品用に、保色剤や酸化防止剤として使われている。
塩化スズ(II)は放射性核種血管造影法において、テクネチウム99m(英語版)の過テクネチウム酸塩が血球に結合しやすくなるように放射性物質を減らすために使われている。
溶融した塩化スズ(II)は酸化して、緻密な結晶構造を持つ酸化スズ(IV)に変化することがある[9] [10]。
脚注
[編集]- ^ “Tin (無機化合物、スズとして)”. 生活や健康に直接的な危険性がある. アメリカ国立労働安全衛生研究所(NIOSH). 2024年11月21日閲覧。
- ^ J. M. Leger, J. Haines, A. Atouf (1996). “The high pressure behaviour of the cotunnite and post-cotunnite phases of PbCl2 and SnCl2”. J. Phys. Chem. Solids 57 (1): 7–16. Bibcode: 1996JPCS...57....7L. doi:10.1016/0022-3697(95)00060-7.
- ^ H. Nechamkin (1968). The Chemistry of the Elements. New York: McGraw-Hill
- ^ B. Cetinkaya, I. Gumrukcu, M. F. Lappert, J. L. Atwood, R. D. Rogers and M. J. Zaworotko (1980). “Bivalent germanium, tin, and lead 2,6-di-tert-butylphenoxides and the crystal and molecular structures of M(OC6H2Me-4-But2-2,6)2 (M = Ge or Sn)”. 米国化学会誌 102 (6): 2088–2089. doi:10.1021/ja00526a054.
- ^ W. L. F. Armarego, C. L. L. Chai (2009). Purification of laboratory chemicals (6 ed.). The United States of America: Butterworth-Heinemann
- ^ 金精錬フォーラム
- ^ F. D. Bellamy and K. Ou (1984). “Selective reduction of aromatic nitro compounds with stannous chloride in non acidic and non aqueous medium”. テトラヘドロン・レターズ 25 (8): 839–842. doi:10.1016/S0040-4039(01)80041-1.
- ^ Williams, J. W. (1955). "β-Naphthaldehyde". Organic Syntheses (英語).; Collective Volume, vol. 3, p. 626
- ^ A.R.Kamali, Thermokinetic characterisation of tin(11) chloride, J Therm Anal Calorim 118(2014) 99-104.
- ^ A.R.Kamali et al.Transformation of molten SnCl2 to SnO2 nano-single crystals, Ceram Intern 40 (2014)8533-8538.
参考文献
[編集]- N. N. Greenwood, A. Earnshaw, Chemistry of the Elements, 2nd ed., Butterworth-Heinemann, Oxford, UK, 1997.
- "Handbook of Chemistry and Physics", 71st edition, CRC Press, Ann Arbor, Michigan, 1990.
- The Merck Index, 7th edition, Merck & Co, Rahway, New Jersey, USA, 1960.
- A. F. Wells, 'Structural Inorganic Chemistry, 5th ed., Oxford University Press, Oxford, UK, 1984.
- J. March, Advanced Organic Chemistry, 4th ed., p. 723, Wiley, New York, 1992.












