利用者:YasuakiH/note
英語版 Molecule の2021-03-01T10:21:34(UTC)版を翻訳


分子(英: molecule)は、2つ以上の原子が化学結合によって結合した、電気的に中性のグループである[4][5][6][7][8]。分子は、電荷を持たないという点でイオンとは区別される。
量子物理学、有機化学、生化学の分野では、イオンとの区別がなくなり、多原子イオンを指す場合には「分子」(molecule)がよく使われる。
気体分子運動論では、分子という用語は、その組成にかかわらず、あらゆる気体粒子に使われることが多い。希ガスが個々の原子であることから、分子が2つ以上の原子を含むという定義に反する[9]。
分子には、酸素分子(O2)の2つの原子のように、1つの化学元素の原子で構成される等核分子と、水(水素原子2個、酸素原子1個、H2O)のように、2つ以上の元素からなる化学物質である異核分子の場合もある。
水素結合やイオン結合などの非共有結合で結合された原子や錯体は、通常、単一分子とはみなされない[10]。
物質の構成要素としての分子は一般的なものである。それらはまた、海や大気の大部分を構成している。ほとんどの有機物質は分子である。タンパク質、その材料となるアミノ酸、核酸(DNA、RNA)、糖質、炭水化物、脂質、ビタミンなど、生命を構成する物質は分子である。栄養素であるミネラルは、通常、分子ではない。(例:硫酸鉄)
しかし、地球上の身近な固体物質の大半は、分子でできているわけではない。これらは、地球の物質を構成するすべての鉱物、土壌、土砂、粘土、小石、岩、地殻、マントル、地球のコアなどである。これらはすべて、多くの化学結合を含んでいるが、特定の分子でできているわけではない。
塩類や共有結合結晶については、典型的な分子を定義することはできない。グラフェンのように平面的に、あるいはダイヤモンド、石英、塩化ナトリウムのように3次元的に伸びる単位格子の繰り返しで構成されていることが多い。単位セルの繰り返し構造というそのテーマは、金属結合を持つ縮合相であるほとんどの金属にも当てはまる。したがって、固体金属は分子でできているわけではない。
ガラスは、ガラス質の無秩序な状態で存在する固体であり、原子は化学結合によって結合しているが、明確な分子は存在せず、塩や共有結合の結晶、金属のような規則的な単位セル構造の繰り返しもない。
分子科学
分子科学は、化学と物理のどちらに重点を置くかによって、「分子化学」または「分子物理学」と呼ばれる。分子化学では、化学結合の形成や切断といった分子間の相互作用を支配する法則を扱い、分子物理学では、分子の構造や性質を支配する法則を扱う。しかし、実際にはこの区別は曖昧である。分子科学では、分子は2つ以上の原子から構成される安定した系(束縛状態)で構成される。多原子イオンは、電気を帯びた分子と考えることもできる。「不安定分子」という用語は、非常に反応性の高い種、すなわちラジカル、分子イオン、リュードベリ分子、遷移状態、ファンデルワールス錯体、ボーズ=アインシュタイン凝縮のように原子が衝突した系など、電子と原子核の短命な集合体(共鳴)に対して使われる。
歴史と語源
メリアム=ウェブスターやオンライン・エティモロジー・ディクショナリーによると、「molecule」はラテン語の「moles」または「小さな質量単位」に由来するとされている。
- Molecule (1794) - 「極めて微細な粒子」、フランス語のmolécule(1678)から、新ラテン語のmoleculaから、ラテン語のmoles「mass, barrier」の縮約形。当初は漠然とした意味だったが、この言葉(18世紀後半まではラテン語の形でのみ使われていた)の流行は、デカルトの哲学にまでさかのぼることができる[11][12]。
分子の定義は、分子の構造に関する知識が増えるにつれて進化してきた。初期の定義はあまり正確ではなく、分子の定義を、その組成と化学的性質を維持している純粋な化学物質の最小の粒子としていた[13]。しかし、岩石、塩、金属など身近な物質の多くは、化学結合した原子やイオンの大きな結晶ネットワークで構成されており、個別の分子で構成されているわけではないため、この定義はしばしば破綻する。
結合
分子は、共有結合とイオン結合のいずれかによって結合される。非金属元素の中には、環境中では分子としてしか存在しないものがいくつかある。たとえば、水素は水素分子としてのみ存在する。化合物の分子は、2つ以上の元素で構成されている[14]。等核分子は、単一の元素の2つ以上の原子からできている。
金属の結晶は、金属結合によって結合された単一の巨大な分子とみなすことができるという人もいれば[15]、金属は分子とは全く異なる働きをすると指摘する人もいる[16]。
共有結合

共有結合とは、原子間で電子対(電子のペア)を共有する化学結合のことである。これらの電子対は「共有対」または「結合対」と呼び、原子間で電子を共有するときの引力と反発力の安定したバランスを「共有結合」と呼ぶ[17]。
イオン結合

イオン結合は、反対の電荷を持つイオン間の静電引力を伴う化学結合の一種であり、イオン化合物で発生する主な相互作用である。イオンとは、1つまたは複数の電子を失った原子(カチオン)と、1つまたは複数の電子を獲得した原子(アニオン)のことである[18]。このような電子の移動は、共有結合とは対照的に、「共有原子価」と呼ばれている。最も単純なケースでは、カチオンは金属原子であり、アニオンは非金属原子であるが、これらのイオンは、NH4+やSO42−のような分子イオンなど、より複雑な性質を持つこともある。
常温常圧では、イオン結合はほとんどの場合、個別の識別可能な分子を持たない固体(場合によっては液体)を形成するが、このような物質が気化/昇華すると、小さな個別の分子が生成され、電子が十分に移動するため、結合は共有結合ではなくイオン結合とみなされる。
分子の大きさ
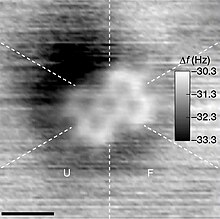
ほとんどの分子は肉眼で見ることができないほど小さいが、多くのポリマーの分子は、DNAのような生体高分子を含めて、巨視的なサイズに達する。有機合成の構成要素として一般的に用いられる分子の大きさは、数オングストローム(Å)から数十Å、つまり10億分の1メートル程度である。単一の分子は通常、光で観察することはできないが(前述のように)、原子間力顕微鏡を使用して、低分子(小分子)や個々の原子の輪郭を追跡できる場合もある。最大の分子には高分子や超分子もある。
最小の分子は二原子水素(H2)で、結合長は0.74 Åである[19]。
有効分子半径とは、分子が溶液中で示す大きさである[20][21]。各物質の透過選択性の表に例が記載されている。
分子式
化学式の種類
分子の化学式には、1行の化学元素記号、数字のほか、括弧、ダッシュ、角括弧、プラス(+)とマイナス(-)記号など他の記号も使用する。これらの記号は、活版印刷(タイポグラフィ)では1行に限られており、下付き、上付きを含む場合もある。
化合物の実験式は、非常にシンプルなタイプの化学式である[22]。これは、化合物を構成する化学元素の最も単純な整数比である[23]。たとえば、水は常に水素原子と酸素原子が2:1の割合で構成され、エタノール(エチルアルコール)は常に炭素、水素、酸素が2:6:1の割合で構成されている。ただし、これによって分子の種類が一意に決定されるわけではなく、たとえばジメチルエーテルはエタノールと同じ比率である。同じ原子が異なる配置になっている分子を異性体と呼ぶ。また、たとえば炭水化物は、炭素:水素:酸素=1:2:1という比率が同じ(したがって同じ実験式)であるが、分子内の原子の総数は異なる。
分子式は、分子を構成する原子の正確な数を反映しているため、異なる分子を特徴づける。ただし、異なる異性体は、異なる分子でありながら同じ原子組成を持つことがある。
実験式は、分子式と同じということがよくあるが、必ずしもそうとは限らない。たとえば、アセチレンの分子式はC2H2であるが、元素の最も単純な整数比はCHである。
分子量は、化学式から計算することができ、中性炭素12(12C同位体)原子の質量の1/12に相当する通常の原子質量単位で表される。ネットワーク固体の場合、化学量論的計算では式単位という用語が使われる。
構造式
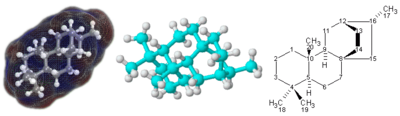
複雑な3次元構造を持つ分子、特に4つの異なる置換基に結合した原子を持つ分子の場合、単純な分子式や半構造化学式では、分子を完全に特定するのには不十分な場合がある。このような場合には、構造式と呼ばれるグラフィカルな式が必要になることがある。構造式は一次元の化学名で表すこともできるが、そうした化学命名法には化学式には含まれない多くの単語や用語が必要である。
分子構造
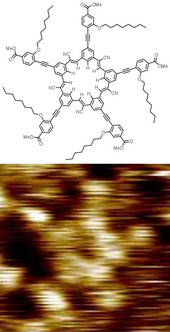
分子は、固定された平衡形状(結合長と結合角)を持ち、その周りで振動や回転運動が連続的に繰り返している。純粋な物質は、同じ平均的な幾何学的構造を持つ分子で構成されている。分学式と構造は、その性質、特に反応性を決定する2つの重要な要素である。異性体は、化学式は同じだが、構造が異なるため、通常は大きく異なる性質を持っている。異性体の一種である立体異性体は、物理化学的性質が非常によく似ているが、同時に生化学的活性が異なる場合がある。
分子分光法
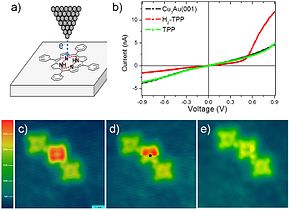
分子分光学は、既知のエネルギー(プランクの公式では周波数)を持つプローブ信号と相互作用する分子の応答(スペクトル)を扱う。分子は量子化されたエネルギーレベルを持っており、分子のエネルギー交換を吸光度または発光によって検出するして分析することができる[26]。分子分光法は一般に、中性子、電子、または高エネルギーX線などの粒子が(結晶のように)規則的に配列された分子と相互作用する回折研究を指すものではない。
マイクロ波分光法は、一般的に分子の回転の変化を測定するもので、宇宙空間の分子を識別するのにも使われる。赤外線分光法は、分子の振動を測定するもので、伸縮、曲げ、ねじれなどの運動を含む。これは一般的に、分子内の結合または官能基の種類を特定するために使用される。電子の配列が変化することで、紫外光、可視光、または近赤外光の吸収線や輝線を生成し、色をもたらす。核共鳴分光法は、分子内の特定の原子核の環境を測定するもので、分子内の異なる位置にある原子の数を特定するのに用いられる。
理論的側面
分子物理学や理論化学による分子の研究は、主に量子力学に基づいており、化学結合の理解には欠かせない。最も単純な分子は水素分子イオンH2+であり、化学結合の中で最も単純なものは1電子結合である。H2+は正の電荷を帯びた2個の陽子と負の電荷を帯びた1個の電子で構成されている。つまり、電子と電子の反発がないため、この系のシュレーディンガー方程式は、より簡単に解くことができる。高速デジタルコンピューターの開発により、より複雑な分子の近似解が可能になり、計算化学の主要な側面の一つとなっている。
ある原子配列が分子として「十分に安定しているか」どうかを厳密に定義しようとした場合、IUPACは「少なくとも1つの振動状態を閉じ込めるのに十分な深さの、ポテンシャルエネルギー曲面上のくぼみに対応していなければならない」と示唆している[4]。この定義は、原子間の相互作用の性質に依存するのではなく、相互作用の強さにのみ依存する。たとえば、ヘリウム二量体であるHe2は、1つの振動結合状態を持ち[27]、結合が非常に緩いため、極低温でしか観測されない可能性があるとされている。
原子の配列が「十分に安定しているか」どうかは、本質的に操作上の定義である。したがって、哲学的には、分子は基本的な実体ではなく(たとえば、素粒子とは対照的に)、むしろ分子という概念は、私たちが観察している世界における原子スケールの相互作用の強さについて、化学者が有用な声明を出す方法なのである。
関連項目
参照項目sn
- Atom
- Chemical polarity
- Covalent bond
- Diatomic molecule
- List of compounds
- List of interstellar and circumstellar molecules
- Molecular biology
- Molecular design software
- Molecular engineering
- Molecular geometry
- Molecular Hamiltonian
- Molecular ion
- Molecular modelling
- Molecular promiscuity
- Molecular orbital
- Non-covalent bonding
- Periodic systems of small molecules
- Small molecule
- Comparison of software for molecular mechanics modeling
- Van der Waals molecule
- World Wide Molecular Matrix
脚注
- ^ Iwata, Kota; Yamazaki, Shiro; Mutombo, Pingo; Hapala, Prokop; Ondráček, Martin; Jelínek, Pavel; Sugimoto, Yoshiaki (2015). “Chemical structure imaging of a single molecule by atomic force microscopy at room temperature”. Nature Communications 6: 7766. Bibcode: 2015NatCo...6.7766I. doi:10.1038/ncomms8766. PMC 4518281. PMID 26178193.
- ^ Dinca, L.E.; De Marchi, F.; MacLeod, J.M.; Lipton-Duffin, J.; Gatti, R.; Ma, D.; Perepichka, D.F.; Rosei, F. (2015). “Pentacene on Ni(111): Room-temperature molecular packing and temperature-activated conversion to graphene”. Nanoscale 7 (7): 3263–9. Bibcode: 2015Nanos...7.3263D. doi:10.1039/C4NR07057G. PMID 25619890.
- ^ Hapala, Prokop; Švec, Martin; Stetsovych, Oleksandr; Van Der Heijden, Nadine J.; Ondráček, Martin; Van Der Lit, Joost; Mutombo, Pingo; Swart, Ingmar et al. (2016). “Mapping the electrostatic force field of single molecules from high-resolution scanning probe images”. Nature Communications 7: 11560. Bibcode: 2016NatCo...711560H. doi:10.1038/ncomms11560. PMC 4894979. PMID 27230940.
- ^ a b IUPAC, Compendium of Chemical Terminology, 2nd ed. (the "Gold Book") (1997). オンライン版: (2006-) "Molecule".
- ^ Ebbin, Darrell D. (1990). General Chemistry (3rd ed.). Boston: Houghton Mifflin Co.. ISBN 978-0-395-43302-7
- ^ Brown, T.L.; Kenneth C. Kemp; Theodore L. Brown; Harold Eugene LeMay; Bruce Edward Bursten (2003). Chemistry – the Central Science (9th ed.). New Jersey: Prentice Hall. ISBN 978-0-13-066997-1
- ^ Chang, Raymond (1998). Chemistry (6th ed.). New York: McGraw Hill. ISBN 978-0-07-115221-1
- ^ Zumdahl, Steven S. (1997). Chemistry (4th ed.). Boston: Houghton Mifflin. ISBN 978-0-669-41794-4
- ^ Chandra, Sulekh (2005). Comprehensive Inorganic Chemistry. New Age Publishers. ISBN 978-81-224-1512-4
- ^ "Molecule". Encyclopædia Britannica. 22 January 2016. 2016年2月23日閲覧。
- ^ Harper, Douglas. "molecule". Online Etymology Dictionary. 2016年2月22日閲覧。
- ^ "molecule". Merriam-Webster. 2016年2月22日閲覧。
- ^ Molecule Definition Archived 13 October 2014 at the Wayback Machine. (Frostburg State University)
- ^ The Hutchinson unabridged encyclopedia with atlas and weather guide. Oxford, England. OCLC 696918830
- ^ Harry B. Gray. Chemical Bonds: An Introduction to Atomic and Molecular Structure. 1994. "Chapter 6: Bonding in Solids". p. 210-211.
- ^ "How many gold atoms make gold metal?".
- ^ Campbell, Neil A.; Brad Williamson; Robin J. Heyden (2006). Biology: Exploring Life. Boston: Pearson Prentice Hall. ISBN 978-0-13-250882-7 2012年2月5日閲覧。
- ^ Campbell, Flake C. (2008) (英語). Elements of Metallurgy and Engineering Alloys. ASM International. ISBN 978-1-61503-058-3
- ^ Roger L. DeKock; Harry B. Gray; Harry B. Gray (1989). Chemical structure and bonding. University Science Books. p. 199. ISBN 978-0-935702-61-3
- ^ Chang RL; Deen WM; Robertson CR; Brenner BM (1975). “Permselectivity of the glomerular capillary wall: III. Restricted transport of polyanions”. Kidney Int. 8 (4): 212–218. doi:10.1038/ki.1975.104. PMID 1202253.
- ^ Chang RL; Ueki IF; Troy JL; Deen WM; Robertson CR; Brenner BM (1975). “Permselectivity of the glomerular capillary wall to macromolecules. II. Experimental studies in rats using neutral dextran”. Biophys. J. 15 (9): 887–906. Bibcode: 1975BpJ....15..887C. doi:10.1016/S0006-3495(75)85863-2. PMC 1334749. PMID 1182263.
- ^ Wink, Donald J.; Fetzer-Gislason, Sharon; McNicholas, Sheila (2003) (英語). The Practice of Chemistry. Macmillan. ISBN 978-0-7167-4871-7
- ^ “ChemTeam: Empirical Formula”. www.chemteam.info. 2017年4月16日閲覧。
- ^ Hirsch, Brandon E.; Lee, Semin; Qiao, Bo; Chen, Chun-Hsing; McDonald, Kevin P.; Tait, Steven L.; Flood, Amar H. (2014). “Anion-induced dimerization of 5-fold symmetric cyanostars in 3D crystalline solids and 2D self-assembled crystals”. Chemical Communications 50 (69): 9827–30. doi:10.1039/C4CC03725A. PMID 25080328.
- ^ Zoldan, V. C.; Faccio, R; Pasa, A.A. (2015). “N and p type character of single molecule diodes”. Scientific Reports 5: 8350. Bibcode: 2015NatSR...5E8350Z. doi:10.1038/srep08350. PMC 4322354. PMID 25666850.
- ^ IUPAC, Compendium of Chemical Terminology, 2nd ed. (the "Gold Book") (1997). オンライン版: (2006-) "Spectroscopy".
- ^ Anderson JB (May 2004). “Comment on "An exact quantum Monte Carlo calculation of the helium-helium intermolecular potential" [J. Chem. Phys. 115, 4546 (2001)]”. J Chem Phys 120 (20): 9886–7. Bibcode: 2004JChPh.120.9886A. doi:10.1063/1.1704638. PMID 15268005.
外部リンク
- Molecule of the MonthTemplate:SndsSchool of Chemistry, University of Bristol
