「アセトアルデヒド脱水素酵素」の版間の差分
表示
削除された内容 追加された内容
反応式は <ce> による記述の方がソースが理解しやすい。 |
|||
| 9行目: | 9行目: | ||
| caption = [[シュードモナス属|''Pseudomonas'' sp.]]のアセトアルデヒド脱水素酵素の結晶学的構造.<ref name="pmid12764229">{{PDB|1NVM}}; {{cite journal | author = Manjasetty BA, Powlowski J, Vrielink A | title = Crystal structure of a bifunctional aldolase-dehydrogenase: sequestering a reactive and volatile intermediate | journal = Proc. Natl. Acad. Sci. U.S.A. | volume = 100 | issue = 12 | pages = 6992–7 | year = 2003 | month = June | pmid = 12764229 | pmc = 165818 | doi = 10.1073/pnas.1236794100 | url = | issn = }}</ref> |
| caption = [[シュードモナス属|''Pseudomonas'' sp.]]のアセトアルデヒド脱水素酵素の結晶学的構造.<ref name="pmid12764229">{{PDB|1NVM}}; {{cite journal | author = Manjasetty BA, Powlowski J, Vrielink A | title = Crystal structure of a bifunctional aldolase-dehydrogenase: sequestering a reactive and volatile intermediate | journal = Proc. Natl. Acad. Sci. U.S.A. | volume = 100 | issue = 12 | pages = 6992–7 | year = 2003 | month = June | pmid = 12764229 | pmc = 165818 | doi = 10.1073/pnas.1236794100 | url = | issn = }}</ref> |
||
}} |
}} |
||
'''アセトアルデヒド脱水素酵素'''(アセトアルデヒドだっすいそこうそ、Acetaldehyde Dehydrogenase; ACDH<ref name="BRENDA" />)は、[[アセトアルデヒド]]を[[アセチルCoA]]に変換する[[可逆反応]]を触媒する[[酵素]]。[[アルデヒドデヒドロゲナーゼ]](ALDH)スーパーファミリーの1種であり、CoA依存的ALDHに含まれる。Acetaldehyde Dehydrogenase (CoA-Acetylating)<ref name="Eram2013">{{Cite journal |last=Eram |first=Mohammad |last2=Ma |first2=Kesen |date=2013-08-21 |title=Decarboxylation of Pyruvate to Acetaldehyde for Ethanol Production by Hyperthermophiles |url=http://www.mdpi.com/2218-273X/3/3/578 |journal=Biomolecules |volume=3 |issue=4 |pages=578–596 |language=en | |
'''アセトアルデヒド脱水素酵素'''(アセトアルデヒドだっすいそこうそ、Acetaldehyde Dehydrogenase; ACDH<ref name="BRENDA" />)は、[[アセトアルデヒド]]を[[アセチルCoA]]に変換する[[可逆反応]]を触媒する[[酵素]]。[[アルデヒドデヒドロゲナーゼ]](ALDH)スーパーファミリーの1種であり、CoA依存的ALDHに含まれる。Acetaldehyde Dehydrogenase (CoA-Acetylating)<ref name="Eram2013">{{Cite journal |last=Eram |first=Mohammad |last2=Ma |first2=Kesen |date=2013-08-21 |title=Decarboxylation of Pyruvate to Acetaldehyde for Ethanol Production by Hyperthermophiles |url=http://www.mdpi.com/2218-273X/3/3/578 |journal=Biomolecules |volume=3 |issue=4 |pages=578–596 |language=en |doi=10.3390/biom3030578 |issn=2218-273X |pmid=24970182 |pmc=PMC4030962}}</ref>や、Acetaldehyde Dehydrogenase (acetylating)<ref name="BRENDA">{{Cite web |url=https://www.brenda-enzymes.org/enzyme.php?ecno=1.2.1.10 |title=BRENDA - Information on EC 1.2.1.10 - acetaldehyde dehydrogenase (acetylating) |accessdate=2019-09-03 |website=www.brenda-enzymes.org}}</ref>とも表記される。 |
||
以下の可逆反応を触媒する<ref name="Eram2013" />。 |
以下の可逆反応を触媒する<ref name="Eram2013" />。 |
||
| 19行目: | 19行目: | ||
:: <math>\rm acetyl-CoA</math> :[[アセチルCoA|アセチル補酵素A]]、補酵素Aと酢酸が結合した物質 |
:: <math>\rm acetyl-CoA</math> :[[アセチルCoA|アセチル補酵素A]]、補酵素Aと酢酸が結合した物質 |
||
1968年、[[大腸菌]]の嫌気環境での成長に必須な酵素として最初に発見された<ref name="Eram2013" />。その後の研究により、アセトアルデヒド脱水素反応だけを触媒するACDHと、アルコール脱水素反応も同時に触媒するACDHの2種類があることが知られている<ref name="Eram2013" />。生理反応については、微生物において[[エタノールアミン]]を利用する反応系におけるアセチルCoAの合成や、エタノールを生成する[[細菌]]においてエタノールの前駆物質となるアセトアルデヒドの合成を担うことが知られている<ref>{{Cite journal |last=Toth |first=J. |last2=Ismaiel |first2=A. A. |last3=Chen |first3=J. S. |date=1999-11 |title=The ald gene, encoding a coenzyme A-acylating aldehyde dehydrogenase, distinguishes Clostridium beijerinckii and two other solvent-producing clostridia from Clostridium acetobutylicum |url=https://www.ncbi.nlm.nih.gov/pubmed/10543811 |journal=Applied and Environmental Microbiology |volume=65 |issue=11 |pages=4973–4980 |issn=0099-2240 | |
1968年、[[大腸菌]]の嫌気環境での成長に必須な酵素として最初に発見された<ref name="Eram2013" />。その後の研究により、アセトアルデヒド脱水素反応だけを触媒するACDHと、アルコール脱水素反応も同時に触媒するACDHの2種類があることが知られている<ref name="Eram2013" />。生理反応については、微生物において[[エタノールアミン]]を利用する反応系におけるアセチルCoAの合成や、エタノールを生成する[[細菌]]においてエタノールの前駆物質となるアセトアルデヒドの合成を担うことが知られている<ref>{{Cite journal |last=Toth |first=J. |last2=Ismaiel |first2=A. A. |last3=Chen |first3=J. S. |date=1999-11 |title=The ald gene, encoding a coenzyme A-acylating aldehyde dehydrogenase, distinguishes Clostridium beijerinckii and two other solvent-producing clostridia from Clostridium acetobutylicum |url=https://www.ncbi.nlm.nih.gov/pubmed/10543811 |journal=Applied and Environmental Microbiology |volume=65 |issue=11 |pages=4973–4980 |issn=0099-2240 |pmid=10543811 |pmc=PMC91669}}</ref>。 |
||
== CoA非依存的ALDH == |
== CoA非依存的ALDH == |
||
CoA非依存的ALDHに含まれる酵素にもアセトアルデヒド脱水素酵素として機能するタンパク質があることが知られている。ヒトにおいては{{仮リンク|ALDH1A1|en|ALDH1A1}}、{{仮リンク|ALDH1B1|en|ALDH1B1}}、[[ALDH2]]の3つが以下の反応を触媒し、アセトアルデヒドを[[酢酸]]へ変換する<ref name="Koppaka2012" />。ALDH2はこの中で最もアセトアルデヒドとの結合能が高く、飲酒によって生じるアセトアルデヒドの解毒の大部分を担っている<ref name="Koppaka2012">{{Cite journal |last=Koppaka |first=Vindhya |last2=Thompson |first2=David C. |last3=Chen |first3=Ying |last4=Ellermann |first4=Manuel |last5=Nicolaou |first5=Kyriacos C. |last6=Juvonen |first6=Risto O. |last7=Petersen |first7=Dennis |last8=Deitrich |first8=Richard A. |last9=Hurley |first9=Thomas D. |date=2012-7 |title=Aldehyde Dehydrogenase Inhibitors: a Comprehensive Review of the Pharmacology, Mechanism of Action, Substrate Specificity, and Clinical Application |url=https://www.ncbi.nlm.nih.gov/pmc/articles/PMC3400832/ |journal=Pharmacological Reviews |volume=64 |issue=3 |pages=520–539 | |
CoA非依存的ALDHに含まれる酵素にもアセトアルデヒド脱水素酵素として機能するタンパク質があることが知られている。ヒトにおいては{{仮リンク|ALDH1A1|en|ALDH1A1}}、{{仮リンク|ALDH1B1|en|ALDH1B1}}、[[ALDH2]]の3つが以下の反応を触媒し、アセトアルデヒドを[[酢酸]]へ変換する<ref name="Koppaka2012" />。ALDH2はこの中で最もアセトアルデヒドとの結合能が高く、飲酒によって生じるアセトアルデヒドの解毒の大部分を担っている<ref name="Koppaka2012">{{Cite journal |last=Koppaka |first=Vindhya |last2=Thompson |first2=David C. |last3=Chen |first3=Ying |last4=Ellermann |first4=Manuel |last5=Nicolaou |first5=Kyriacos C. |last6=Juvonen |first6=Risto O. |last7=Petersen |first7=Dennis |last8=Deitrich |first8=Richard A. |last9=Hurley |first9=Thomas D. |date=2012-7 |title=Aldehyde Dehydrogenase Inhibitors: a Comprehensive Review of the Pharmacology, Mechanism of Action, Substrate Specificity, and Clinical Application |url=https://www.ncbi.nlm.nih.gov/pmc/articles/PMC3400832/ |journal=Pharmacological Reviews |volume=64 |issue=3 |pages=520–539 |doi=10.1124/pr.111.005538 |issn=0031-6997 |pmid=22544865 |pmc=3400832}}</ref>。 |
||
: <ce>CH3CHO + NAD^+ + H2O -> CH3COOH + NADH + H^+</ce> |
: <ce>CH3CHO + NAD^+ + H2O -> CH3COOH + NADH + H^+</ce> |
||
2020年1月25日 (土) 07:40時点における版
| アセトアルデヒド脱水素酵素 | |||||||||
|---|---|---|---|---|---|---|---|---|---|
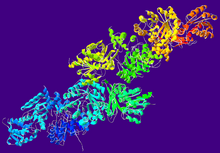 Pseudomonas sp.のアセトアルデヒド脱水素酵素の結晶学的構造.[1] | |||||||||
| 識別子 | |||||||||
| EC番号 | 1.2.1.10 | ||||||||
| CAS登録番号 | 9028-91-5 | ||||||||
| データベース | |||||||||
| IntEnz | IntEnz view | ||||||||
| BRENDA | BRENDA entry | ||||||||
| ExPASy | NiceZyme view | ||||||||
| KEGG | KEGG entry | ||||||||
| MetaCyc | metabolic pathway | ||||||||
| PRIAM | profile | ||||||||
| PDB構造 | RCSB PDB PDBj PDBe PDBsum | ||||||||
| 遺伝子オントロジー | AmiGO / QuickGO | ||||||||
| |||||||||
アセトアルデヒド脱水素酵素(アセトアルデヒドだっすいそこうそ、Acetaldehyde Dehydrogenase; ACDH[2])は、アセトアルデヒドをアセチルCoAに変換する可逆反応を触媒する酵素。アルデヒドデヒドロゲナーゼ(ALDH)スーパーファミリーの1種であり、CoA依存的ALDHに含まれる。Acetaldehyde Dehydrogenase (CoA-Acetylating)[3]や、Acetaldehyde Dehydrogenase (acetylating)[2]とも表記される。
以下の可逆反応を触媒する[3]。
-
- : ニコチンアミドアデニンジヌクレオチドの酸化型
- : ニコチンアミドアデニンジヌクレオチドの還元型
- : 補酵素A
- :アセチル補酵素A、補酵素Aと酢酸が結合した物質
1968年、大腸菌の嫌気環境での成長に必須な酵素として最初に発見された[3]。その後の研究により、アセトアルデヒド脱水素反応だけを触媒するACDHと、アルコール脱水素反応も同時に触媒するACDHの2種類があることが知られている[3]。生理反応については、微生物においてエタノールアミンを利用する反応系におけるアセチルCoAの合成や、エタノールを生成する細菌においてエタノールの前駆物質となるアセトアルデヒドの合成を担うことが知られている[4]。
CoA非依存的ALDH
CoA非依存的ALDHに含まれる酵素にもアセトアルデヒド脱水素酵素として機能するタンパク質があることが知られている。ヒトにおいてはALDH1A1、ALDH1B1、ALDH2の3つが以下の反応を触媒し、アセトアルデヒドを酢酸へ変換する[5]。ALDH2はこの中で最もアセトアルデヒドとの結合能が高く、飲酒によって生じるアセトアルデヒドの解毒の大部分を担っている[5]。
関連項目
脚注
- ^ PDB: 1NVM; Manjasetty BA, Powlowski J, Vrielink A (June 2003). “Crystal structure of a bifunctional aldolase-dehydrogenase: sequestering a reactive and volatile intermediate”. Proc. Natl. Acad. Sci. U.S.A. 100 (12): 6992–7. doi:10.1073/pnas.1236794100. PMC 165818. PMID 12764229.
- ^ a b “BRENDA - Information on EC 1.2.1.10 - acetaldehyde dehydrogenase (acetylating)”. www.brenda-enzymes.org. 2019年9月3日閲覧。
- ^ a b c d Eram, Mohammad; Ma, Kesen (2013-08-21). “Decarboxylation of Pyruvate to Acetaldehyde for Ethanol Production by Hyperthermophiles” (英語). Biomolecules 3 (4): 578–596. doi:10.3390/biom3030578. ISSN 2218-273X. PMC PMC4030962. PMID 24970182.
- ^ Toth, J.; Ismaiel, A. A.; Chen, J. S. (1999-11). “The ald gene, encoding a coenzyme A-acylating aldehyde dehydrogenase, distinguishes Clostridium beijerinckii and two other solvent-producing clostridia from Clostridium acetobutylicum”. Applied and Environmental Microbiology 65 (11): 4973–4980. ISSN 0099-2240. PMC PMC91669. PMID 10543811.
- ^ a b Koppaka, Vindhya; Thompson, David C.; Chen, Ying; Ellermann, Manuel; Nicolaou, Kyriacos C.; Juvonen, Risto O.; Petersen, Dennis; Deitrich, Richard A. et al. (2012-7). “Aldehyde Dehydrogenase Inhibitors: a Comprehensive Review of the Pharmacology, Mechanism of Action, Substrate Specificity, and Clinical Application”. Pharmacological Reviews 64 (3): 520–539. doi:10.1124/pr.111.005538. ISSN 0031-6997. PMC 3400832. PMID 22544865.






