C型肝炎
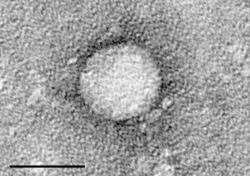
C型肝炎(Cがたかんえん、英: Hepatitis C)とは、C型肝炎ウイルス(HCV)に感染することで発症するウイルス性肝炎の一つ。かつては非A非B型肝炎[1]輸血後肝炎・血清肝炎[2]と呼ばれていた。C肝とも呼ばれる。
疫学
[編集]現在の日本のHCV感染者数は約200万人、世界では1億7千万人(世界人口の3パーセント近く)がキャリアであると見られている。
日本ではインターフェロン治療が効きにくい1b型が70 - 85パーセントを占め、以降2a型が10 - 15パーセント、2b型が約5パーセントで、他はまれである。ただし、血友病患者では1a型が多い。これは、血友病患者がC型肝炎に罹患する原因となった、血液製剤の輸入元であるアメリカ合衆国では、1a型が最も多いことに由来する。
U.S. Preventive Services Task Forceは、1945〜1965年生まれの全てのアメリカ人に対して、C型肝炎スクリーニングを推奨することとした[3]。
感染経路
[編集]HCVは血液が主な感染経路で、かつては輸血による感染が多かった。ディスポーザブル注射器の普及により現在においては先進国では検査体制が確立したためほとんど見られない。現在は針刺し事故や、鍼、ピアス、入れ墨(刺青)、覚醒剤注射の回し打ちなどが主である。カミソリの共用、歯ブラシの取り違え、コンタクトスポーツでも感染者の血液や唾液の付着による感染リスクがある。B型肝炎と異なり、性行為ではほとんど感染せず[4]、また母子感染も少ない。
性行為感染は、1回毎の性行為で感染が起こる頻度は低いとしても、感染者との接触を続ける限りは起こり得ると見るべきであり、感染頻度に性交回数が関与するという報告もある[要出典]。
日本では性行為感染の報告例は高齢者層が多いが、高齢者層では性活動が減退するため、感染者が多い世代の高齢化、他の原因による感染が考えにくいことにより、性行為感染と特定できるといった理由が考えられる。ただし老化による粘膜の脆弱化、免疫能の低下、閉経後にコンドームを使用しなくなるといった、高齢者層の感染を助長する要因もある[5]。
血液製剤(フィブリノゲン製剤、第IX因子製剤)の投与によるC型肝炎感染については、非血友病患者に対する投与に対して、日本国政府と製薬会社を相手とする訴訟(薬害肝炎訴訟)が起こされている。
病態
[編集]初期感染
[編集]一般に自覚症状が乏しい場合もあるが、発熱、全身倦怠感、食欲不振、吐き気、嘔吐、口腔扁平苔癬[6]が出現し、血液検査にて肝障害(AST・ALT高値)、黄疸総ビリルビン(T-Bil)高値)を認めるといった急性肝炎症状を呈する場合が多い。なお、B型肝炎やA型肝炎に比較して劇症肝炎を呈する例は稀である。
持続感染
[編集]初期感染後に、血液検査にてALT値が正常化しHCV-RNAも陰性となってC型肝炎ウイルスが排除され治癒する場合もあるが、70パーセント程度はC型肝炎ウイルスが排除されず、血液検査にてHCV-RNA陽性状態が続き、持続感染状態となる。
慢性肝炎
[編集]血液検査にて、HCV-RNA陽性でALT値が正常な場合は無症候性キャリアであるが、多くの場合はALT高値持続し慢性肝炎状態となる。ALT高値が持続する慢性肝炎の状態を5〜10年以上経過することで、その後肝硬変への移行・肝細胞癌発症となってくる。慢性肝炎持続の場合、約60パーセントが肝硬変へと進展し、肝硬変後は年間7 - 8パーセントが肝細胞癌を発症する。肝硬変に至る前は肝細胞癌への発症率は低い。肝硬変になると腹水貯留や浮腫(むくみ)、黄疸などの症状が現れ、腎臓の炎症(膜性増殖性糸球体腎炎)を合併することがある[7]。
検査
[編集]問診
[編集]基本的に血液感染によって成立するため、輸血、注射、手術、針刺し事故、覚醒剤注射などの感染の原因となりうることがあったかどうかを確認が大切である。
血液検査
[編集]血液検査の目的は主に肝炎があるかどうかや、肝炎の程度、肝臓の機能を調べること。
- ウイルス検査
- HCV抗体:多くの医療機関・検診等にてスクリーニングで施行。感染初期には陰性を呈する場合も多い。
- HCV-RNA:C型肝炎ウイルスのRNA量を測定する。手法はいくつがあるが、現在主にTaqMan real-time PCR法が用いられる。HCV抗体陽性でも、HCV-RNA陰性の場合は既感染・治癒症例と診断する。HCVウイルス量は、治療成功予測因子でもある。抗ウイルス治療後の効果判定にも用いられる。発癌とウイルス量は相関しない。
- HCV-RNA定量のDNA-probe法やTMA法は、測定感度が低く、現在はあまり用いられない。
- HCV-RNA genotype/serotype:HCV-RNAの型によってインターフェロン療法の治療効果推測に用いられる。
- 肝障害
- 肝線維化
- 肝機能
- 肝細胞癌の腫瘍マーカー
- AFP、AFP-L3、PIVKA-II:これらは肝炎マーカーではないが、肝癌スクリーニングのため、上記検査と同時に行われることが多い。
画像検査
[編集]以下の画像検査によって、慢性肝炎〜肝硬変・肝細胞癌の発生を評価していく。
病理組織検査
[編集]治療
[編集]A型肝炎やB型肝炎などと異なり、有効なワクチンは実用化されていない。慢性C型肝炎の治療の目的は、C型肝炎ウイルスの除去による慢性肝炎の沈静化(ALT値の正常化)と、その後の肝硬変への移行・肝細胞癌発症の阻止にある。急性C型肝炎は基本的に保存的加療がなされる。
抗ウイルス療法
[編集]抗ウイルス治療は、C型肝炎ウイルスを排除する治療である。従来は組換えタンパク質製剤であるヒトインターフェロンを基本とした治療が基軸であったが、その後は「直接作用型抗ウイルス剤(Direct Acting Antivirals; DAA)」の治療成績が極めて良好で、非常に高額な治療費であるが、第一選択薬として行われている。
治療効果は、血液検査にてHCV-RNA量を測定して評価する。治療終了後6ヶ月の時点まで、HCV-RNA陰性が持続している状態を「ウイルス学的著効 (SVR; sustained virological response)」と言う。
- 治療対象
「日本肝臓学会」による治療対象は「肝細胞癌を発症していない非代償期肝硬変以外のすべてのC型肝炎症例」が、抗ウイルス療法の治療対象である。肝病変以外の合併疾患にて、予後が不良である場合には適応としないことや、肝細胞癌を発症している場合には、癌の治療コントロールが優先とされ、癌の治療を終えて再発を認めていない場合にのみ治療対象とされている。
治療費が高額であるため、指定専門医療機関での指定専門医の診断申請による公費負担医療が必須であり、左記の治療適応が決められている。
- 直接作用型抗ウイルス薬(Direct acting Antiviral Agents:DAAs)
- 以下の直接作用型抗ウイルス薬(Direct acting Antiviral Agents:DAAs)が開発され、治療成績が非常に良好で、第一選択として行われている。中でもマヴィレットやハーボニーは、ガイドラインにおいて、多くの症例で第一選択とされている[8]。
- ただ、非常に高額な薬剤であることが世界的に問題となっており、日本においては指定医療機関での指定専門医による診断申請で、公費負担医療になる制度が存在している。
- また薬剤耐性遺伝子変異(NS5A領域上のL31M/V、Y93Hや、NS3/4A領域上のD168A/E/Vなど)がある症例では、一部治療効果が低くなることが知られており、高額治療のため薬剤選択適応において、慎重な判断が必要とされる。
- NS3/4A(プロテアーゼ)阻害薬
- ボセプレビル Boceprevir(BOC) :日本未承認。
- テラプレビル Telaprevir(TVR) : TVR(テラビック Telavic インシベックIncivek バーテックス・ファーマシューティカルズ)として日本で最初に承認されたDAA製剤で、遺伝子型(genotype:GT)1a、1b、2a、2bのC型慢性肝炎に対し、PEG-IFNα2b+RBV+TVRの3剤併用療法で使用された(2011年-2017年)。服用回数の多さ(1日3回)、副作用、インターフェロンフリーのDAAsの登場などにより使用機会が減少。現在製造販売終了。
- シメプレビル Simeprevir(SMV):SMV(ソブリアード Sovriad ヤンセン)として、GT1a、1bのC型慢性肝炎に対し、PEG-IFNα-2a (or 2b) +RBV+SMVの3剤併用療法で使用された(2013年-2019年)。現在製造販売終了。本剤の販売終了により、日本ではDAA製剤によるC型慢性肝炎の治療はすべてインターフェロンフリーとなった。
- ファルダプレビル Faldaprevir:日本未承認。
- バニプレビル Vaniprevir(VPV) : VPV(バニヘップ Vanihep メルク)として、GT1a、1bのC型慢性肝炎に対し、PEG-IFNα-2b+RBV+VPVの3剤併用療法で使用された(2014年-2016年)。現在製造販売終了。
- アスナプレビル Asunaprevir(ASV):ASV(スンベプラ Sunvepra ブリストル・マイヤーズ)としてDCV+ASV 2剤併用療法があり、GT1のウイルスに対して髙いSVR効果を示す。後継の他薬よりも服用回数が1日2回とやや多く、治療期間も24週と他薬に比べてやや長い(後継薬では8-12週が主流)。また併用禁止薬も非常に多い。ただし、インターフェロンフリーで使用可能なDAAの中ではやや安価(DCVとの併用で1.4万円/日、228万円/24週)。現在製造販売終了。
- パリタプレビル Paritaprevir(PTV):OBV+PTV/rの3剤配合剤(ヴィキラックス Viekirax アッヴィ)としてGT1のウイルスに対して使用された(2015年-2018年)。非常に高いSVR効果を示したが非常に高額であった(2017年時点で4.6万円/2錠/日、387万円/12週)。現在は製造販売終了。
- リトナビル Ritonavir(RTV/r):OBV+PTV/rの3剤配合剤(ヴィキラックス Viekirax アッヴィ)に含まれ、NS3/4Aに対する作用よりもCYP3A4に対する阻害作用により、OBV、PTVの有効濃度を高めるためのブースターとして配合された(ヴィキラックスとしては2018年に販売終了)。
- グラゾプレビル Grazoprevir (GZR):GZR(グラジナ Grazyna メルク)ないしEBV+GZR の2剤配合剤(ゼパティア ZEPATIER メルク.国内未承認)があり、GT1のウイルスに対して非常に髙いSVR効果を示す。現在製造販売終了。
- グレカプレビル Glecaprevir (GCR):GCR+PBVの2剤配合剤(マヴィレット Mavyret アッヴィ)があり、GT1~6までのすべての遺伝子型(pangenotype)に対して短期間(GT1,2のC型慢性肝炎なら8週間、それ以外は12週間)に髙いSVR効果を示す。また小児適応が認められており、2017年の承認時は12歳以上、2022年に3歳以上と適応が拡大された。マヴィレットとしての薬価は5.5万円/日、308万円/8週(2022年現在)。
- NS5A阻害薬
- ダクラタスビル Daclatasvir(DCV):DCV(ダクルインザ Daklinza ブリストル・マイヤーズ)としてDCV+ASV 2剤併用療法があり、GT1のウイルスに対しての非常に高いSVR効果を示す。非常に高額であるが、インターフェロンフリーで使用可能なDAAの中ではやや安価(DCVとの併用で1.4万円/日、228万円/24週)。現在製造販売終了。
- レジパスビル Ledipasvir(LDV):LDV+SOF の2剤配合剤(ハーボニー Harvoni ギリアド・サイエンシズ)があり、GT1のウイルスに対して非常に高いSVR効果を示す。腎機能低下例または心疾患合併例に対しては非対応。薬価はハーボニーとして5.5万円/日、466.1万円/12週(2022年現在)。
- オムビタスビル Ombitasvir(OBV):OBV+PTV/rの3剤配合剤(ヴィキラックス Viekirax アッヴィ)GT1のウイルスに対して使用された(2015年-2018年)。非常に高いSVR効果を示したが非常に高額であった(2017年時点で4.6万円/2錠/日、387万円/12週)。現在は製造販売終了。
- エルバスビル Elbasvir(EBV):EBV(エレルサ Erelsa メルク)ないしEBV+GZR の2剤配合剤(ゼパティア Zepatier メルク)があり、GT1のウイルスに対して非常に高いSVR効果を示す。現在製造販売終了。
- ピブレンタスビル Pibrentasvir(PBV):GCR+PBVの2剤配合剤(マヴィレット Mavyret アッヴィ)があり、GT1~6までのすべての遺伝子型(pangenotype)に対して短期間(GT1,2のC型慢性肝炎なら8週間、それ以外は12週間)に髙いSVR効果を示す。また小児適応が認められており、2017年の承認時は12歳以上、2022年に3歳以上と適応が拡大された。マヴィレットとしての薬価は5.5万円/日、308万円/8週(2022年現在)。
- ベルパタスビル Velpatasvir(VEL):SOF+VELの2剤配合剤(エプクルーサ Epclusa ギリアド・サイエンシズ)があり、GT1~6までのすべての遺伝子型(pangenotype)に対して非常に高いSVR効果を示す。エプクルーサとしての薬価は6.1万円/日、514万円/12週(2022年現在)。
- NS5B(ポリメラーゼ)阻害薬
- ソホスブビル Sofosbuvir(SOF):SOF+LDV配合剤(ハーボニー Harvoni ギリアド・サイエンシズ)や、SOF+VELの2剤配合剤(エプクルーサ Epclusa ギリアド・サイエンシズ)があり、エプクルーサではGT1~6型までのすべての遺伝子型(pangenotype)に対して非常に高いSVR効果を示す。薬価は、ハーボニーとして5.5万円/日(459万円/12週)、エプクルーサとして6万円/日(505万円/12週)。また、以前よりSOF単剤(ソバルディ Sovaldi ギリアド・サイエンシズ)+RBVの2剤併用療法でも使用されており、GT2のウイルスに対して非常に高いSVR効果を示してきた。単剤の薬価は4.2万円/日、355万円/12週。重度腎機能障害例での使用は禁忌。2022年、単剤での販売が終了し、現在は合剤のハーボニーまたはエプクルーサとしてのみ処方される。
- ダサブビル Dasabuvir(DSB):OBV+PTV/r+DSBの4剤配合剤(ヴィキラパック Viekira Pak アッヴィ.国内未承認)があり、GT1のウイルスに対して非常に高いSVR効果を示す。
- ベクラブビル Beclabuvir(BCV):DCV+ASV+BCVの3剤配合剤(ジメンシー Ximency ブリストル・マイヤーズ) として用いられ、GT1のウイルスに対して非常に高いSVR効果を示した(2016年-2018年)。現在は製造販売終了。
- NS3/4A(プロテアーゼ)阻害薬
- インターフェロン治療(IFN)
- インターフェロン (IFNα) を基本とし、IFNα単独療法から、IFNα2b+Ribavirin(RBV; リバビリン)併用療法が開発され発展してきた。以下のポリエチレングリコールを付加し体内停滞時間を持続させたペグインターフェロン (PEG-IFNα)+RBVの併用療法が一般的であった。治療方法はウイルスのserotype(血清型)やgenotype(遺伝子型)によって選択されていた。基本は24週間の投薬で、治癒が見られない場合はさらに24週間の計48週間の投薬治療が行われていた。サイトカインであるインターフェロンの投与であることから、様々な副作用の問題もあった。
- PEG-IFNα2a+RBV
- PEG-IFNα2b+RBV:現在製造販売終了。
- また以下のIFNを用いることもあった。
- IFNα
- IFNα:肝硬変進行例でも適応
- IFNβ:肝硬変進行例でも適応
- Consensus-IFNα・IFNαcon1
- 血液浄化療法
- VRAD(virus removal and eradication by DFPP:ウイルス除去療法)と呼ばれ、IFN治療に二重濾過血漿交換療法を併用することで治療効果を高める目的で施行されていた。
- その他
- 一般的ではないが、スタチン(脂質異常症治療剤)製剤をインターフェロンに併用して行う治療方法があり、臨床学的信頼性は低いものの、安価でかつ可能性のある療法として選択されていた。スタチンによりウイルスが成熟に必要な脂質が不足し、ウイルス粒子複製を阻害すると考えられている[9]。
肝庇護療法
[編集]抗ウイルス療法以外に、ALT値の正常化を計る目的で、以下が用いられていた。
肝外病変
[編集]- C型肝炎ウイルスによって肝臓以外の病変を合併している場合は、肝外病変の治療も並行して行う[11]。
- 主な病態は、クリオグロブリン血症[12]、膜性増殖性糸球体腎炎、晩発性皮膚ポルフィリン症、シェーグレン症候群、慢性甲状腺炎、悪性リンパ腫、扁平苔癬
- 血中の鉄分が肝障害を与えるとし、瀉血療法を用いることもある(鉄による酸化ストレスを軽減すると考えられている)[10]。
- シクロスポリンを併用している肝/腎移植後や乾癬を合併したC型肝炎患者では、HCVの増殖が抑制されることが観察されている。研究ではシクロフィリンがHCV複製に重要な働きをしていることが示唆されている[13][14](類薬であっても、シクロフィリンでなくFKBPに作用するタクロリムスでは抑制されない)。
- ウイルスを排除できた (SVR) 後にも、SVR肝癌と呼ばれる発癌症例がまれにみられるため、治療終了後も肝癌スクリーニングは必要とされる[15]。
予防
[編集]この節の加筆が望まれています。 |
注射器から外したキャップを再び針につける際に事故が起こりやすいため、しないようにする(リキャップ禁止)。また感染者の体液や血液は、適切に処置するようにする。針刺し事故では、血液を絞り出しつつ速やかに傷口を流水で洗い流す[16]。医療事故後に予防的にインターフェロンを投与することもある。
出典
[編集]- ^ 下遠野邦忠、C型肝炎の克服に向けて ウイルス 53巻 (2003) 1号 p.87-91, doi:10.2222/jsv.53.87
- ^ “輸血後肝炎”. 一般社団法人 日本血液製剤協会. 2019年9月18日閲覧。
- ^ Ann Intern Med 2013 Jun 25; [e-pub ahead of print].
- ^ Terrault, Norah A.; Jennifer L. Dodge, Edward L. Murphy, John E. Tavis, Alexi Kiss, T. R. Levin, Robert G. Gish, Michael P. Busch, Arthur L. Reingold, Miriam J. Alter (March 2003). “Sexual Transmission of Hepatitis C Virus Among Monogamous Heterosexual Couples: The HCV Partners Study”. HEPATOLGY (American Association for the Study of Liver Diseases) 57 (3): 881-889.
- ^ 相川達也、小島眞樹、宮本久仁子、上野ちさと、高橋雅春、岡本宏明「結婚40年後の配偶者間性行為感染が疑われたC型急性肝炎の1例」(PDF)『肝臓』第49巻8号、2008年9月、352-361頁、doi:10.2957/kanzo.49.352。
- ^ 渡邉陽、柴崎浩一、山口晃、口腔癌患者における肝炎ウイルスの持続感染とその臨床的意義 日本口腔科学会雑誌 Vol.49 (2000) No.2 P112-121
- ^ 慢性肝炎 メルクマニュアル18版 日本語版
- ^ “C型肝炎治療ガイドライン”. 日本肝臓学会. 2019年11月21日閲覧。
- ^ Rosen HR (2011). “Clinical practice. Chronic hepatitis C infection”. N. Engl. J. Med. 364 (25): 2429-2438. doi:10.1056/NEJMcp1006613. PMID 21696309.
- ^ a b c 伊藤義人、岡上武、「慢性肝炎治療の新たな展開、 5. 難治性C型慢性肝炎に対する非抗ウイルス療法の実際と有用性」、『肝臓』、Vol.43 (2002) No.10 P.442-445, doi:10.2957/kanzo.43.442
- ^ 長尾由実子、佐田通夫、C型肝炎ウイルスと肝外病変 日本消化器病学会雑誌 Vol.96 (1999) No.11 P.1249-1257, doi:10.11405/nisshoshi1964.96.1249
- ^ 巴雅威、高取正雄、岩渕省吾 ほか、本邦のC型慢性肝疾患におけるクリオグロブリン血症についての検討 日本消化器病学会雑誌 Vol.94 (1997) No.4 P.241-248, doi:10.11405/nisshoshi1964.94.241
- ^ 学術月報 57(8): 704-708, 2004
- ^ 医薬ジャーナル 40(7):1990-1993, 2004
- ^ 池田健次、インターフェロン治療によりHCV RNAが消失した後の肝発癌について 肝臓 Vol.48 (2007) No.2 P.43-47, doi:10.2957/kanzo.48.43
- ^ 針刺し事故対応マニュアル 全日本民主医療機関連合会
関連項目
[編集]- 壊疽性膿皮症 - 合併することがある。
- ラクトフェリン
- World Community Grid - 新薬開発のための分散コンピューティング
- 伍代夏子 - C型肝炎であることを公表した。
- 猿島町(現坂東市) - 1962年から局地的に肝炎の患者が発生、当時は奇病と騒がれたが疫学調査などで井戸水を媒介としたC型肝炎であることが判明した。
外部リンク
[編集]- C型肝炎 - 国立研究開発法人 国立国際医療研究センター 肝炎情報センター
- C型肝炎とは(2013年06月19日改訂) - NIID 国立感染症研究所
- C型肝炎について(ファクトシート) - 厚生労働省検疫所 FORTH、2017年10月
