拡張周期表
拡張周期表(かくちょうしゅうきひょう、extended periodic table)とは、ドミトリ・メンデレーエフの周期表を未知の超重元素の領域まで論理的に発展させた周期表である。未知の元素についてはIUPACの元素の系統名に準じて表記される。原子番号119(ウンウンエンニウム)以降の元素は全て未発見である(発見報告無し)。
現在発見されているよりも大きい原子番号の元素が発見された場合には、既存の周期と同様に、その元素の性質が周期的に繰り返される傾向を示すようにレイアウトされた、追加の周期に置かれることになるだろう。追加される周期は、第7周期よりも多くの元素を含むことが予想される。これは、いわゆるgブロックが追加され、g軌道の一部が満たされた少なくとも18個の元素が含まれると計算されるからである。gブロックと第8周期を含む周期表は、1969年にグレン・シーボーグによって提案された[1][2]。 gブロックの最初の元素は原子番号121である可能性があり、その場合ウンビウニウムという系統名を持つことになる。この領域の元素は、多くの探索にもかかわらず、合成されたり自然界で発見されたりしていない[3]。
原子構造の量子力学的記述における軌道近似計算によれば、gブロックは部分的にg軌道が充填された元素に対応するが、スピン軌道相互作用により、原子番号の高い元素では軌道近似計算の有効性が大幅に低下する。シーボーグの拡張周期表では相対論的効果を考慮していなかったため、重い元素が軽い元素のパターンに従っていたが、相対論効果を考慮したモデルでは異なる。ペッカ・ピューッコとブルクハルト・フリッケはコンピュータモデルを用いてZ = 172までの元素の配置を計算し、いくつかの元素が構造原理からずれていることを発見した[4]。 原子番号120を超える元素の化学的・物理的性質の予測には不確実性とばらつきがあるため、現在のところ拡張周期表における元素の配置についてはコンセンサスが得られていない。
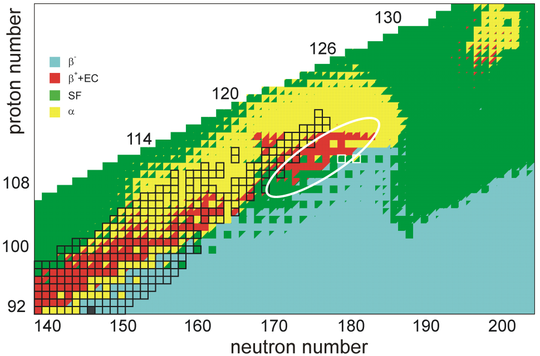
この領域の元素は、放射性崩壊に対して非常に不安定であり、半減期が極めて短いアルファ崩壊や自発核分裂を起こす可能性が高いが、126番元素は自発核分裂には耐性があるがアルファ崩壊を起こす安定の島にあると考えられている。既知の元素以降にも安定の島が存在する可能性があり、その中には164番元素を中心に理論化されたものも含まれるが、閉じた核の殻による安定化効果がどの程度あるかは不明である。予測される安定の島を超えて元素が物理的にどのくらい存在可能なのか、第8周期に終わりがあるのか、第9周期があるのかは明らかではない。国際純正・応用化学連合(IUPAC)では、原子核が電子雲を形成する時間である10-14秒(0.01ピコ秒、10フェムト秒)よりも寿命が長い元素を存在の定義としている[5]。
1940年には、相対論的なディラック方程式を単純に解釈すると、Z > 1/α ≈ 137の電子軌道が問題となることが指摘されていた。137番元素より先には中性原子が存在できず、電子軌道に基づく元素周期表はこの時点で破綻することが示唆されていた[6]。 一方、より厳密な分析では、類似の限界をZ ≈ 168から172までと計算し、ここで1s電子軌道がディラックの海に飛び込むとした。ただし、これを超えて存在できないのは中性原子ではなく裸の原子核であり、周期系のさらなる拡張を妨げるものではないとしている。この臨界原子番号を超える原子を「超臨界原子」と呼ぶ。
歴史
[編集]アクチノイドより重い元素の存在は既に1895年には提案されており、デンマークの化学者ユリウス・トムセンが、ウランやトリウムを含む32元素の周期(第7周期)は、化学的に不活性な原子量292の元素で終わることを予測していた。これは、オガネソンで現在唯一発見されている同位体の原子量294に近い。1913年、スウェーデンの物理学者ヨハネス・リュードベリは、ラドンの次の貴ガスは原子番号118であると同様に予測し、ラドンより重い同族体は Z = 168, 218, 290, 362, 460 であることを、純粋に構造原理より導き出した。ニールス・ボーアは1922年に、ラドンの次となる貴ガスの電子構造を Z = 118 と予測し、また自然界でウランより原子番号が大きい元素が見られないのは、あまりにも不安定だからであると指摘した。ドイツの物理学者で技術者でもあるRichard Swinneは、1926年に超ウラン元素についての予測を含むレビュー論文を発表し、安定の島という現代の予測を先取りしていた。彼は1914年より、半減期は厳密には原子番号とともに減少しないという仮説を立て、Z = 98–102 と Z = 108–110 に長寿命の元素があるかもしれないと示唆し、こうした元素は地球の核、鉄隕石、あるいは宇宙起源の物質がグリーンランド氷床(en:Greenland ice sheet)の中に閉じ込められて存在しているのではないかと推測していた[7]。1955年には、これらの元素は超重元素と呼ばれるようになった[8]。
未発見の超重元素の性質について最初の予測がなされたのは1957年のことで、殻模型の概念が初めて検討され、126番元素近辺に安定の島が存在することが理論的に示された[9]。1967年にはより厳密な計算が行われ、安定の島は当時未発見のフレロビウム(114番元素)を中心にしていることが理論づけられた。この研究やその後の研究により、多くの研究者が自然界での超重元素の探索や、加速器での合成を試みるようになった[8]。1970年代に超重元素の多くの検索が行われたが、いずれも否定的な結果だった。元素合成は、ウンビトリウム (Z = 123) を除くウンビセプチウム (Z = 127) までの元素で試みられ[10] [11][12]、合成に成功した最も重い元素は2002年のオガネソン、最も新しい元素の発見は2010年のテネシンである[10]。
一部の超重元素は周期表の第7周期を超えると予測されたため、これらの元素を含む追加の第8周期が、1969年にグレン・シーボーグによって最初に提案された。このモデルは既存元素のパターンを継承しつつ、gブロックおよび121番元素から始まる超アクチノイド系列を導入し、今までの周期よりも第8周期の元素数が増えている[1][8]。しかしこれら初期の計算では、周期的な傾向を崩し、単純な予測が不可能になる相対論的な効果を考慮していなかった。
1971年、ドイツの化学者Frickeは Z = 172 までの周期表を計算し、いくつかの元素が既存のパターンと異なる特性を持つことを発見した。また、2010年にペッカ・ピューッコが行った計算でも、いくつかの元素が予想とは異なる振る舞いをする可能性があるとされている[13]。重い元素ほどより不安定になると予測されているため、周期表が既知の118元素を超えてどこまで拡張されるかは未知数である。グレン・シーボーグは、実際には核の不安定性のために、早ければ Z = 120 付近で周期表の終わりが来るのではないかと示唆している[14]。
拡張周期表の予想される構造
[編集]周期表における原子番号120を超える元素の配置については、現在合意が得られていない。
すべての仮説上の元素には、国際純正・応用化学連合(IUPAC)の体系的な元素名が与えられる。それらの元素が発見および確認され、正式名称が承認されるまで使用される。これらの名前は通常、文献では使用されず、元素は原子番号で参照される。したがって、164番元素は、「ウンヘキサクアジウム」または「Uhq」(体系名と記号))ではなく「164番元素」、または記号で「164」、「(164)」、または「E164」と呼ばれる[15]。
シーボーグの拡張周期表
[編集]1969年にアメリカの化学者グレン・シーボーグが提案した周期表である。第7周期までの法則に合わせて、素直にGブロックを配置した形をしている。構造原理からの単純な外挿では、8行目は8s、5g、6f、7d、8pの順序で軌道が満たされると予測されるが、121番元素以降では電子殻のエネルギーが近接しているため、単純な表に配置することが困難になる。
| Period | s1 | s2 | ||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 1 | 1 H |
2 He |
p1 | p2 | p3 | p4 | p5 | p6 | ||||||||||||||||||||||||||||||||||||||||||
| 2 | 3 Li |
4 Be |
5 B |
6 C |
7 N |
8 O |
9 F |
10 Ne | ||||||||||||||||||||||||||||||||||||||||||
| 3 | 11 Na |
12 Mg |
d1 | d2 | d3 | d4 | d5 | d6 | d7 | d8 | d9 | d10 | 13 Al |
14 Si |
15 P |
16 S |
17 Cl |
18 Ar | ||||||||||||||||||||||||||||||||
| 4 | 19 K |
20 Ca |
21 Sc |
22 Ti |
23 V |
24 Cr |
25 Mn |
26 Fe |
27 Co |
28 Ni |
29 Cu |
30 Zn |
31 Ga |
32 Ge |
33 As |
34 Se |
35 Br |
36 Kr | ||||||||||||||||||||||||||||||||
| 5 | 37 Rb |
38 Sr |
f1 | f2 | f3 | f4 | f5 | f6 | f7 | f8 | f9 | f10 | f11 | f12 | f13 | f14 | 39 Y |
40 Zr |
41 Nb |
42 Mo |
43 Tc |
44 Ru |
45 Rh |
46 Pd |
47 Ag |
48 Cd |
49 In |
50 Sn |
51 Sb |
52 Te |
53 I |
54 Xe | ||||||||||||||||||
| 6 | 55 Cs |
56 Ba |
57 La |
58 Ce |
59 Pr |
60 Nd |
61 Pm |
62 Sm |
63 Eu |
64 Gd |
65 Tb |
66 Dy |
67 Ho |
68 Er |
69 Tm |
70 Yb |
71 Lu |
72 Hf |
73 Ta |
74 W |
75 Re |
76 Os |
77 Ir |
78 Pt |
79 Au |
80 Hg |
81 Tl |
82 Pb |
83 Bi |
84 Po |
85 At |
86 Rn | ||||||||||||||||||
| 7 | 87 Fr |
88 Ra |
g1 | g2 | g3 | g4 | g5 | g6 | g7 | g8 | g9 | g10 | g11 | g12 | g13 | g14 | g15 | g16 | g17 | g18 | 89 Ac |
90 Th |
91 Pa |
92 U |
93 Np |
94 Pu |
95 Am |
96 Cm |
97 Bk |
98 Cf |
99 Es |
100 Fm |
101 Md |
102 No |
103 Lr |
104 Rf |
105 Db |
106 Sg |
107 Bh |
108 Hs |
109 Mt |
110 Ds |
111 Rg |
112 Cn |
113 Nh |
114 Fl |
115 Mc |
116 Lv |
117 Ts |
118 Og |
| 8 | 119 Uue |
120 Ubn |
121 Ubu |
122 Ubb |
123 Ubt |
124 Ubq |
125 Ubp |
126 Ubh |
127 Ubs |
128 Ubo |
129 Ube |
130 Utn |
131 Utu |
132 Utb |
133 Utt |
134 Utq |
135 Utp |
136 Uth |
137 Uts |
138 Uto |
139 Ute |
140 Uqn |
141 Uqu |
142 Uqb |
143 Uqt |
144 Uqq |
145 Uqp |
146 Uqh |
147 Uqs |
148 Uqo |
149 Uqe |
150 Upn |
151 Upu |
152 Upb |
153 Upt |
154 Upq |
155 Upp |
156 Uph |
157 Ups |
158 Upo |
159 Upe |
160 Uhn |
161 Uhu |
162 Uhb |
163 Uht |
164 Uhq |
165 Uhp |
166 Uhh |
167 Uhs |
168 Uho |
| Sブロック元素 | Pブロック元素 | Dブロック元素 | Fブロック元素 | Gブロック元素 |
Frickeの拡張周期表
[編集]すべてのモデルが、より軽い元素によって確立されたパターンに従って、より重い元素を示しているわけではない。ドイツの化学者であるBurkhard Frickeらは、1971年に発表された論文で、172番元素までおよび184番元素の計算を行った。電子軌道のエネルギーが重なった結果として、一部の元素がマーデルング則(en:Madelung rule)から外れることも発見した。これは、重い元素における相対論効果の役割が増大していることが原因である[4][16]。
Frickeらの形式は、起こり得る化学的挙動よりも、形式的な電子配置に重点を置いている。彼らは156番元素から164番元素を4族から12族に配置しているが、これらの電子配置が7d2から7d10になると考えたためである。ただし、それらは、8s電子殻が化学結合に利用できず、代わりに9s電子殻が利用できる点で、今までのdブロック元素と異なる。例えば、7d109s0の164番元素は、4d105s0のパラジウムと類似しているとFrickeらに指摘されており、157番元素から172番元素までは、第3族から第18族までと化学的に類似していると考えられている(ただし、165と166番元素がそれぞれ第1族と第2族の元素に近いのか、それとも第11族と第12族の元素に近いのかについては意見が分かれている)。そのため、彼らの表において157番元素から164番元素までは、著者らが化学的に最も類似していると予想したものとは異なる族に分類されている[17]。
| Period | s1 | s2 | |||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 1 | 1 H |
2 He |
p1 | p2 | p3 | p4 | p5 | p6 | |||||||||||||||||||||||||||||||||||||||||||||
| 2 | 3 Li |
4 Be |
5 B |
6 C |
7 N |
8 O |
9 F |
10 Ne | |||||||||||||||||||||||||||||||||||||||||||||
| 3 | 11 Na |
12 Mg |
d1 | d2 | d3 | d4 | d5 | d6 | d7 | d8 | d9 | d10 | 13 Al |
14 Si |
15 P |
16 S |
17 Cl |
18 Ar | |||||||||||||||||||||||||||||||||||
| 4 | 19 K |
20 Ca |
21 Sc |
22 Ti |
23 V |
24 Cr |
25 Mn |
26 Fe |
27 Co |
28 Ni |
29 Cu |
30 Zn |
31 Ga |
32 Ge |
33 As |
34 Se |
35 Br |
36 Kr | |||||||||||||||||||||||||||||||||||
| 5 | 37 Rb |
38 Sr |
f1 | f2 | f3 | f4 | f5 | f6 | f7 | f8 | f9 | f10 | f11 | f12 | f13 | f14 | 39 Y |
40 Zr |
41 Nb |
42 Mo |
43 Tc |
44 Ru |
45 Rh |
46 Pd |
47 Ag |
48 Cd |
49 In |
50 Sn |
51 Sb |
52 Te |
53 I |
54 Xe | |||||||||||||||||||||
| 6 | 55 Cs |
56 Ba |
57 La |
58 Ce |
59 Pr |
60 Nd |
61 Pm |
62 Sm |
63 Eu |
64 Gd |
65 Tb |
66 Dy |
67 Ho |
68 Er |
69 Tm |
70 Yb |
71 Lu |
72 Hf |
73 Ta |
74 W |
75 Re |
76 Os |
77 Ir |
78 Pt |
79 Au |
80 Hg |
81 Tl |
82 Pb |
83 Bi |
84 Po |
85 At |
86 Rn | |||||||||||||||||||||
| 7 | 87 Fr |
88 Ra |
g1 | g2 | g3 | g4 | g5 | g6 | g7 | g8 | g9 | g10 | g11 | g12 | g13 | g14 | g15 | g16 | g17 | g18 | p1 | p2 | 89 Ac |
90 Th |
91 Pa |
92 U |
93 Np |
94 Pu |
95 Am |
96 Cm |
97 Bk |
98 Cf |
99 Es |
100 Fm |
101 Md |
102 No |
103 Lr |
104 Rf |
105 Db |
106 Sg |
107 Bh |
108 Hs |
109 Mt |
110 Ds |
111 Rg |
112 Cn |
113 Nh |
114 Fl |
115 Mc |
116 Lv |
117 Ts |
118 Og | |
| 8 | 119 Uue |
120 Ubn |
121 Ubu |
122 Ubb |
123 Ubt |
124 Ubq |
125 Ubp |
126 Ubh |
127 Ubs |
128 Ubo |
129 Ube |
130 Utn |
131 Utu |
132 Utb |
133 Utt |
134 Utq |
135 Utp |
136 Uth |
137 Uts |
138 Uto |
139 Ute |
140 Uqn |
141 Uqu |
142 Uqb |
143 Uqt |
144 Uqq |
145 Uqp |
146 Uqh |
147 Uqs |
148 Uqo |
149 Uqe |
150 Upn |
151 Upu |
152 Upb |
153 Upt |
154 Upq |
155 Upp |
156 Uph |
157 Ups |
158 Upo |
159 Upe |
160 Uhn |
161 Uhu |
162 Uhb |
163 Uht |
164 Uhq| | |||||||
| 9 | 165 Uhp |
166 Uhh |
167 Uhs |
168 Uho |
169 Uhe |
170 Usn |
171 Usu |
172 Usb |
|||||||||||||||||||||||||||||||||||||||||||||
| Sブロック元素 | Pブロック元素 | Dブロック元素 | Fブロック元素 | Gブロック元素 |
ピューッコの拡張周期表
[編集]2010年にペッカ・ピューッコが提唱した周期表である[18]。相対論効果を考慮した理論計算によって電子軌道の準位を8s<5g≤8p1/2<6f<7d<9s<9p1/2<8p3/2であるとし、これに基づいて172番元素(ウンセプトビウム)までの元素を配置している。一部で原子番号と配置が前後する。また、2011年に発表された論文で、コンピューターモデルを使用してZ = 172までの元素の配置と、予想される化学的性質を計算した[13]。彼はFrickeらの軌道構成を再現し、イオン構成に基づいて121番元素から164番元素までを正式に周期表へ割り当てることで、彼らの周期表への改良を提案した。139と140番元素は、8p1/2電子殻が埋まることを反映して13族と14族に配置され、5g、8p1/2、および6f系列を区別している[13]。FrickeらとNefedovらは、これらの系列を分割していない[17][19]。
| 1 1s |
1 H |
2 He | ||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 2 2s 2p |
3 Li |
4 Be |
5 B |
6 C |
7 N |
8 O |
9 F |
10 Ne | ||||||||||||||||||||||||||||||||||||||||||
| 3 3s 3p |
11 Na |
12 Mg |
13 Al |
14 Si |
15 P |
16 S |
17 Cl |
18 Ar | ||||||||||||||||||||||||||||||||||||||||||
| 4 4s 3d 4p |
19 K |
20 Ca |
21 Sc |
22 Ti |
23 V |
24 Cr |
25 Mn |
26 Fe |
27 Co |
28 Ni |
29 Cu |
30 Zn |
31 Ga |
32 Ge |
33 As |
34 Se |
35 Br |
36 Kr | ||||||||||||||||||||||||||||||||
| 5 5s 4d 5p |
37 Rb |
38 Sr |
39 Y |
40 Zr |
41 Nb |
42 Mo |
43 Tc |
44 Ru |
45 Rh |
46 Pd |
47 Ag |
48 Cd |
49 In |
50 Sn |
51 Sb |
52 Te |
53 I |
54 Xe | ||||||||||||||||||||||||||||||||
| 6 6s 4f 5d 6p |
55 Cs |
56 Ba |
57 La |
58 Ce |
59 Pr |
60 Nd |
61 Pm |
62 Sm |
63 Eu |
64 Gd |
65 Tb |
66 Dy |
67 Ho |
68 Er |
69 Tm |
70 Yb |
71 Lu |
72 Hf |
73 Ta |
74 W |
75 Re |
76 Os |
77 Ir |
78 Pt |
79 Au |
80 Hg |
81 Tl |
82 Pb |
83 Bi |
84 Po |
85 At |
86 Rn | ||||||||||||||||||
| 7 7s 5f 6d 7p |
87 Fr |
88 Ra |
89 Ac |
90 Th |
91 Pa |
92 U |
93 Np |
94 Pu |
95 Am |
96 Cm |
97 Bk |
98 Cf |
99 Es |
100 Fm |
101 Md |
102 No |
103 Lr |
104 Rf |
105 Db |
106 Sg |
107 Bh |
108 Hs |
109 Mt |
110 Ds |
111 Rg |
112 Cn |
113 Nh |
114 Fl |
115 Mc |
116 Lv |
117 Ts |
118 Og | ||||||||||||||||||
| 8 8s 5g 6f 7d 8p |
119 Uue |
120 Ubn |
121 Ubu |
122 Ubb |
123 Ubt |
124 Ubq |
125 Ubp |
126 Ubh |
127 Ubs |
128 Ubo |
129 Ube |
130 Utn |
131 Utu |
132 Utb |
133 Utt |
134 Utq |
135 Utp |
136 Uth |
137 Uts |
138 Uto |
141 Uqu |
142 Uqb |
143 Uqt |
144 Uqq |
145 Uqp |
146 Uqh |
147 Uqs |
148 Uqo |
149 Uqe |
150 Upn |
151 Upu |
152 Upb |
153 Upt |
154 Upq |
155 Upp |
156 Uph |
157 Ups |
158 Upo |
159 Upe |
160 Uhn |
161 Uhu |
162 Uhb |
163 Uht |
164 Uhq |
139 Ute |
140 Uqn |
169 Uhe |
170 Usn |
171 Usu |
172 Usb |
| 9 9s 9p |
165 Uhp |
166 Uhh |
167 Uhs |
168 Uho | ||||||||||||||||||||||||||||||||||||||||||||||
| 8p1/2(8p*)軌道に電子が満たされるブロック | 8p3/2軌道に電子が満たされるブロック |
より簡易な表示によるピューッコの拡張周期表[18]。

Nefedovの拡張周期表
[編集]Nefedov(ロシア語版)、Trzhaskovskaya、Yarzhemskiiは164番元素までの計算を行い、結果を2006年に発表した。ピューッコやFrickeらとは対照的に、彼らは第5周期遷移金属との電子配置の類似性に注目し、158番元素から164番元素は6族から12族ではなく、4族から10族の同族体であると考えた。RgとCnには、AuとHgとは異なる電子配置を反映するためにアスタリスクが付けられている(論文では、これらは3次元に配置されているように描かれている)。一方で、PtとDsの電子配置の違いは顕著ではないとしている[19]。
| Cs | Ba | La–Lu | Hf | Ta | W | Re | Os | Ir | Pt | Au | Hg | Tl | Pb | Bi | Po | At | Rn |
| Fr | Ra | Ac–Lr | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg* | Cn* | Nh | Fl | Mc | Lv | Ts | Og |
| 119 | 120 | 121–157 | 158 | 159 | 160 | 161 | 162 | 163 | 164 |
Kulshaの拡張周期表
[編集]計算化学者Andrey Kulshaは、ピューッコの計算を参考にして、Nefedovらによる164番元素までの拡張周期表をもとに、172番元素までの改良された2つの形式を提案した[20]。考えられる化学的性質に基づき、元素157から172は、どちらの形式においても、第8周期のイットリウムからキセノンまでの第5周期の同族元素として位置付けられている[20]。これは、Nefedovらによる157から164のイットリウムからパラジウムまでの配置を拡張するものであり[19]、Frickeらによる化学的類似性と一致している[17]。
Kulshaは、従来の元素へ正確に対応するものが存在しない、121番元素から156番元素までを扱う2つの方法を提案した。彼の最初の形式(2011年、ピューッコの論文が発表された後)[20]では、元素121から138までと、139から156までを2つの別々の列(まとめて「Ultransition elements」と呼ばれる)として配置され、5g18電子殻をコアに追加することによって2つの列を関連付けた。ピューッコによる酸化状態の計算では[13]、それぞれランタノイドとアクチノイドに似ると予想される[20][21]。彼の2番目の提案(2016年)では、121番元素から142番元素まではgブロックを形成し(5g活性があるため)、元素143から156はアクチニウムからノーベリウムの下に配置されたfブロックを形成する[22]。したがって、第8周期には54の元素が現れ、118番元素の次の貴ガス(液体または固体と予想[4])は172番元素と考えられる[23]。


Smitsらの拡張周期表
[編集]2023年、Smits、Düllmann、Indelicato、Nazarewicz、Schwerdtfegerは、電子配置に基づいて周期表の119番から170番までの元素を配置する試みを行った。いくつかの元素(121番から124番までと、168番)は、明確に配置できなかった。145番元素は2回出現し、いくつかの場所は二重に占有され、他の場所は空である[24]。
| Cs | Ba | ||||||||||||||||||
| Fr | Ra | ||||||||||||||||||
| 119 | 120 | 125 | 126 | 127 | 128/129 | 130 | 131 | 132 | 133/134 | 135 | 136 | 137 | 138 | 139 | 140 | 141 | 142/143 | 144 | 145 |
| 165 | 166 |
| La | Ce | Pr | Nd | Pm | Sm | Eu | Gd | Tb | Dy | Ho | Er | Tm | Yb | Lu | Hf | Ta | W | Re | Os | Ir | Pt | Au | Hg | Tl | Pb | Bi | Po | At | Rn |
| Ac | Th | Pa | U | Np | Pu | Am | Cm | Bk | Cf | Es | Fm | Md | No | Lr | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og |
| 145 | 146 | 147 | 148/149 | 150 | 151 | 152 | 153 | 154 | 155 | 156 | 157 | 158/159 | 160 | 161 | 162 | 163 | 164 | 167 | |||||||||||
| 169 | 170 |
未発見の元素の探索
[編集]合成の試み
[編集]ウンビセプチウムまでの第8周期元素は、ウンビトリウムを除いて合成が試みられているが、成功していない。
ウンウンエンニウム
[編集]ウンウンエンニウムの合成が初めて試みられたのは、1985年にカリフォルニア州バークレーにあるsuperHILAC加速器で、アインスタイニウム254の標的にカルシウム48イオンを衝突させて行われた。
- 254
99Es + 48
20Ca → 302
119Uue* → no atoms
原子は確認されず,断面積(核反応を起こす割合を表す尺度)の限界は300nbとされた[25]。後の計算では、299Uueと3個の中性子を生成物とする3n反応の断面積は、実際にはこの上限の60万分の1の0.5pbになるとされている[26]。
ウンウンエンニウムは未発見の最軽量元素であり、ドイツとロシアによって合成実験の対象となった。 ロシアの実験は2011年に行われたが、結果は公表されず、ウンウンエンニウム原子が確認されなかったのではないかと考えられている。2012年4月から9月にかけて、ドイツのダルムシュタットにある重イオン研究所(GSI)で、バークリウム249を標的にチタン50を衝突させて295Uueと296Uueの同位体を合成する試みが行われた[27][28]。 理論的に予測される断面積から、実験開始から5ヶ月以内にウンウンエンニウム原子が合成されると予想されていた[29]。さらに、バークリウム 249は327日という短い半減期でカリフォルニウム249(次の元素)に崩壊するため、これにより119番元素と120番元素を同時に探索することが可能であった[30]。
- 249
97Bk + 50
22Ti → 299
119Uue* → 296
119Uue + 3 1
0n - 249
97Bk + 50
22Ti → 299
119Uue* → 295
119Uue + 4 1
0n
当初、実験は2012年11月まで行われる予定であったが[31]、テネシンの合成を確認するために249Bkのターゲットを利用するため(衝突させるイオンをチタン50からカルシウム48に変更)、早期に中止された[32]。 この249Bkと50Tiの反応は、やや非対称であり[29]、やや冷たい合成反応である[32]が、ウンウンエンニウムの生成に最も好ましい実用的な反応であると予測されていた[28](254Esと48Caの反応の方が優れているが、標的用にミリグラム量の254Esを準備するのは難しい[29])。とはいえ、「銀の弾丸」である48Caから50Tiへと変更する必要があり、ウンウンエンニウムの収量は核融合反応の非対称性に強く依存しているため、期待される収量は約20分の1になってしまう[29]。
半減期が短いと予測されたため、GSIのチームはマイクロ秒以内に崩壊イベントを記録できる新しい「高速」機器を使用した[28]。ウンウンエンニウム原子は特定されず、限界断面積は70fbと考えられる[32]。予測される実際の断面積は約40fbであり、これは現在の技術の限界である[29]。
理化学研究所(理研、埼玉県和光市)のチームは、2018年1月にキュリウム248の標的をバナジウム51のビームで照射し、119番元素の探索を開始した[33]。より重いバークリウムやカリホルニウムではなくキュリウムが選ばれたのは、これらのより重い元素は用意が難しいためである[34]。248Cmはオークリッジ国立研究所から提供された。理研は高強度バナジウムビームを開発した[35]。実験はサイクロトロンで始まり、その間に理研は線形加速器をアップグレードし、アップグレードは2020年に完了した[36]。最初の元素合成が観測されるまで、両方の機器で照射を続けることができる。実験は現在、少なくとも年間100日間断続的に実行されている[37][34]。
JINRのチームは将来、おそらく243Am + 54Crの反応を使用して119番元素の合成を試みることを計画しているが、正確な時期は公表されていない[38][39]。
ウンビニリウム
[編集]2006年に、249Cfと48Caの反応でオガネソンを得ることに成功したドゥブナ合同原子核研究所(JINR)のチームは、58Feと244Puの原子核からウンビニリウム(120番元素)を作ることを目指して、2007年3月から4月にかけて同様の実験を開始した[40][41]。ウンビニリウムの同位体は、アルファ崩壊の半減期がマイクロ秒のオーダーであると予想されている[42][43]。初期の分析ではウンビニリウムの原子は生成されず、エネルギーの限界断面積は400fbという結果であった[44]。
- 244
94Pu + 58
26Fe → 302
120Ubn* → no atoms
ロシアのチームは、この反応に再挑戦する前に設備を更新することを計画していた[44]。
2007年4月、ドイツのダルムシュタットにある重イオン研究所(GSI)のチームは、ウラン238とニッケル64を用いてウンビニリウムの生成を試みた[45]。
- 238
92U + 64
28Ni → 302
120Ubn* → no atoms
原子は検出されず、このエネルギーでの断面積は1.6pbであった。GSIは、2007年4月から5月、2008年1月から3月、2008年9月から10月の3回にわたり、より高い感度で実験を繰り返したが、いずれも否定的な結果となり、断面積の限界値は90fbであった[45]。
GSIでは、より多くの放射性ターゲットを使用できるように装置を更新した後、2010年6月から7月、および2011年に、より非対称な核融合反応を試みた[46]。
- 248
96Cm + 54
24Cr → 302
120Ubn* → no atoms
このような反応の収率は、その非対称性に強く依存しているため、反応の変化によってウンビニリウムの合成確率が5倍になることが期待されていた[47]。 その結果、299Ubnとその娘核295Ogの予測されるアルファ崩壊のエネルギーと、そのまた娘核である291Lvの実験的に知られている崩壊エネルギーに一致する3つの相関信号が観測されたが、これらの可能性のある崩壊の寿命が予想よりもずっと長く、結果を確認することはできなかった[48][49][46]。
2011年8月から10月にかけて、GSIの別チームがTASCA施設を使って、さらに非対称な新しい反応を試みた[50][32]。
- 249
98Cf + 50
22Ti → 299
120Ubn* → no atoms
249Cfと50Tiの反応は、その非対称性から[51]、ウンビニリウムの合成に最も適した実用的な反応であると予測されていたが、やや冷たい合成反応でもある。ウンビニリウムの原子は確認されず、限界断面積は200fbであることが示唆された[32]。Jens Volker Kratzは、これらのどの反応によってもウンビニリウムを生成できる実際の最大断面積は0.1fb程度であると予測した[52]。これに対して、成功した反応の最小断面積の世界記録は、209Bi(70Zn,n)278Nhという反応の30fbであり[29]、Kratzは隣のウンウンエンニウムを生成するための最大断面積を20fbと予測した[52]。 これらの予測が正確であれば、ウンウンエンニウムの合成は現在の技術の限界であり、ウンビニリウムの合成には新しい手法が必要になるだろう[52]。
2021年5月、JINRは新しい施設で249Cf+50Tiの反応を調査する計画を発表した[53]。しかし、249Cfの標的は米国のオークリッジ国立研究所によって作成される必要があり、2022年2月にロシアのウクライナ侵攻が始まった後は、制裁のためJINRと他の研究所との協力は完全に停止した[54]。その結果、JINRは現在、代わりに248Cm+54Crの反応を試みることを計画している。 54Cr発射体を使用するための準備実験が2023年末に実施され、238U+54Cr反応で288Lvの合成に成功した[55]。120番元素を合成する実験が2025年に開始されることが期待されている[56]。
2022年から[35]、米国カリフォルニア州バークレーにあるローレンス・バークレー国立研究所(LBNL)で、88インチのサイクロトロンを使用し、50Ti発射体を使用して新しい元素を合成する試みも行われている。計画では、2023年末にまずプルトニウムを用いてリバモリウム(116番元素)を生成する実験を行うことになっている。それが成功すれば、249Cf+50Ti反応で120番元素を生成する試みが、早ければ2024年に開始されることになる[57][58]。
ウンビウニウム
[編集]ウンビウニウムの合成は、1977年にドイツのダルムシュタットにある重イオン研究所(GSI)で、ウラン238を標的にして銅65イオンを照射することで初めて試みられた。
- 238
92U + 65
29Cu → 303
121Ubu* → no atoms
原子は確認されなかった[11]。
ウンビビウム
[編集]ウンビビウムの合成は、1972年にドゥブナ合同原子核研究所(JINR)のゲオルギー・フリョロフらによって、重イオンによる熱核融合反応を利用して初めて試みられた[10]。
- 238
92U + 66,68
30Zn → 304, 306
122Ubb* → no atoms
この実験は、N = 184、Z > 120に安定の島が存在するという初期の予測に基づいて行われた。原子は検出されず、収率限界は5nb(5,000pb)と測定された。現在の結果(フレロビウム参照)では、これらの実験の感度は少なくとも3桁は低かったことが示されている[12]。
2000年には、ドイツの重イオン研究所(GSI)のチームが、より高い感度で類似した実験を行った[10]。
- 238
92U + 70
30Zn → 308
122Ubb* → no atoms
これらの結果は、このような重い元素の合成は依然として大きな課題であり、ビーム強度と実験効率のさらなる向上が必要であることを示している。より質の高い結果を得るためには、将来的には感度を1fbまで上げる必要がある。
ウンビビウムの合成は、1978年にもGSIで行われ、天然のエルビウムを標的にキセノン136イオンを照射したが原子は確認されなかった[10]。
- nat
68Er + 136
54Xe → 298, 300, 302, 303, 304, 306
122Ubb* → no atoms
特に、170Erと136Xeの反応では、半減期がマイクロ秒のアルファ線が発生し、半減期が数時間にも及ぶフレロビウムの同位体に崩壊すると予想されていた。フレロビウムは安定の島の中心近くにあると予測されていたためである。しかし12時間照射しても、この反応は起こらなかった。同じように238Uと65Cuからウンビビウムを合成しようとしたが成功しなかった。超重核の半減期は1マイクロ秒以下であるか、あるいは断面積が非常に小さいと結論づけられた[59]。 超重元素の合成に関する最近の研究では、この2つの結論が正しいことが示唆されている[29][60]。ウンビビウムを合成する1970年代の2つの試みは両方とも、超重元素が潜在的に自然に存在する可能性があるかどうかを調査する研究によって推進された[10]。
306Ubbのような様々な超重核化合物核の核分裂特性を調べるいくつかの実験が、2000年から2004年にかけて、ロシアのドゥブナ合同原子核研究所(JINR)で行われた。2つの核反応、すなわち248Cm + 58Feと242Pu + 64Niについて実施された[10]。その結果、超重核は主に132Sn(Z = 50、N = 82)のような閉殻核を排出して核分裂することが明らかになった。また、48Caと58Feの発射体では、核融合-核分裂経路の収率が同程度であることが判明し、将来的に58Feの発射体を超重元素生成に利用できる可能性が示唆された[61]。
ウンビクアジウム
[編集]フランスのカーンにあるGANIL(Grand Accélérateur National d'Ions Lourds、国立重イオン大型加速器)の科学者たちは、この領域での殻模型効果を探り、次の球状陽子殻を突き止めるために、Z = 114、120、124の元素の複合核の直接核分裂と遅延核分裂を測定しようとした。これは、原子核の殻が完全であれば(あるいは陽子や中性子が魔法数であれば)、超重元素の原子核の安定性が高まり、安定の島に近づくことになるからである。2006年には、天然のゲルマニウムにウランイオンを衝突させた反応の結果が発表され、2008年には完全な結果が発表された。
- 238
92U + nat
32Ge → 308, 310, 311, 312, 314
124Ubq* → fission
研究チームは、半減期が10-18秒以上の複合核の核分裂を確認できたことを報告した。この結果は、Z = 124で強い安定化効果があることを示唆しており、次の陽子殻が、従来考えられていたZ = 114ではなく、Z > 120であることを示している。複合核とは、まだ核の殻に収まっていない核子のゆるやかな組み合わせである。内部構造を持たず、標的核と発射核の衝突力のみで結合している。核子が核の殻に収まるまでには約10-14秒かかると言われており、その時点で複合核は核子となる。IUPACではこの数字を、発見された同位体と認められるために必要な最小半減期としている。そのため、GANILの実験は124番元素の発見にはならない[10]。
複合核312124の核分裂は,2006年にイタリアのレニャーロ国立研究所(Laboratori Nazionali di Legnaro)にあるタンデムALPI重イオン加速器でも研究されている[62]。
- 232
90Th + 80
34Se → 312
124Ubq* → fission
ドゥブナ合同原子核研究所(JINR)で行われた過去の実験と同様に、核分裂片は132Sn(Z = 50、N = 82)のような二重魔法数の周りに集まっており、超重核が核分裂でこのような二重魔法数の核子を排出する傾向があることが明らかになった[61]。また、312124複合核からの核分裂1回あたりの平均中性子数も(軽い系に比べて)増加しており、重い核が核分裂でより多くの中性子を放出する傾向が超重質量領域まで続いていることが確認された[62]。
ウンビペンチウム
[編集]1970年から1971年にかけて、ドゥブナ合同原子核研究所で亜鉛イオンとアメリシウム243の標的を用いて、最初で唯一のウンビペンチウムの合成が行われた[12]。
- 243
95Am + 66, 68
30Zn → 309, 311
125Ubp* → no atoms
原子は検出されず,断面積の限界は5nbと決定された。この実験は、Z ~ 126やN ~ 184付近の原子核がより安定である可能性に基づいて行われたが[12]、最近の研究では,安定の島はむしろより低い原子番号(コペルニシウム、Z = 112など)にあるのではないかと考えられており、ウンビペンチウムのような重い元素の合成には、より感度の高い実験が必要であるとされている[29]。
ウンビヘキシウム
[編集]1971年にCERN(欧州合同素粒子原子核研究機構)でRené BimbotとJohn M. Alexanderが熱核融合反応を用いてウンビヘキシウムの合成を試みたが、成功しなかった[10]。
- 232
90Th + 84
36Kr → 316
126Ubh* → no atoms
高エネルギー(13から15MeV)のアルファ粒子が観測され、ウンビヘキシウムの合成の証拠となる可能性があるとされた。その後、より高い感度での実験に失敗したことから、この実験の10mbの感度は低すぎたと考えられ、この反応でウンビヘキシウムの原子核が生成される可能性は極めて低いと考えられている[8]。
ウンビセプチウム
[編集]1978年、重イオン研究所(GSI)のUNILAC加速器で、天然タンタルを標的にキセノン136イオンを照射し、ウンビセプチウムを合成する最初で唯一の試みが行われたが、成功しなかった[10]。
- nat
73Ta + 136
54Xe → 316, 317
127Ubs* → no atoms
自然界での探索
[編集]1976年、アメリカの複数の大学の研究者グループが、鉱物による原因不明の放射線障害(特に放射性ハロー(en:Pleochroic halo))の原因として、原生的な超重元素、主にリバモリウム、ウンビクアジウム、ウンビヘキシウム、ウンビセプチウムがあると提唱した[8]。 これを受けて、1976年から1983年にかけて、多くの研究者が自然界での探索を行った。1976年、カリフォルニア大学デービス校のTom Cahill教授のグループは、観察された障害を引き起こすのに該当するエネルギーのアルファ粒子とX線を検出したと主張し、これらの元素の存在を裏付けた。特に、長寿命(109年オーダー)のウンビクアジウムとウンビヘキシウムの原子核および、その崩壊生成物の存在が推測され、その存在量は同族体のウランやプルトニウムと比較して10−11であるとされた[63]。 他の人々は、何も検出されなかったと主張し、原初の超重原子核の提案された特徴に疑問を呈した[8]。特に彼らは、そのような超重核はN = 184またはN = 228で閉じた中性子殻を持っていなければならず、安定性を高めるために必要なこの条件は、リバモリウムの中性子不足の同位体または、(ほとんどの天然に存在する同位体とは異なり)ベータ安定性[8]を持たない他の元素の中性子過剰同位体にしか存在しないことを挙げていた[64]。 また超重元素は、天然のセリウムの核変換によって引き起こされたとも提案されており、超重元素の観測と主張していたものの、さらに曖昧さを増していた[8]。
2008年4月24日、ヘブライ大学のAmnon Marinovを中心とするグループが、自然界に存在するトリウムの鉱床から、トリウムに対して10−11から10−12の割合でウンビビウム292の単原子を発見したと主張した[65]。Marinovらの主張は、一部の科学者から批判された。Marinovは、ネイチャー誌とネイチャー フィジクス誌に論文を投稿したが、査読に回さずに両誌から断られたと主張していた[66]。ウンビビウム292原子は超変形または過変形された核異性体であり、半減期は少なくとも1億年であると主張していた[10]。
2008年のフィジカル・レビューC誌に、質量分析法でより軽いトリウムの同位体を識別すると称して使われていた[67]、この技術に対する批判が掲載された[68]。掲載されたコメントの後に、Marinovらによる反論がフィジカル・レビューC誌に掲載された[69]。
加速器質量分析(AMS)の優れた方法を使用したトリウムの繰り返し実験では、感度が100倍優れているにもかかわらず、結果を確認できなかった[70]。この結果は、Marinovらが主張するトリウム[67]、レントゲニウム[71]、ウンビビウム[65]の長寿命同位体に関する結果に大きな疑問を投げかけるものであった。ウンビビウムの痕跡が一部のトリウム試料にのみ存在する可能性はあるが、見込みは薄い[10]。
現在の地球上に原生超重元素がどの程度存在しうるかは不確かである。それらがずっと前に放射線損傷を引き起こしたことが確認されたとしても、それらは今では単なる痕跡に崩壊したか、あるいは完全になくなったかもしれない[72]。そのような超重元素の原子核が自然に生成されるかどうかも不確かである。というのも、自発核分裂によって、質量数270から290の間で重元素生成の原因となるr過程を終了させると予想されており、ウンビニリウムよりも重い元素が生成されるずっと前に終了するからである[73]。
最近の仮説では、プシビルスキ星のスペクトルを用いて、フレロビウム、ウンビニリウム、ウンビヘキシウムの天然での存在を説明しようとしている[74][75][76]。
第8周期元素の予想される性質
[編集]118番元素のオガネソンは、これまでに合成された元素の中で最も重い元素である。次の2つの元素、119番元素と120番元素はそれぞれアルカリ金属とアルカリ土類金属の8s元素になると思われる。120番元素を超えると超アクチノイド系列が始まると予想されており、8s電子と8p1/2、7d3/2、6f、5gの各電子殻の充填によって、これらの元素の化学的性質が決定される。122番より大きい元素については状態が非常に複雑であるため、完全で正確なCCSD計算はできない。5g、6fおよび7d軌道はほぼ同じエネルギー準位を持ち、160番元素の領域では、9s、8p3/2、9p1/2の各軌道もほぼ同じエネルギーになると考えられる。これにより電子殻が混ざり合い、ブロックの概念がうまく適用されなくなる。また、一部の元素を周期表に配置するのが非常に困難になる新しい化学的性質が生じると予想される[15]。

化学的および物理的性質
[編集]119番元素および120番元素
[編集]第8周期における最初の2つの元素は、119番元素のウンウンエンニウムと120番元素のウンビニリウムである。これらの元素の電子配置は、8s軌道が満たされると思われる。この軌道は相対論的に安定し収縮しているので、119番元素と120番元素は、周期表直上のフランシウムやラジウムよりも、ルビジウムやストロンチウムに似ていると考えられる。8s軌道の相対論的収縮によるもう一つの効果は、これら2つの元素の原子半径が、フランシウムやラジウムの原子半径とほぼ同じになることである。これらの元素は、通常のアルカリ金属やアルカリ土類金属のように振る舞い(周期表直上の元素よりも反応性は低い)、通常はそれぞれ+1と+2の酸化数を取るが、7p3/2電子殻の相対論的な不安定さと7p3/2電子の比較的低いイオン化エネルギーにより、それぞれ+3や+4のような高い酸化数も可能になると考えられる[4][15]。
超アクチノイド元素
[編集]ロシアの化学者Nefedov(ロシア語版)らによると、超アクチノイド元素は121番元素から157番元素までと考えられており、第8周期の5g、6f元素と一部の7d元素に分類される[19]。超アクチノイド系列では、7d3/2、8p1/2、6f5/2、5g7/2の各電子殻が同時に満たされると予想される[16]。これは非常に複雑な状態となるため、完全で正確なCCSD計算は121番元素と122番元素に対してのみ適用される[15]。最初の超アクチノイド元素であるウンビウニウム(121番元素)は、ランタンやアクチニウムと似ていると考えられる[77]。主な酸化状態は+3であるが、価電子殻のエネルギー準位が近いため、119番元素や120番元素のように、より高い酸化数を取る可能性がある[15]。8p電子殻が相対論的に安定しているので、121番元素の基底状態における価電子配置は8s28p1となり、ランタンやアクチニウムのds2配置とは対照的である[15]。しかし、この異常な配置は計算上の化学的性質に影響を与えないようで、性質はアクチニウムと似ていると考えられる[78]。第一イオン化エネルギーは429.4 kJ/molと予想され、アルカリ金属のカリウム、ルビジウム、セシウム、フランシウムを除くすべての既知の元素よりも低く、この値は第8周期のアルカリ金属であるウンウンエンニウム(463.1 kJ/mol)よりもさらに低い。同様に、次の超アクチノイド元素であるウンビビウム(122番元素)は、セリウムやトリウムと似ており、主な酸化数は+4と予想される。基底状態では7d18s28p1か8s28p2の価電子配置を持ち[79]、トリウムの6d27s2配置とは異なると考えられる。したがって、第一イオン化エネルギーはトリウムよりも小さくなる(Th: 6.3 eV; Ubb: 5.6 eV)。これは、ウンビビウムの8p1/2電子がトリウムの6d電子よりもイオン化しやすいことによる[15]。5g軌道の軌道崩壊(原子番号が大きくなる際、他の電子軌道よりもエネルギー準位が小さくなること)は125番元素あたりまで遅れる。電子数が119のときの等電子的な電子配置は、119番元素から122番元素では[Og]8s1、123番元素と124番元素では[Og]6f1、125番元素以降では[Og]5g1になると予想されている[80]。
原子番号の小さい超アクチノイド元素では電子の結合エネルギーが十分に小さく、すべての価電子を電離することができると予測されている。例えば、ウンビヘキシウム(126番元素)は、容易に+8の酸化数を取ることができ、次のいくつかの元素ではさらに高い酸化数が可能であると考えられる。ウンビヘキシウムは、他のさまざまな酸化数を示すことも予測されている。最近の計算では、ウンビヘキシウムの5g軌道とフッ素の2p軌道の間の結合相互作用によって、安定な一フッ化物UbhFができる可能性が示唆されている[81]。 その他の予測される酸化数には+2、+4、+6などがあり、+4はウンビヘキシウムにおける最も普通の酸化数であると予想されている[16]。ウンビセプチウム(125番元素)からウンビエンニウム(129番元素)までの超アクチノイド元素は+6の酸化数を示し六フッ化物を形成すると予測されているが、UbpF6とUbhF6は比較的弱い結合になると予測されている[80]。 結合解離エネルギーは127番元素で大きく増加し、129番元素ではさらに増加すると予測されている。このことは、125番元素フッ化物の強いイオン性から、129番元素フッ化物における8p軌道を含んだ共有結合性への移行を示唆している。これら超アクチノイド元素六フッ化物における結合のほとんどは、六フッ化ウランのようにウランが5fと6dの軌道を使って結合するのではなく、超アクチノイド元素で最もエネルギー準位の高い8p電子殻とフッ素の2p電子殻の間で行われる[80]。
初期の超アクチノイド元素は高い酸化数に達することができるにもかかわらず、5g電子は最もイオン化しにくいと計算されている、Ubp6+とUbh7+イオンは5g1配置になると予想されており、これはNp6+イオンの5f1配置に似ている[13][80]。 似たような挙動は化学的活性の低いランタノイドの4f電子でも見られるが、これは5g軌道が小さく、電子雲に深く埋もれていることに起因する[13]。 現在知られている元素の基底状態の電子配置には存在しないg軌道の電子が存在することで、未知の混成軌道が形成され、超アクチノイド元素の化学的性質に新たな影響を与えると考えられる。だが既知の元素にg軌道電子が存在しないため、超アクチノイド元素の化学的性質を予測することは困難である[4]。
超アクチノイド元素の予想される化合物(Xはハロゲン)[13][80][82] 121 122 123 124 125 126 127 128 129 132 142 143 144 145 146 148 153 154 155 156 157 化合物 UbuX3 UbbX4 UbtX5 UbqX6 UbpF
UbpF6
UbpO2+
2UbhF
UbhF6
UbhO4UbsF6 UboF6 UbeF
UbeF6UqbX4
UqbX6UqtF6 UqqX6
UqqO2+
2
UqqF8
UqqO4UqpF6 UqoO6 類似化合物 LaX3
AcX3CeX4
ThX4NpO2+
2ThF4 UF6
UO2+
2
PuF8
PuO4UO6 酸化数 3 4 5 6 1, 6, 7 1, 2, 4, 6, 8 6 6 1, 6 6 4, 6 6, 8 3, 4, 5, 6, 8 6 8 12 3 0, 2 3, 5 2 3
超アクチノイド元素の後半では、酸化数が低くなると予想される。132番元素では、最も安定した酸化数は+6のみが主となり、144番元素ではさらに+3と+4へ減少し、超アクチノイド系列の最後では+2(場合によっては0)となると考えられる。これは、その時点で充填される6f電子殻が電子雲の奥深くにあり、8sおよび8p1/2電子が強く結合しているため、化学的に活性とならないためである。5g電子殻が満たされるのは144番元素、6f電子殻が満たされるのは154番元素あたりと予想されるが、この領域の超アクチノイド元素では、8p1/2電子が強く結合して化学的に活性ではなくなり、化学反応に関与できるのは数個の電子だけになる。Frickeらの計算によると、154番元素で6f電子軌道が満たされ、化学的に不活性な8s殻と8p1/2殻の外側には、d軌道または他の電子の波動関数がないと予測されている。これにより、154番元素は貴ガスのような性質を持ち、むしろ不活性である可能性がある[4][15]。それにもかかわらず、ピューッコの計算では、155番元素は6f電子がイオン化可能であると予想している。Upp3+は6f電子殻が満たされ、第4イオン化ポテンシャルは、+4価のテルビウムとジスプロシウムの間になると考えられる[13]。
ランタノイドやアクチノイドの収縮と同様に、超アクチノイド元素のイオン半径が予想よりも小さい超アクチノイド系列では、超アクチノイドの収縮が起こると思われる。ランタノイドおよびアクチノイドの波動関数は5f軌道に比べ4f軌道でより局在化しているため、アクチノイドよりもランタノイドの方が収縮率が大きい。ランタノイド、アクチノイド、超アクチノイドで外殻電子の波動関数を比較すると、超アクチノイドでは1元素あたり約2pmの収縮が予想される。これはランタノイドとアクチノイドの収縮よりも小さいが、ランタノイドとアクチノイドではそれぞれ4f軌道と5f軌道に14個の電子が満たされるのに対し、超アクチノイドでは深く埋もれている5g軌道と6f軌道に32個の電子が満たされるため、全体の効果は大きくなる[4]。
ペッカ・ピューッコは、超アクチノイドを3つに分類した。5g系列(121番元素から138番元素まで)、8p1/2系列(139番元素から140番元素まで)、6f系列(141番元素から155番元素まで)。これらはエネルギー準位間の重複が多く、初期の超アクチノイド原子やイオンでは6f、7d、8p1/2軌道も占有されている可能性がある。また彼は、これらが「超ランタノイド」に近い挙動を示すと予想している。5g電子はほとんど化学的に不活性であることと、各ランタノイドの1つか2つの4f電子だけが化合物でイオン化されるのに似ているという意味である。彼はまた、超アクチノイド元素の取りうる酸化数は6f系列で非常に高くなり、148番元素では+12のような値になるかもしれないと予想した[13]。
Andrey Kulshaは、121番から156番までの36個の元素を「Ultransition elements」と呼び、121番から138番までと139番から156番まで、18個ずつ2系列の元素に分けて考えることを提案した。1つ目はランタノイドに類似した元素群で、酸化数は主に+4から+6の範囲、5g電子殻の充填が支配的であり、ウラン、ネプツニウム、プルトニウムのように隣り合う元素は互いに非常によく似ていると考えた。最初(140番台の元素あたり)は、6f電子殻が7d電子殻より優先されるため非常に高い酸化数が予想されるが、その後典型的な酸化数は下がり、150番台以降の元素では8p1/2電子によって化学的に活性ではなくなる。この18元素2系列は5g18電子殻によって分離されているため、互いに類似体であると考えることができる[20][21]。
後半の超アクチノイド元素の例として、156番元素は主に+2の酸化数を示すと予想されるが、これは安定した[Og]5g186f148s28p2
1/2電子配置の上に電離しやすい7d2電子があるためである。これはノーベリウムのより重い同族体と考えることができ、安定した[Rn]5f14電子配置の上に電離しやすい7s2電子のペアを持つため、通常は+2価であるのと同様である(+3価のノーベリウムを得るためには強力な酸化剤が必要である)[20]。 その第一イオン化エネルギーは約400kJ/mol、金属半径は約170ピコメートルと予想される。原子量は445u前後[4]で、密度は約26g/cm3と非常に重い金属であると推定される。
157 - 166番元素
[編集]第8周期の7d遷移金属は157番元素から166番元素までと予想されている。これらの元素では8sと8p1/2電子が非常に強く結合しているため、いかなる化学反応にも関与しないと考えられるが、9sと9p1/2軌道は容易に混成すると予想される[4][15]。 これらの7d元素は、4d元素のイットリウムからカドミウムに似ていると思われる[20]。 特に、7d109s0電子配置を持つ164番元素は、4d105s0電子配置を持つパラジウムと明確な類似性がある[16]。
第8周期遷移元素の貴金属は、より軽い同族元素ほどの貴金属性を示さないと考えられている。遮蔽のための外側のs殻がないことと、相対論的効果により7d電子殻が2つの副殻に強く分かれるためである。このため、7d遷移金属の第一イオン化エネルギーは、より軽い同族元素の第一イオン化エネルギーよりも小さくなっている[4][15][16]。
ウンヘキサクアジウムの化学への関心は、理論的な予測に大きく向けられている。特に、472Uhqと482Uhqの同位体(陽子が164個、中性子が308個または318個)が、仮想的な第2の安定の島の中心になるという予測がされている点である(第1の島はコペルニシウム、特に半減期が数百年または数千年と予想される同位体291Cn、293Cn、296Cnが中心である)[83][52][84][85]。
計算上、164番元素(ウンヘキサクアジウム)の7d電子は化学反応に対して非常に関与しやすいと予測されるため、ウンヘキサクアジウムは通常の+2価に加えて、強い配位子を持つ水溶液中で安定した+6および+4の酸化数を示すと予想される。このため、ウンヘキサクアジウムは、Uhq(CO)4、Uhq(PF3)4(いずれも対応するパラジウム化合物と同様に四面体)、Uhq(CN)2−
2(直線形分子構造)のような化合物を形成することができると考えられ、これは鉛の挙動とは非常に異なる。もし相対論的な影響がなければ、ウンヘキサクアジウムはより重い鉛の同族体となっていたであろう。とはいえ、水溶液中では2価の状態が主であり(ただし、より強い配位子を用いれば、+4や+6の状態も可能である)、ウンヘキサクアジウム(II)はウンヘキサクアジウム(IV)やウンヘキサクアジウム(VI)よりも鉛に近い挙動を示すと考えられる[15][16]。
ウンヘキサクアジウムはやわらかいルイス酸であり、Ahrlands硬度は4eVに近いと予測される。ウンヘキサクアジウムは中程度の反応性であり、第一イオン化エネルギーはモリブデンに近く、約685kJ/molと予想される[4][16]。ランタノイド、アクチノイド、超アクチノイドの収縮により、ウンヘキサクアジウムの金属半径はわずか158pmであり、はるかに軽い元素のマグネシウムと非常に近い(ウンヘキサクアジウムの予想原子量は約474uであり、マグネシウム原子量の約19.5倍であるにもかかわらず、である)[4]。 この半径の小ささと重量の大きさから、密度は約46g·cm−3と非常に高く、現在知られている元素の中で最も密度の高いオスミウムの22.61g·cm−3の2倍以上になると予想されている。ウンヘキサクアジウムは、周期表の172元素の中で2番目に密度の高い元素であると考えられ、これより密度が高いのは隣のウンヘキサトリウム(163番元素)の47g·cm−3のみと予想されている[4]。 金属状態のウンヘキサクアジウムは、共有結合による凝集エネルギー(結晶化エンタルピー)が非常に大きく、その結果、融点が高くなると考えられる。金属状態のウンヘキサクアジウムは、パラジウムや白金に似た貴金属であると予想されている。Frickeらは、閉殻構造を持ちイオン化エネルギーが似ているオガネソンとの類似性を示唆しているが、オガネソンが反応しやすい貴ガスであるのに対し、ウンヘキサクアジウムは反応しにくい貴金属であると述べている[16]。
最後の2つの7d金属である元素165(ウンヘキサペンチウム)と166(ウンヘキサヘキシウム)は、それぞれ+1と+2の酸化数を取り、アルカリ金属とアルカリ土類金属と同様の挙動を示すと予想される。相対論的な効果により、9s電子は非相対論的な計算で予測されるよりもはるかに強く結合するため、9s電子のイオン化エネルギーはナトリウムやマグネシウムの3s電子のイオン化エネルギーに匹敵すると考えられる。165番元素と166番元素は通常それぞれ+1と+2の酸化数を示すと思われるが、7d電子のイオン化エネルギーが十分に低いため、元素165は+3価のような高い酸化数も可能である。166番元素の酸化数+4は起こりにくく、11族と12族のより軽い元素(特に金と水銀)と似た状態を作ると思われる[4][15]。166番元素はコペルニシウムではなく水銀のようにUhh2+にイオン化し、d電子ではなくs電子を失って7d10配置になり、12族元素の亜鉛、カドミウム、水銀のような遷移金属の性質を持たない「相対性の低い」状態になると予想される[13] 。
156 - 166番元素の予測される性質
金属の半径と密度は概算である[4][13][15]。
最も類似した元素族を最初に表記し、次いで他の類似した元素族を示した[16]。156 157 158 159 160 161 162 163 164 165 166 原子量 [445] [448] [452] [456] [459] [463] [466] [470] [474] [477] [481] 族 Yb
(4)3
(5)4
(6)5
(7)6
(8)7
(9)8
(10)9
(11)10
(12, 14, 18)11
(1, 13)12
(2, 14)価電子配置 7d2 7d3 7d4 7d5 7d6 7d7 7d8 7d9 7d10 7d10 9s1 7d10 9s2 安定した酸化数 2 3 4 1, 5 2, 6 3, 7 4, 8 5 0, 2, 4, 6 1, 3 2 第一イオン化エネルギー 400 kJ/mol 450 kJ/mol 520 kJ/mol 340 kJ/mol 420 kJ/mol 470 kJ/mol 560 kJ/mol 620 kJ/mol 690 kJ/mol 520 kJ/mol 630 kJ/mol 金属結合半径 170 pm 163 pm 157 pm 152 pm 148 pm 148 pm 149 pm 152 pm 158 pm 250 pm 200 pm 密度 26 g/cm3 28 g/cm3 30 g/cm3 33 g/cm3 36 g/cm3 40 g/cm3 45 g/cm3 47 g/cm3 46 g/cm3 7 g/cm3 11 g/cm3
167 - 172番元素
[編集]周期表の次の6つの元素は、第8周期での最後の元素群になると予想され[13]、5p元素のインジウムからキセノンに似ていると考えられる[20]。 167番元素から172番元素では、9p1/2電子殻と8p3/2電子殻が満たされると予想される。これらのエネルギー固有値は非常に近いため、非相対論的な2pと3pの電子軌道と同様に、1つの結合したp軌道として振る舞う。したがって不活性電子対効果は起こらず、167番元素から170番元素までの最も一般的な酸化数はそれぞれ+3、+4、+5、+6になると予想される。171番元素(ウンセプトウニウム)は、酸化数を-1から+7まで取りハロゲンに似た性質を示すが、物性は金属に近いと予想される。電子親和力は3.0eVで、ハロゲン化水素に似たHUsuを形成できると考えられる。Usu−イオンはヨウ化物(I−)のようなやわらかい塩基になると予想されている。172番元素(ウンセプトビウム)は、イオン化エネルギーが非常に似ていることから(Xe, 1170.4 kJ/mol; Usb, 1090 kJ/mol)、キセノンと同じような化学的挙動を示す貴ガスになると予想されている。両者の唯一の主な違いは、172番元素はキセノンと異なり原子量がはるかに大きいため、標準状態では液体または固体になると予想されることである[4]。ウンセプトビウムは、より軽い同族体であるキセノンと同様に、フッ化物や酸化物を形成する強いルイス酸であると予想される[16]。165-172番元素が第2周期や第3周期に類似していることから、Frickeらはこれらの元素が周期表の第9周期を形成すると考え、一方で第8周期は貴金属の164番元素で終わると考えた。この第9周期は、第2、第3周期と同様に、遷移金属を持たないと予想されている[16]。しかし、165番と166番元素については類推が不完全である。新しいs電子殻(9s)は始まるが、これはd電子殻の上にあり、化学的には11族および12族により類似している[17]。
167 - 172番元素の予想される性質
金属半径または共有結合半径と密度は概算である[4][15][16]。167 168 169 170 171 172 原子量 [485] [489] [493] [496] [500] [504] 族 13 14 15 16 17 18 価電子配置 9s2 9p1 9s2 9p2 9s2 9p2 8p1 9s2 9p2 8p2 9s2 9p2 8p3 9s2 9p2 8p4 安定した酸化数 3 4 5 6 −1, 3, 7 0, 4, 6, 8 第一イオン化エネルギー 620 kJ/mol 720 kJ/mol 800 kJ/mol 890 kJ/mol 984 kJ/mol 1090 kJ/mol 金属半径または共有結合半径 190 pm 180 pm 175 pm 170 pm 165 pm 220 pm 密度 17 g/cm3 19 g/cm3 18 g/cm3 17 g/cm3 16 g/cm3 9 g/cm3
172番より大きい元素
[編集]原子番号が172を超えると、少なくとも6g、7f、8d、10s、10p1/2、そしておそらく6h11/2の電子殻が満たされる可能性がある。これらの電子は非常に緩く結合しており、非常に高い酸化数に到達できる可能性があるが、イオン価が増えると電子はより強固に結合することになる。したがって、非常に長い超アクチノイドのような遷移系列がおそらく存在するだろう[16]。
173番元素(ウンセプトトリウム)では、一番外側の電子が6g7/2、9p3/2、または 10s電子殻に入る。スピン軌道相互作用によって、これらの電子殻と8p3/2の間に非常に大きなエネルギーギャップが生じるため、この最外殻の電子は非常に緩く結合し、非常に簡単に電離してUst+カチオンを形成すると予想される。その結果、173番元素は化学的にはアルカリ金属のように振る舞い、セシウムよりもはるかに反応性が高いと予想されている(フランシウムと119番元素は相対論的効果のためにセシウムよりも反応性が低い)[86][20]。セシウムの実験的に知られているイオン化エネルギー3.894eVに対し、173番元素の計算された値は3.070 eVである[87]。174番元素 (ウンセプトクアジウム)では8d電子が追加され、閉殻のUsq2+カチオンを形成する可能性があり、イオン化エネルギーの計算値は3.614 eVである[87]。
元素184(ウンオクタクアジウム)は、当初陽子数184がマジックナンバーになると推測されていたため、初期の予測ではかなり関心を集めていた。電子配置は[Usb] 6g5 7f4 8d3で、少なくとも7fと8dの電子が化学的に活性であると予測されている。この物質の化学的挙動は、ウランやネプツニウムと同様に、+6価より大きく(6g電子の電離に相当)イオン化することはむずかしいと予想される。水溶液中では+4価が最も一般的で、固体化合物では+5価と+6価に到達すると考えられる[4][16][88]。
周期表の終わり
[編集]物理的に可能な元素の数は明らかになっていない。低く見積もった場合、周期表は安定の島の後すぐに終わる可能性があり[14]、それはZ = 126を中心としたものになると予想される。周期表と原子核種の拡張は、陽子および中性子のドリップラインと、アルファ崩壊や自発核分裂に対する安定性によって制限される[89]。Y.Gambhirらの計算では、様々な崩壊経路における核結合エネルギーと安定性を分析し、結合した原子核の存在はZ = 146が限界であることを示唆している[90]。 ワルター・グライナーのように、周期表に終わりがないかもしれないと予測した人もいる[91]。 周期表に終わりがあると予測した人には、Z = 128(John Emsley)やZ = 155(Albert Khazan)がいる[10]。
原子番号137以上の元素
[編集]物理学者の間では、リチャード・P・ファインマンが、Z = 137より大きい原子番号の中性原子は存在しないと示唆したという「民間伝説」がある。これは、相対論的なディラック方程式によって、そのような原子の最内殻電子では基底状態のエネルギーが虚数になることが予測されるためである。この137という数字は、微細構造定数の逆数である。この論法では、中性原子はウントリセプチウムまでしか存在しないことになり、電子軌道に基づいた元素周期表はこの時点で破綻する。しかし、この議論は、原子核が点状であることを前提としている。より正確に計算するためには、原子核の大きさが小さいがゼロではないことを考慮しなければならず、その結果、限界はさらにZ ≈ 173まで上がると予測されている[91]。
ボーアの原子模型
[編集]ボーアの原子模型は、原子番号が137より大きい原子が成立することの難しさを示す。1s電子軌道上の電子の速度vは次式で与えられる。
ここで、Zは原子番号、αは電磁的相互作用の強さを表す微細構造定数である[92]。この近似式では、原子番号が137より大きい元素は、1s電子が光速であるcより速く移動する必要がある。したがって、非相対論的なボーアの原子模型をこのような元素に適用することは不正確である。
相対論的ディラック方程式
[編集]
相対論的なディラック方程式により、基底状態のエネルギーは次のように与えられる。
ここで、mは電子の静止質量である[93]。Z > 137の場合、ディラック基底状態の波動関数は束縛ではなく振動的であり、クラインのパラドックスのように正負のエネルギースペクトルの間にギャップはない[94]。 原子核の有限サイズの影響を考慮したより正確な計算では、結合エネルギーがZ > Zcrに対して初めて2mc2を超えるのは、168から172の間であることが示されている[95]。Z > Zcrの場合、最も内側の軌道(1s)が満たされていないと、原子核の電場によって電子が真空から引き出され、陽電子が自然放出される[96][97]。 この1s電子殻における負の連続体への飛び込みは、しばしば周期表の「終わり」を意味すると考えられてきたが[13][91][98]、そのような共鳴はガモフ状態として解釈できる。しかしながら、計算と周期表をZcr≈172を超えて拡張するために必要な、多電子系におけるこのような状態の正確な記述は、まだ未解決の問題である[95]。
Zcr ≈ 173以上の原子番号を持つ原子は、「超臨界原子」と呼ばれている。超臨界原子は、電子と陽電子のペアが負の連続体から生成されるため、完全にイオン化することはできない。電子が束縛され、陽電子が脱出する自発的なペア生成によって1s電子殻が満たされるためである。しかし、原子核の周りの強磁場は非常に狭い空間に限られているため、負の連続体に飛び込んだ電子殻が埋まると、それ以上の自発的な対生成はパウリの排他原理によって禁じられてしまう。173番元素から184番元素は、1s電子殻のみが負の連続体に飛び込んでいるため、「弱超臨界原子」と呼ばれている。185番元素では2p1/2電子殻が、245番元素では2s電子殻が結合すると予想されている。重い原子核を衝突させて超臨界電荷を作り出し、自発的なペアの生成を検出する実験は今のところ成功していない(例えば、鉛とウランを衝突させると瞬間的に実効Zが174になり、ウランとウランでは実効Z = 184、ウランとカリホルニウムでは実効Z = 190となる)。超臨界原子は電子構造に問題がないと予想されるので、周期表の最後は電子殻の不安定性ではなく核の不安定性で決まるのかもしれない[99]。
Zcrを過ぎても元素が存在できなくなるわけではないが、Zcrに近づくにつれて原子核近くの 1s密度の濃度が増加するため、これらの電子はK殻電子捕獲に対してより脆弱になる可能性がある。このような重い元素の場合、これらの1s電子は、かなりの時間を原子核の近くで過ごす可能性が高く、実際には原子核の内部に存在する。これは周期表に新たな限界をもたらす可能性がある[100]。
ミュオニック原子は電子の約207倍の重さであるため、係数mによって、はるかに大きい原子番号約2200で超臨界状態となる[95]。
クォーク物質
[編集]また、A > 300を超える領域には、陽子や中性子に束縛されたクォークではなく、アップクォークやダウンクォークが自由に流れる、安定したクォーク物質の仮想的な相からなる「安定の大陸」が存在するのではないかと考えられている。このような物質は、バリオンあたりの結合エネルギーが陽子や中性子よりも大きいバリオン物質の基底状態であり、この質量閾値を超えると陽子や中性子が崩壊してクォーク物質になると考えられている。もしこの状態の物質が存在するならば,通常の超重核に生成するのと同じ核融合反応で合成される可能性があり、クーロン斥力を克服するのに十分なほど強い結合の結果として、核分裂に対して安定となるだろう[101]。
2020年に発表された計算[102]では、アップダウンクォークマター(udQM)ナゲットはA ~ 266を超えても従来の原子核に対して安定であることが示唆されており、また、udQMナゲットは従来の原子核(Zcr ~ 177、A ~ 480)よりも早く(Zcr ~ 163、A ~ 609)超臨界になることが示されている。
原子核の性質
[編集]魔法数と安定の島
[編集]原子核の安定性は、96番元素のキュリウム以降原子番号が大きくなるにつれて急速に短くなるため、101番より大きい原子番号を持つ同位体は、半減期が1日以下で放射性崩壊をしてしまう。原子番号が82(鉛)より大きい元素には安定同位体が存在しない[103]。しかし、まだあまりよくわかっていない理由で、原子番号110から114付近では核の安定性がわずかに増し、核物理学では「安定の島」と呼ばれるものが存在する。この概念はカリフォルニア大学バークレー校のグレン・シーボーグ教授が提唱したもので,超重元素が予測よりも長持ちする理由を説明している[104]。
非相対論的なSkyrme相互作用を用いたハートリー=フォック方程式による計算では、Z = 126が陽子の閉殻として提案されている。周期表のこの領域では、中性子の閉殻としてN = 184、N = 196、N = 228が提案されている。したがって、最も関心のある同位体は310Ubh、322Ubh、354Ubhであり、これらは他の同位体よりもかなり長命である可能性がある。魔法数の陽子を持つ126番元素は、この領域の他の元素よりも安定していると予想され、半減期の非常に長い核異性体が存在する可能性がある[72]。 また代わりに、球状の安定の島が306Ubbを中心とする可能性もあり、これは二重魔法数かもしれないと考えられている[52]。おそらく、安定の島はZ=114から126まで、およびN=184付近で発生し、その寿命は数時間から数日程度である。N=184で閉殻になると、自発核分裂の寿命は10-15秒未満と大幅に低下すると予測される。これは原子核が電子雲を獲得して元素として振る舞うには短すぎる。ただし、こうした寿命はモデルに大きく依存しており、予測の範囲は何桁にもわたる[95]。
核変形と相対論的効果を考慮した超重核での単粒子の解析では、Z = 126、138、154、164とN = 228、308、318の新しい魔法数が予想されている[9][83] 。したがって、291Cn、293Cn[29]、298Flを中心とした安定の島に加えて、さらに二重魔法数の354126や472164、482164の周りにも安定の島が存在する可能性がある[84][85]。これらの原子核はベータ崩壊に対し安定で、比較的長い半減期でアルファ崩壊や自発核分裂によって崩壊すると予測されており、それぞれN = 228同中性子体近辺や152-168番元素にさらなる安定性を与えている[105]。一方で同分析によると、354Ubhのようなケースでは、陽子殻の閉じ方が比較的弱いかまたは存在しない可能性がある。こうした原子核は二重魔法数ではないかもしれず、安定性は主に強い中性子殻の閉じ方によって決定されることになる[83]。さらに、第2の島(Z = 164)では電磁的な反発の力が非常に大きく、強い力に打ち勝つと考えられるため[106]、この領域周辺の原子核は共鳴としてしか存在せず、原子核を有意な時間で保つことができない可能性がある。また、これらの系列の間にある超アクチノイド元素のいくつかは、両方の島から離れすぎているために実際には存在しない可能性もあり[106]、その場合、周期表はZ = 130あたりで終わるかもしれない[16]。興味深いことに、周期性が停止している121番元素から156番元素までの領域は、2つの島の間のギャップと非常によく似ている[20]。
164番元素を超えると、核分裂性物質に対する安定性の限界を示す領域が中性子ドリップラインに収束し、より重い元素の存在に限界が生じる可能性がある[105]。とはいえ、Z = 210、274、354、N = 308、406、524、644、772とさらなる魔法数が予測されており[107]、616210と798274の2つのベータ崩壊に安定な二重魔法核が発見されたが、同じ計算方法で298Flと472164も予測された(Z = 354で予測された二重魔法核はベータ崩壊に対し不安定で、998354は中性子不足、1126354は中性子過剰であった)。616210と798274にはアルファ崩壊や核分裂に対するさらなる安定性が予測されており、616210の半減期は数百マイクロ秒にも及ぶ[107]が、Z = 114や164で予測されているような大きな安定性の島は存在しないと考えられている。超重元素の存在は閉殻による安定化効果に強く依存しているため、核の不安定性と自発核分裂が安定の島を超えて周期表の終わりを決定することになるだろうと考えられている[16][90][105]。
国際純正応用化学連合(IUPAC)は、原子核が電子雲を形成するのにかかる時間である10−14秒より長い寿命を持つ元素を、存在の定義としている。ただし、原子核は一般的に、核構造が形成されるのにかかる時間である約10 −22秒より長い寿命を持つ場合に存在するとみなされる。したがって、一部のZ値では原子核のみ実現可能であり、対応する元素が存在しない可能性がある[100]。
また、原子番号126を超える安定の島が、実際には存在しない可能性もある。原子核の殻構造がぼやけ、電子の閉殻構造はオガネソン付近で過ぎてしまうと予想され、また低エネルギー崩壊モードが容易に利用可能になるためである[108]。
核種の表の一部の領域では、球形核とは異なる魔法数を持つ非球形核によって、別の安定領域が存在することが予想される。卵形の原子核を持つ270Hs(Z = 108、N = 162)は、変形した二重魔法核の1つである[109]。超重核領域では、ほとんどの小さな原子核の内部で陽子がほぼ均一に分布しているのとは異なり、オガネソン同位体を含む一部の核では陽子の強いクーロン反発により、基底状態で陽子の中心密度が低下した泡のような形状を取ることがある[110][111]。ただし、このような形状では非常に自発核分裂が起こりやすい[112]。342136や466156など、さらに重い一部の領域の原子核は、代わりにトーラス(いわゆる「ドーナツ型」)または赤血球のような形状になり独自の魔法数と安定の島を持つが、簡単に自発核分裂を起こすこともある[113][114]。
未発見元素の崩壊特性の予測
[編集]安定性の主要な島は291Cnと293Cnの周辺にあると考えられているため、オガネソンを超える未発見の元素は非常に不安定で、マイクロ秒以下でアルファ崩壊や自発核分裂を起こす可能性がある。半減期が1マイクロ秒を超える正確な領域は不明だが、利用可能なターゲットや発射体との核融合反応で生成される、ウンビニリウムより重い元素の同位体は、半減期が1マイクロ秒以下となり検出されない可能性があることを様々なモデルが示唆している[60]。 一貫して予測されているのは、N = 184とN = 228、そしておそらくZ ~ 124とN ~ 198にも安定領域が存在することである。これらの核は数秒の半減期を持ち、主にアルファ崩壊と自発核分裂を起こすが、わずかなベータプラス崩壊(または電子捕獲)の分岐も存在するかもしれないと考えられている[115]。 これらの安定性が高まった領域の外側では、安定化効果が失われるために核分裂障壁が大幅に低下し核子の半減期は10−18秒未満になると予想される。特に、核子のペアによって障壁がさらに低くなる偶数-偶数の原子核では顕著である[105]。一般にアルファ崩壊の半減期は中性子数とともに増加し、最も中性子数の少ない同位体ではナノ秒、ベータ安定線(ベータ崩壊を起こさない核種群)に近いところでは数秒になると予想されている[43]。魔法数よりも中性子数が少ない原子核では結合エネルギーが大幅に低下するため、この傾向は崩れ、半減期は短くなる[43]。さらに中性子が不足している同位体も結合エネルギーが低く、陽子放出の可能性がある。クラスタ崩壊(重粒子放出)もいくつかの同位体の代替崩壊モードとして提案されているが[116]、これらの元素の同定にはさらに別のハードルがある。
電子配置
[編集]以下は、119番元素から174番元素まで、および184番元素の予想される電子配置である。記号[Og]は、現在知られている最後の元素であるオガネソン(Z = 118)の推定電子配置を示す。119番元素より前では、オガネソンが閉殻(不活性ガス)配置を持つ最後の元素であると予想されるため、表の元素の配置は[Og]で始まるように書かれている。[Og]は1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p6 4d10 4f14 5s2 5p6 5d10 5f14 6s2 6p6 6d10 7s2 7p6である。同様に、173、174および184番元素の構成の[172]は、172番元素の予想される閉殻構成を示す。
123番元素以降では完全なCCSD計算は利用できないため、この表のデータは暫定的なものとして考慮する必要がある[16][86][117]。123番元素およびより重い元素の場合、いくつかの考えられる電子配置は非常に類似したエネルギーレベルを持つと予想されるため、基底状態を予測することは非常に困難である。下表には提案されているすべての構成が含まれる(マーデルング則がおそらくこれ以降機能しなくなると考えられているため)[117][79][118]。
172番元素までの予測されたブロックはKulshaの提案であり、予想される利用可能な電子軌道に従う[22]。 ただし、138番元素以降のブロックについて、文献による合意はない。
元素 ブロック 予想される電子配置[15][16][86][19] 119 Uue ウンウンエンニウム sブロック [Og] 8s1 120 Ubn ウンビニリウム sブロック [Og] 8s2 121 Ubu ウンビウニウム gブロック [Og] 8s2 8p1
1/2[79]122 Ubb ウンビビウム gブロック [Og] 8s2 8p2
1/2[79]
[Og] 7d1 8s2 8p1
1/2123 Ubt ウンビトリウム gブロック [Og] 6f1 8s2 8p2
1/2[119]
[Og] 6f1 7d1 8s2 8p1
1/2[117][79]
[Og] 6f2 8s2 8p1
1/2
[Og] 8s2 8p2
1/2 8p1
3/2[117]124 Ubq ウンビクアジウム gブロック [Og] 6f2 8s2 8p2
1/2[79][119]
[Og] 6f3 8s2 8p1
1/2125 Ubp ウンビペンチウム gブロック [Og] 6f4 8s2 8p1
1/2[79]
[Og] 5g1 6f2 8s2 8p2
1/2[119]
[Og] 5g1 6f3 8s2 8p1
1/2
[Og] 8s2 0.81(5g1 6f2 8p2
1/2) + 0.17(5g1 6f1 7d2 8p1
1/2) + 0.02(6f3 7d1 8p1
1/2)126 Ubh ウンビヘキシウム gブロック [Og] 5g1 6f4 8s2 8p1
1/2[79]
[Og] 5g2 6f2 8s2 8p2
1/2[119]
[Og] 5g2 6f3 8s2 8p1
1/2
[Og] 8s2 0.998(5g2 6f3 8p1
1/2) + 0.002(5g2 6f2 8p2
1/2)127 Ubs ウンビセプチウム gブロック [Og] 5g2 6f3 8s2 8p2
1/2[79]
[Og] 5g3 6f2 8s2 8p2
1/2[119]
[Og] 8s2 0.88(5g3 6f2 8p2
1/2) + 0.12(5g3 6f1 7d2 8p1
1/2)128 Ubo ウンビオクチウム gブロック [Og] 5g3 6f3 8s2 8p2
1/2[79]
[Og] 5g4 6f2 8s2 8p2
1/2[119]
[Og] 8s2 0.88(5g4 6f2 8p2
1/2) + 0.12(5g4 6f1 7d2 8p1
1/2)129 Ube ウンビエンニウム gブロック [Og] 5g4 6f3 7d1 8s2 8p1
1/2
[Og] 5g4 6f3 8s2 8p2
1/2[79][119]
[Og] 5g5 6f2 8s2 8p2
1/2
[Og] 5g4 6f3 7d1 8s2 8p1
1/2130 Utn ウントリニリウム gブロック [Og] 5g5 6f3 7d1 8s2 8p1
1/2
[Og] 5g5 6f3 8s2 8p2
1/2[79][119]
[Og] 5g6 6f2 8s2 8p2
1/2
[Og] 5g5 6f3 7d1 8s2 8p1
1/2131 Utu ウントリウニウム gブロック [Og] 5g6 6f3 8s2 8p2
1/2[79][119]
[Og] 5g7 6f2 8s2 8p2
1/2
[Og] 8s2 0.86(5g6 6f3 8p2
1/2) + 0.14(5g6 6f2 7d2 8p1
1/2)132 Utb ウントリビウム gブロック [Og] 5g7 6f3 8s2 8p2
1/2[119]
[Og] 5g8 6f2 8s2 8p2
1/2133 Utt ウントリトリウム gブロック [Og] 5g8 6f3 8s2 8p2
1/2[119]134 Utq ウントリクアジウム gブロック [Og] 5g8 6f4 8s2 8p2
1/2[119]135 Utp ウントリペンチウム gブロック [Og] 5g9 6f4 8s2 8p2
1/2[119]136 Uth ウントリヘキシウム gブロック [Og] 5g10 6f4 8s2 8p2
1/2[119]137 Uts ウントリセプチウム gブロック [Og] 5g11 6f4 8s2 8p2
1/2[119]138 Uto ウントリオクチウム gブロック [Og] 5g12 6f4 8s2 8p2
1/2[119]
[Og] 5g12 6f3 7d1 8s2 8p2
1/2139 Ute ウントリエンニウム gブロック [Og] 5g13 6f3 7d1 8s2 8p2
1/2[119]
[Og] 5g13 6f2 7d2 8s2 8p2
1/2140 Uqn ウンクアドニリウム gブロック [Og] 5g14 6f3 7d1 8s2 8p2
1/2[119]
[Og] 5g15 6f1 8s2 8p2
1/2 8p2
3/2141 Uqu ウンクアドウニウム gブロック [Og] 5g15 6f2 7d2 8s2 8p2
1/2[119]142 Uqb ウンクアドビウム gブロック [Og] 5g16 6f2 7d2 8s2 8p2
1/2[119]143 Uqt ウンクアドトリウム fブロック [Og] 5g17 6f2 7d2 8s2 8p2
1/2[119]144 Uqq ウンクアドクアジウム fブロック [Og] 5g18 6f2 7d2 8s2 8p2
1/2[119]
[Og] 5g18 6f1 7d3 8s2 8p2
1/2
[Og] 5g17 6f2 7d3 8s2 8p2
1/2
[Og] 8s2 0.95(5g17 6f2 7d3 8p2
1/2) + 0.05(5g17 6f4 7d1 8p2
1/2)145 Uqp ウンクアドペンチウム fブロック [Og] 5g18 6f3 7d2 8s2 8p2
1/2[119]146 Uqh ウンクアドヘキシウム fブロック [Og] 5g18 6f4 7d2 8s2 8p2
1/2[119]147 Uqs ウンクアドセプチウム fブロック [Og] 5g18 6f5 7d2 8s2 8p2
1/2[119]148 Uqo ウンクアドオクチウム fブロック [Og] 5g18 6f6 7d2 8s2 8p2
1/2[119]149 Uqe ウンクアドエンニウム fブロック [Og] 5g18 6f6 7d3 8s2 8p2
1/2[119]150 Upn ウンペントニリウム fブロック [Og] 5g18 6f6 7d4 8s2 8p2
1/2
[Og] 5g18 6f7 7d3 8s2 8p2
1/2[119]151 Upu ウンペントウニウム fブロック [Og] 5g18 6f8 7d3 8s2 8p2
1/2[119]152 Upb ウンペントビウム fブロック [Og] 5g18 6f9 7d3 8s2 8p2
1/2[119]153 Upt ウンペントトリウム fブロック [Og] 5g18 6f10 7d3 8s2 8p2
1/2
[Og] 5g18 6f11 7d2 8s2 8p2
1/2[119]154 Upq ウンペントクアジウム fブロック [Og] 5g18 6f11 7d3 8s2 8p2
1/2
[Og] 5g18 6f12 7d2 8s2 8p2
1/2[119]155 Upp ウンペントペンチウム fブロック [Og] 5g18 6f12 7d3 8s2 8p2
1/2
[Og] 5g18 6f13 7d2 8s2 8p2
1/2[119]156 Uph ウンペントヘキシウム fブロック [Og] 5g18 6f13 7d3 8s2 8p2
1/2
[Og] 5g18 6f14 7d2 8s2 8p2
1/2[119]157 Ups ウンペントセプチウム dブロック [Og] 5g18 6f14 7d3 8s2 8p2
1/2[119]158 Upo ウンペントオクチウム dブロック [Og] 5g18 6f14 7d4 8s2 8p2
1/2[119]159 Upe ウンペントエンニウム dブロック [Og] 5g18 6f14 7d5 8s2 8p2
1/2
[Og] 5g18 6f14 7d4 8s2 8p2
1/2 9s1[119]160 Uhn ウンヘキスニリウム dブロック [Og] 5g18 6f14 7d6 8s2 8p2
1/2
[Og] 5g18 6f14 7d5 8s2 8p2
1/2 9s1[119]161 Uhu ウンヘキスウニウム dブロック [Og] 5g18 6f14 7d7 8s2 8p2
1/2
[Og] 5g18 6f14 7d6 8s2 8p2
1/2 9s1[119]162 Uhb ウンヘキスビウム dブロック [Og] 5g18 6f14 7d8 8s2 8p2
1/2
[Og] 5g18 6f14 7d7 8s2 8p2
1/2 9s1[119]163 Uht ウンヘキストリウム dブロック [Og] 5g18 6f14 7d9 8s2 8p2
1/2
[Og] 5g18 6f14 7d8 8s2 8p2
1/2 9s1[119]164 Uhq ウンヘキスクアジウム dブロック [Og] 5g18 6f14 7d10 8s2 8p2
1/2[119]165 Uhp ウンヘキスペンチウム dブロック [Og] 5g18 6f14 7d10 8s2 8p2
1/2 9s1[119]166 Uhh ウンヘキスヘキシウム dブロック [Og] 5g18 6f14 7d10 8s2 8p2
1/2 9s2[119]167 Uhs ウンヘキスセプチウム pブロック [Og] 5g18 6f14 7d10 8s2 8p2
1/2 9s2 9p1
1/2
[Og] 5g18 6f14 7d10 8s2 8p2
1/2 8p1
3/2 9s2[119]168 Uho ウンヘキスオクチウム pブロック [Og] 5g18 6f14 7d10 8s2 8p2
1/2 9s2 9p2
1/2
[Og] 5g18 6f14 7d10 8s2 8p2
1/2 8p2
3/2 9s2[119]169 Uhe ウンヘキスエンニウム pブロック [Og] 5g18 6f14 7d10 8s2 8p2
1/2 8p1
3/2 9s2 9p2
1/2
[Og] 5g18 6f14 7d10 8s2 8p2
1/2 8p3
3/2 9s2[119]170 Usn ウンセプトニリウム pブロック [Og] 5g18 6f14 7d10 8s2 8p2
1/2 8p2
3/2 9s2 9p2
1/2
[Og] 5g18 6f14 7d10 8s2 8p2
1/2 8p4
3/2 9s2[119]171 Usu ウンセプトウニウム pブロック [Og] 5g18 6f14 7d10 8s2 8p2
1/2 8p3
3/2 9s2 9p2
1/2
[Og] 5g18 6f14 7d10 8s2 8p2
1/2 8p4
3/2 9s2 9p1
1/2[119]172 Usb ウンセプトビウム pブロック [Og] 5g18 6f14 7d10 8s2 8p2
1/2 8p4
3/2 9s2 9p2
1/2[119]173 Ust ウンセプトトリウム ? [172] 6g1
[172] 9p1
3/2
[172] 10s1[87]174 Usq ウンセプトクアジウム ? [172] 8d1 10s1[87] ... ... ... ... ... 184 Uoq ウンオクトクアジウム ? [172] 6g5 7f4 8d3
出典
[編集]- ^ a b Seaborg, Glenn T. (August 26, 1996). “An Early History of LBNL”. 2011年2月25日閲覧。
- ^ Frazier, K. (1978). “Superheavy Elements”. Science News 113 (15): 236–238. doi:10.2307/3963006. JSTOR 3963006.
- ^ Element 122 was claimed to exist naturally in April 2008, but this claim was widely believed to be erroneous. “Heaviest element claim criticised”. Rsc.org (2008年5月2日). 2010年3月16日閲覧。
- ^ a b c d e f g h i j k l m n o p q r s t Fricke, B.; Greiner, W.; Waber, J. T. (1971). “The continuation of the periodic table up to Z = 172. The chemistry of superheavy elements”. Theoretica Chimica Acta 21 (3): 235–260. doi:10.1007/BF01172015.
- ^ “Kernchemie”. www.kernchemie.de. 2014年11月9日閲覧。
- ^ Schiff, L. I.; Snyder, H.; Weinberg, J. (1940). “On the Existence of Stationary States of the Mesotron Field”. Physical Review 57 (4): 315–318. Bibcode: 1940PhRv...57..315S. doi:10.1103/PhysRev.57.315.
- ^ Kragh, Helge (2018). From Transuranic to Superheavy Elements: A Story of Dispute and Creation. Springer. pp. 6–10. ISBN 9783319758138
- ^ a b c d e f g h Hoffman, D.C; Ghiorso, A.; Seaborg, G.T. (2000). The Transuranium People: The Inside Story. Imperial College Press. ISBN 978-1-86094-087-3
- ^ a b Maly, J.; Walz, D.R. (1980). Search for superheavy elements among fossil fission tracks in zircon. ReportNumber:SLAC-PUB-2554 2021年11月28日閲覧。.
- ^ a b c d e f g h i j k l m Emsley, John (2011). Nature's Building Blocks: An A-Z Guide to the Elements (New ed.). New York, NY: Oxford University Press. p. 588. ISBN 978-0-19-960563-7
- ^ a b Hofmann, Sigurd (2002). On Beyond Uranium. Taylor & Francis. p. 105. ISBN 978-0-415-28496-7
- ^ a b c d Epherre, M.; Stephan, C. (1975). “Les éléments superlourds” (フランス語). Le Journal de Physique Colloques 11 (36): C5-159-C5-164. doi:10.1051/jphyscol:1975541.
- ^ a b c d e f g h i j k l m Pyykkö, Pekka (2011). “A suggested periodic table up to Z≤ 172, based on Dirac–Fock calculations on atoms and ions”. Physical Chemistry Chemical Physics 13 (1): 161–8. Bibcode: 2011PCCP...13..161P. doi:10.1039/c0cp01575j. PMID 20967377.
- ^ a b Seaborg, Glenn T. (c. 2006). "transuranium element (chemical element)". Encyclopædia Britannica. 2010年3月16日閲覧。
- ^ a b c d e f g h i j k l m n o p Hoffman, Darleane C.; Lee, Diana M.; Pershina, Valeria (2006). “Transactinides and the future elements”. In Morss; Edelstein, Norman M.; Fuger, Jean. The Chemistry of the Actinide and Transactinide Elements (3rd ed.). Dordrecht, The Netherlands: Springer Science+Business Media. ISBN 978-1-4020-3555-5
- ^ a b c d e f g h i j k l m n o p q r s Fricke, Burkhard (1975). Superheavy elements: a prediction of their chemical and physical properties. Structure and Bonding. 21. 89–144. doi:10.1007/BFb0116498. ISBN 978-3-540-07109-9 4 October 2013閲覧。
- ^ a b c d Fricke, Burkhard; Waber, J. T. (1971). “Theoretical Predictions of the Chemistry of Superheavy Elements: Continuation of the Periodic Table up to Z=184”. Actinides Reviews 1: 433–485 5 January 2024閲覧。.
- ^ a b A suggested periodic table up to Z ≤ 172, based on Dirac–Fock calculations on atoms and ions, Pekka Pyykkö, Phys. Chem. Chem. Phys., 2010, Advance Article [1]
- ^ a b c d e Nefedov, V.I.; Trzhaskovskaya, M.B.; Yarzhemskii, V.G. (2006). “Electronic Configurations and the Periodic Table for Superheavy Elements”. Doklady Physical Chemistry 408 (2): 149–151. doi:10.1134/S0012501606060029. ISSN 0012-5016.
- ^ a b c d e f g h i j Kulsha, A. V.. “Есть ли граница у таблицы Менделеева?” [Is there a boundary to the Mendeleev table?] (ロシア語). www.primefan.ru. 8 September 2018閲覧。
- ^ a b Sicius, Hermann (2021) (ドイツ語). Handbuch der chemischen Elemente. Springer. p. 1085. "Kulsha nennt die 36 Elemente zwischen 121 und 156 „Ultransition Elements“ und schlägt vor, sie in zwei Serien aufzuteilen, in eine von 121 bis 138 und eine zweite von 139 bis 156. Die erste ähnelte eher den Lanthanoiden (Seltenerden), die zweite mehr den Actinoiden."
- ^ a b “Feasible electron configurations of dications up to Z = 172”. 2023年6月4日閲覧。
- ^ Wothers, Peter (2019). Antimony, Gold, and Jupiter's Wolf. Oxford University Press. p. vii. ISBN 978-0-19-965272-3. "It’s possible that other elements might be synthesized—research is certainly ongoing—but it’s unlikely that the table will ever appear as neat again, since to fill the next row, another fifty-four elements would need to be made."
- ^ Smits, Odile R.; Düllmann, Christoph E.; Indelicato, Paul; Nazarewicz, Witold; Schwerdtfeger, Peter (2023). “The quest for superheavy elements and the limit of the periodic table”. Nature Reviews Physics 6 (2): 86–98. doi:10.1038/s42254-023-00668-y.
- ^ Lougheed, R. et al. (1985). “Search for superheavy elements using 48Ca + 254Esg reaction”. Physical Review C 32 (5): 1760–1763. Bibcode: 1985PhRvC..32.1760L. doi:10.1103/PhysRevC.32.1760. PMID 9953034.
- ^ Feng, Z; Jin, G.; Li, J.; Scheid, W. (2009). “Production of heavy and superheavy nuclei in massive fusion reactions”. Nuclear Physics A 816 (1): 33. arXiv:0803.1117. Bibcode: 2009NuPhA.816...33F. doi:10.1016/j.nuclphysa.2008.11.003.
- ^ Modern alchemy: Turning a line, The Economist, May 12, 2012.
- ^ a b c Superheavy Element Search Campaign at TASCA. J. Khuyagbaatar
- ^ a b c d e f g h i Zagrebaev, Valeriy; Karpov, Alexander; Greiner, Walter (2013). “Future of superheavy element research: Which nuclei could be synthesized within the next few years?”. Journal of Physics 420 (1): 012001. arXiv:1207.5700. Bibcode: 2013JPhCS.420a2001Z. doi:10.1088/1742-6596/420/1/012001.
- ^ Khuyagbaatar, J.; Yakushev, A.; Düllmann, Ch. E. (2020). “Search for elements 119 and 120”. Physical Review C 102 (6): 064602. Bibcode: 2020PhRvC.102f4602K. doi:10.1103/PhysRevC.102.064602. hdl:1885/289860 25 January 2021閲覧。.
- ^ “Search for element 119: Christoph E. Düllmann for the TASCA E119 collaboration”. 2016年3月4日時点のオリジナルよりアーカイブ。2017年4月5日閲覧。
- ^ a b c d e “Superheavy Element Research at TASCA”. asrc.jaea.go.jp (2012年). 23 September 2016閲覧。
- ^ Sakai, Hideyuki; Haba, Hiromitsu; Morimoto, Kouji; Sakamoto, Naruhiko (9 December 2022). “Facility upgrade for superheavy-element research at RIKEN”. The European Physical Journal A 58 (238): 238. Bibcode: 2022EPJA...58..238S. doi:10.1140/epja/s10050-022-00888-3. PMC 9734366. PMID 36533209.
- ^ a b Sakai, Hideyuki (27 February 2019). “Search for a New Element at RIKEN Nishina Center”. infn.it. 17 December 2019閲覧。
- ^ a b Gates, J.; Pore, J.; Crawford, H.; Shaughnessy, D.; Stoyer, M. A. (25 October 2022). The Status and Ambitions of the US Heavy Element Program. doi:10.2172/1896856. OSTI 1896856 13 November 2022閲覧。.
- ^ 櫻井, 博儀 (1 April 2020). “ごあいさつ | 仁科加速器科学研究センター”. 2024年8月1日閲覧。 “線形加速器と分離装置は2020年初頭に高度化が完了し、新たな装置を利用して、119番元素以降の新元素生成を目指しています。”
- ^ Ball, P. (2019). “Extreme chemistry: experiments at the edge of the periodic table”. Nature 565 (7741): 552–555. Bibcode: 2019Natur.565..552B. doi:10.1038/d41586-019-00285-9. ISSN 1476-4687. PMID 30700884. ""We started the search for element 119 last June," says RIKEN researcher Hideto En'yo. "It will certainly take a long time — years and years — so we will continue the same experiment intermittently for 100 or more days per year, until we or somebody else discovers it.""
- ^ Joint Institute for Nuclear Research (24 July 2021). “JINR presented largest Periodic Table to Dubna”. jinr.ru. Joint Institute for Nuclear Research. 27 January 2022閲覧。
- ^ “Superheavy Element Factory: overview of obtained results”. Joint Institute for Nuclear Research (24 August 2023). 7 December 2023閲覧。
- ^ “A New Block on the Periodic Table”. Lawrence Livermore National Laboratory. (April 2007). オリジナルの2008年5月28日時点におけるアーカイブ。 2008年1月18日閲覧。
- ^ “Synthesis of New Nuclei and Study of Nuclear Properties and Heavy-Ion Reaction Mechanisms”. jinr.ru. Joint Institute for Nuclear Research (2007年). 23 September 2016閲覧。
- ^ Chowdhury, P. Roy; Samanta, C.; Basu, D. N. (2008). “Search for long lived heaviest nuclei beyond the valley of stability”. Physical Review C 77 (4): 044603. arXiv:0802.3837. Bibcode: 2008PhRvC..77d4603C. doi:10.1103/PhysRevC.77.044603.
- ^ a b c Chowdhury, R. P.; Samanta, C.; Basu, D.N. (2008). “Nuclear half-lives for α -radioactivity of elements with 100 ≤ Z ≤ 130”. en:Atomic Data and Nuclear Data Tables 94 (6): 781–806. arXiv:0802.4161. Bibcode: 2008ADNDT..94..781C. doi:10.1016/j.adt.2008.01.003.
- ^ a b Oganessian, Yu. Ts.; Utyonkov, V.; Lobanov, Yu.; Abdullin, F.; Polyakov, A.; Sagaidak, R.; Shirokovsky, I.; Tsyganov, Yu. et al. (2009). “Attempt to produce element 120 in the 244Pu+58Fe reaction”. Phys. Rev. C 79 (2): 024603. Bibcode: 2009PhRvC..79b4603O. doi:10.1103/PhysRevC.79.024603.
- ^ a b Hoffman, S.; et al. (2008). Probing shell effects at Z=120 and N=184 (Report). GSI Scientific Report. p. 131.
- ^ a b Hofmann, S.; Heinz, S.; Mann, R.; Maurer, J.; Münzenberg, G.; Antalic, S.; Barth, W.; Burkhard, H. G. et al. (2016). “Review of even element super-heavy nuclei and search for element 120”. The European Physical Journal A 2016 (52): 180. Bibcode: 2016EPJA...52..180H. doi:10.1140/epja/i2016-16180-4.
- ^ GSI (2012年4月5日). “Searching for the island of stability”. www.gsi.de. GSI. 23 September 2016閲覧。
- ^ “Weighty matters: Sigurd Hofmann on the heaviest of nuclei”. JPhys+ (2 October 2015). 23 September 2016閲覧。
- ^ Hofmann, Sigurd (August 2015). “Search for Isotopes of Element 120 ON the Island of SHN”. 213–224. Bibcode: 2015exon.conf..213H. doi:10.1142/9789814699464_0023. ISBN 978-981-4699-45-7
- ^ “Superheavy Element Research: News from GSI and Mainz” (20 October 2011). 23 September 2016閲覧。
- ^ Siwek-Wilczyńska, K.; Cap, T.; Wilczyński, J. (April 2010). “How can one synthesize the element Z = 120?”. International Journal of Modern Physics E 19 (4): 500. Bibcode: 2010IJMPE..19..500S. doi:10.1142/S021830131001490X.
- ^ a b c d e Kratz, J. V. (5 September 2011). The Impact of Superheavy Elements on the Chemical and Physical Sciences (PDF). 4th International Conference on the Chemistry and Physics of the Transactinide Elements. 2013年8月27日閲覧。
- ^ “How are new chemical elements born?”. jinr.ru. JINR (24 May 2021). 4 November 2021閲覧。 “Previously, we worked mainly with calcium. This is element 20 in the Periodic Table. It was used to bombard the target. And the heaviest element that can be used to make a target is californium, 98. Accordingly, 98 + 20 is 118. That is, to get element 120, we need to proceed to the next particle. This is most likely titanium: 22 + 98 = 120.
There is still much work to adjust the system. I don’t want to get ahead of myself, but if we can successfully conduct all the model experiments, then the first experiments on the synthesis of element 120 will probably start this year.” - ^ Ahuja, Anjana (18 October 2023). “Even the periodic table must bow to the reality of war”. Financial Times 20 October 2023閲覧。
- ^ “В ЛЯР ОИЯИ впервые в мире синтезирован ливерморий-288 [Livermorium-288 was synthesized for the first time in the world at FLNR JINR]” (ロシア語). Joint Institute for Nuclear Research. (23 October 2023) 18 November 2023閲覧。
- ^ Mayer, Anastasiya (31 May 2023). “"Большинство наших партнеров гораздо мудрее политиков" [Most of our partners are much wiser than politicians]” (ロシア語). en:Vedomosti 15 August 2023閲覧. "В этом году мы фактически завершаем подготовительную серию экспериментов по отладке всех режимов ускорителя и масс-спектрометров для синтеза 120-го элемента. Научились получать высокие интенсивности ускоренного хрома и титана. Научились детектировать сверхтяжелые одиночные атомы в реакциях с минимальным сечением. Теперь ждем, когда закончится наработка материала для мишени на реакторах и сепараторах у наших партнеров в «Росатоме» и в США: кюрий, берклий, калифорний. Надеюсь, что в 2025 г. мы полноценно приступим к синтезу 120-го элемента."
- ^ Chapman, Kit (10 October 2023). “Berkeley Lab to lead US hunt for element 120 after breakdown of collaboration with Russia”. Chemistry World 20 October 2023閲覧。
- ^ Biron, Lauren (16 October 2023). “Berkeley Lab to Test New Approach to Making Superheavy Elements”. lbl.gov. en:Lawrence Berkeley National Laboratory. 20 October 2023閲覧。
- ^ Hofmann, Sigurd (2014). On Beyond Uranium: Journey to the End of the Periodic Table. CRC Press. p. 105. ISBN 978-0415284950
- ^ a b c “Superheavy Nuclei: which regions of nuclear map are accessible in the nearest studies”. cyclotron.tamu.edu. Texas A & M University (2015年). 30 October 2018閲覧。
- ^ a b see Flerov lab annual reports 2000–2004 inclusive http://www1.jinr.ru/Reports/Reports_eng_arh.html
- ^ a b Thomas, R.G.; Saxena, A.; Sahu, P.K.; Choudhury, R.K.; Govil, I.M.; Kailas, S.; Kapoor, S.S.; Barubi, M. et al. (2007). “Fission and binary fragmentation reactions in 80Se+208Pb and 80Se+232Th systems”. Physical Review C 75 (2): 024604–1–024604–9. doi:10.1103/PhysRevC.75.024604. hdl:2158/776924.
- ^ Lodhi, M.A.K., ed (March 1978). Superheavy Elements: Proceedings of the International Symposium on Superheavy Elements. Lubbock, Texas: Pergamon Press. ISBN 978-0-08-022946-1
- ^ Audi, G.; Kondev, F.G.; Wang, M.; Huang, W.J.; Naimi, S. (2017). “The NUBASE2016 evaluation of nuclear properties”. Chinese Physics C 41 (3): 030001. Bibcode: 2017ChPhC..41c0001A. doi:10.1088/1674-1137/41/3/030001.
- ^ a b Marinov, A.; Rodushkin, I.; Kolb, D.; Pape, A.; Kashiv, Y.; Brandt, R.; Gentry, R. V.; Miller, H. W. (2010). “Evidence for a long-lived superheavy nucleus with atomic mass number A=292 and atomic number Z=~122 in natural Th”. International Journal of Modern Physics E 19 (1): 131–140. arXiv:0804.3869. Bibcode: 2010IJMPE..19..131M. doi:10.1142/S0218301310014662.
- ^ Royal Society of Chemistry, "Heaviest element claim criticised Archived 2016-03-04 at the Wayback Machine.", Chemical World.
- ^ a b Marinov, A.; Rodushkin, I.; Kashiv, Y.; Halicz, L.; Segal, I.; Pape, A.; Gentry, R. V.; Miller, H. W. et al. (2007). “Existence of long-lived isomeric states in naturally-occurring neutron-deficient Th isotopes”. Phys. Rev. C 76 (2): 021303(R). arXiv:nucl-ex/0605008. Bibcode: 2007PhRvC..76b1303M. doi:10.1103/PhysRevC.76.021303.
- ^ R. C. Barber; J. R. De Laeter (2009). “Comment on 'Existence of long-lived isomeric states in naturally-occurring neutron-deficient Th isotopes'”. Phys. Rev. C 79 (4): 049801. Bibcode: 2009PhRvC..79d9801B. doi:10.1103/PhysRevC.79.049801.
- ^ A. Marinov; I. Rodushkin; Y. Kashiv; L. Halicz; I. Segal; A. Pape; R. V. Gentry; H. W. Miller et al. (2009). “Reply to "Comment on 'Existence of long-lived isomeric states in naturally-occurring neutron-deficient Th isotopes'"”. Phys. Rev. C 79 (4): 049802. Bibcode: 2009PhRvC..79d9802M. doi:10.1103/PhysRevC.79.049802.
- ^ J. Lachner; I. Dillmann; T. Faestermann; G. Korschinek; M. Poutivtsev; G. Rugel (2008). “Search for long-lived isomeric states in neutron-deficient thorium isotopes”. Phys. Rev. C 78 (6): 064313. arXiv:0907.0126. Bibcode: 2008PhRvC..78f4313L. doi:10.1103/PhysRevC.78.064313.
- ^ Marinov, A.; Rodushkin, I.; Pape, A.; Kashiv, Y.; Kolb, D.; Brandt, R.; Gentry, R. V.; Miller, H. W. et al. (2009). “Existence of Long-Lived Isotopes of a Superheavy Element in Natural Au”. International Journal of Modern Physics E 18 (3): 621–629. arXiv:nucl-ex/0702051. Bibcode: 2009IJMPE..18..621M. doi:10.1142/S021830130901280X. オリジナルのJuly 14, 2014時点におけるアーカイブ。 February 12, 2012閲覧。.
- ^ a b Emsley, John (2011). Nature's Building Blocks: An A–Z Guide to the Elements (New ed.). New York: Oxford University Press. p. 592. ISBN 978-0-19-960563-7
- ^ Petermann, I; Langanke, K.; Martínez-Pinedo, G.; Panov, I.V; Reinhard, P.G.; Thielemann, F.K. (2012). “Have superheavy elements been produced in nature?”. European Physical Journal A 48 (122): 122. arXiv:1207.3432. Bibcode: 2012EPJA...48..122P. doi:10.1140/epja/i2012-12122-6.
- ^ Jason Wright (16 March 2017). “Przybylski's Star III: Neutron Stars, Unbinilium, and aliens”. 31 July 2018閲覧。
- ^ V. A. Dzuba; V. V. Flambaum; J. K. Webb (2017). “Isotope shift and search for metastable superheavy elements in astrophysical data”. Physical Review A 95 (6): 062515. arXiv:1703.04250. Bibcode: 2017PhRvA..95f2515D. doi:10.1103/PhysRevA.95.062515.
- ^ Archived at Ghostarchive and the Wayback Machine: SciShow Space (31 July 2018). “This Star Might Be Hiding Undiscovered Elements. Przybylski's Star”. youtube.com. 31 July 2018閲覧。
- ^ Waber, J. T. (1969). “SCF Dirac–Slater Calculations of the Translawrencium Elements”. The Journal of Chemical Physics 51 (2): 664. Bibcode: 1969JChPh..51..664W. doi:10.1063/1.1672054.
- ^ Amador, Davi H. T.; de Oliveira, Heibbe C. B.; Sambrano, Julio R.; Gargano, Ricardo; de Macedo, Luiz Guilherme M. (12 September 2016). “4-Component correlated all-electron study on Eka-actinium Fluoride (E121F) including Gaunt interaction: Accurate analytical form, bonding and influence on rovibrational spectra”. Chemical Physics Letters 662: 169–175. Bibcode: 2016CPL...662..169A. doi:10.1016/j.cplett.2016.09.025. hdl:11449/168956.
- ^ a b c d e f g h i j k l m Umemoto, Koichiro; Saito, Susumu (1996). “Electronic Configurations of Superheavy Elements”. Journal of the Physical Society of Japan 65 (10): 3175–9. Bibcode: 1996JPSJ...65.3175U. doi:10.1143/JPSJ.65.3175 31 January 2021閲覧。.
- ^ a b c d e Dongon, J.P.; Pyykkö, P. (2017). “Chemistry of the 5g elements. Relativistic calculations on hexafluorides”. Angewandte Chemie International Edition 56 (34): 10132–10134. doi:10.1002/anie.201701609. PMID 28444891.
- ^ Jacoby, Mitch (2006). “As-yet-unsynthesized superheavy atom should form a stable diatomic molecule with fluorine”. Chemical & Engineering News 84 (10): 19. doi:10.1021/cen-v084n010.p019a.
- ^ Makhyoun, M. A. (October 1988). “On the electronic structure of 5g1 complexes of element 125: a quasi-relativistic MS-Xα study”. Journal de Chimie Physique et de Physico-Chimie Biologique 85 (10): 917–24. Bibcode: 1988JCP....85..917M. doi:10.1051/jcp/1988850917.
- ^ a b c Koura, H.; Chiba, S. (2013). “Single-Particle Levels of Spherical Nuclei in the Superheavy and Extremely Superheavy Mass Region”. Journal of the Physical Society of Japan 82 (1): 014201. Bibcode: 2013JPSJ...82a4201K. doi:10.7566/JPSJ.82.014201.
- ^ a b “Nuclear scientists eye future landfall on a second 'island of stability'”. EurekAlert! (6 April 2008). 2015年12月17日閲覧。
- ^ a b Grumann, Jens; Mosel, Ulrich; Fink, Bernd; Greiner, Walter (1969). “Investigation of the stability of superheavy nuclei aroundZ=114 andZ=164”. Zeitschrift für Physik 228 (5): 371–386. Bibcode: 1969ZPhy..228..371G. doi:10.1007/BF01406719.
- ^ a b c Fricke, Burkhard (1977). “Dirac-Fock-Slater calculations for the elements Z = 100, fermium, to Z = 173”. Recent Impact of Physics on Inorganic Chemistry 19: 83–192. Bibcode: 1977ADNDT..19...83F. doi:10.1016/0092-640X(77)90010-9 25 February 2016閲覧。.
- ^ a b c d Eliav, Ephraim (26 April 2023). “Benchmark atomic electronic structures calculations at the edge of Periodic Table”. jinr.ru. JINR. 29 July 2023閲覧。
- ^ Penneman, R. A.; Mann, J. B.; Jørgensen, C. K. (February 1971). “Speculations on the chemistry of superheavy elements such as Z = 164”. Chemical Physics Letters 8 (4): 321–326. Bibcode: 1971CPL.....8..321P. doi:10.1016/0009-2614(71)80054-4.
- ^ Cwiok, S.; Heenen, P.-H.; Nazarewicz, W. (2005). “Shape coexistence and triaxiality in the superheavy nuclei”. Nature 433 (7027): 705–9. Bibcode: 2005Natur.433..705C. doi:10.1038/nature03336. PMID 15716943.
- ^ a b Gambhir, Y. K.; Bhagwat, A.; Gupta, M. (2015). “The highest limiting Z in the extended periodic table”. Journal of Physics G: Nuclear and Particle Physics 42 (12): 125105. Bibcode: 2015JPhG...42l5105G. doi:10.1088/0954-3899/42/12/125105.
- ^ a b c Philip Ball (November 2010). “Would element 137 really spell the end of the periodic table? Philip Ball examines the evidence”. en:Chemistry World. Royal Society of Chemistry. 2012年9月30日閲覧。
- ^ Eisberg, R.; Resnick, R. (1985). Quantum Physics of Atoms, Molecules, Solids, Nuclei and Particles. Wiley. ISBN 9780471873730
- ^ “Solution of the Dirac Equation for Hydrogen”. 2024年7月28日閲覧。
- ^ Bjorken, J. D.; Drell, S. D. (1964). Relativistic Quantum Mechanics. McGraw-Hill
- ^ a b c d Smits, O. R.; Indelicato, P.; Nazarewicz, W.; Piibeleht, M.; Schwerdtfeger, P. (2023). “Pushing the limits of the periodic table—A review on atomic relativistic electronic structure theory and calculations for the superheavy elements”. Physics Reports 1035: 1–57. arXiv:2301.02553. Bibcode: 2023PhR..1035....1S. doi:10.1016/j.physrep.2023.09.004.
- ^ Greiner, W.; Schramm, S. (2008). “Resource Letter QEDV-1: The QED vacuum”. en:American Journal of Physics 76 (6): 509. Bibcode: 2008AmJPh..76..509G. doi:10.1119/1.2820395., and references therein
- ^ Wang, Yang; Wong, Dillon; Shytov, Andrey V.; Brar, Victor W.; Choi, Sangkook; Wu, Qiong; Tsai, Hsin-Zon; Regan, William et al. (May 10, 2013). “Observing Atomic Collapse Resonances in Artificial Nuclei on Graphene”. Science 340 (6133): 734–737. arXiv:1510.02890. Bibcode: 2013Sci...340..734W. doi:10.1126/science.1234320. PMID 23470728.
- ^ Indelicato, Paul; Bieroń, Jacek; Jönsson, Per (2011-06-01). “Are MCDF calculations 101% correct in the super-heavy elements range?” (英語). Theoretical Chemistry Accounts 129 (3–5): 495–505. doi:10.1007/s00214-010-0887-3. hdl:2043/12984. ISSN 1432-881X.
- ^ Reinhardt, Joachim; Greiner, Walter (2015). “Probing Supercritical Fields with Real and with Artificial Nuclei”. Nuclear Physics: Present and Future. pp. 195–210. doi:10.1007/978-3-319-10199-6_19. ISBN 978-3-319-10198-9
- ^ a b Giuliani, S. A.; Matheson, Z.; Nazarewicz, W.; Olsen, E.; Reinhard, P.-G.; Sadhukhan, J.; Schtruempf, B.; Schunck, N. et al. (2019). “Colloquium: Superheavy elements: Oganesson and beyond”. Reviews of Modern Physics 91 (1): 011001-1–011001-25. Bibcode: 2019RvMP...91a1001G. doi:10.1103/RevModPhys.91.011001.
- ^ Holdom, B.; Ren, J.; Zhang, C. (2018). “Quark matter may not be strange”. Physical Review Letters 120 (1): 222001-1–222001-6. arXiv:1707.06610. Bibcode: 2018PhRvL.120v2001H. doi:10.1103/PhysRevLett.120.222001. PMID 29906186.
- ^ Cheng-Jun, Xia; She-Sheng, Xue; Ren-Xin, Xu; Shan-Gui, Zhou (2020). “Supercritically charged objects and electron-positron pair creation”. Physical Review D 101 (10): 103031. arXiv:2001.03531. Bibcode: 2020PhRvD.101j3031X. doi:10.1103/PhysRevD.101.103031.
- ^ Marcillac, Pierre de; Noël Coron; Gérard Dambier; Jacques Leblanc; Jean-Pierre Moalic (April 2003). “Experimental detection of α-particles from the radioactive decay of natural bismuth”. Nature 422 (6934): 876–878. Bibcode: 2003Natur.422..876D. doi:10.1038/nature01541. PMID 12712201.
- ^ Considine, Glenn D.; Kulik, Peter H. (2002). Van Nostrand's scientific encyclopedia (9 ed.). Wiley-Interscience. ISBN 978-0-471-33230-5. OCLC 223349096
- ^ a b c d Koura, H. (2011). Decay modes and a limit of existence of nuclei in the superheavy mass region (PDF). 4th International Conference on the Chemistry and Physics of the Transactinide Elements. 2018年11月18日閲覧。
- ^ a b Greiner, W. (2013). “Nuclei: superheavy-superneutronic-strange-and of antimatter”. Journal of Physics: Conference Series 413 (1): 012002. Bibcode: 2013JPhCS.413a2002G. doi:10.1088/1742-6596/413/1/012002.
- ^ a b Denisov, V. (2005). “Magic numbers of ultraheavy nuclei”. Physics of Atomic Nuclei 68 (7): 1133–1137. Bibcode: 2005PAN....68.1133D. doi:10.1134/1.1992567.
- ^ Schwerdtfeger, Peter; Pašteka, Lukáš F.; Punnett, Andrew; Bowman, Patrick O. (2015). “Relativistic and quantum electrodynamic effects in superheavy elements”. Nuclear Physics A 944 (December 2015): 551–577. Bibcode: 2015NuPhA.944..551S. doi:10.1016/j.nuclphysa.2015.02.005.
- ^ Dvorak, J.; Brüchle, W.; Chelnokov, M.; Dressler, R.; Düllmann, Ch. E.; Eberhardt, K.; Gorshkov, V.; Jäger, E. et al. (2006). “Doubly Magic Nucleus 108270Hs162”. Physical Review Letters 97 (24): 242501. Bibcode: 2006PhRvL..97x2501D. doi:10.1103/PhysRevLett.97.242501. PMID 17280272.
- ^ LaForge, Evan; Price, Will; Rafelski, Johann (15 September 2023). “Superheavy elements and ultradense matter”. The European Physical Journal Plus 138 (9): 812. arXiv:2306.11989. Bibcode: 2023EPJP..138..812L. doi:10.1140/epjp/s13360-023-04454-8.
- ^ “Physicists are pushing the periodic table to its limits | Science News”. (27 February 2019) 25 December 2023閲覧。
- ^ Dechargé, J.; Berger, J.-F.; Girod, M.; Dietrich, K. (March 2003). “Bubbles and semi-bubbles as a new kind of superheavy nuclei”. Nuclear Physics A 716: 55–86. Bibcode: 2003NuPhA.716...55D. doi:10.1016/S0375-9474(02)01398-2.
- ^ Agbemava, S. E.; Afanasjev, A. V. (25 March 2021). “Hyperheavy spherical and toroidal nuclei: The role of shell structure”. Physical Review C 103 (3): 034323. arXiv:2012.13799. Bibcode: 2021PhRvC.103c4323A. doi:10.1103/PhysRevC.103.034323.
- ^ Afanasjev, A.V.; Agbemava, S.E.; Gyawali, A. (July 2018). “Hyperheavy nuclei: Existence and stability”. Physics Letters B 782: 533–540. arXiv:1804.06395. Bibcode: 2018PhLB..782..533A. doi:10.1016/j.physletb.2018.05.070.
- ^ Palenzuela, Y. M.; Ruiz, L. F.; Karpov, A.; Greiner, W. (2012). “Systematic Study of Decay Properties of Heaviest Elements”. Bulletin of the Russian Academy of Sciences: Physics 76 (11): 1165–1171. Bibcode: 2012BRASP..76.1165P. doi:10.3103/S1062873812110172. ISSN 1062-8738.
- ^ Poenaru, Dorin N.; Gherghescu, R. A.; Greiner, W. (2012). “Cluster decay of superheavy nuclei”. Physical Review C 85 (3): 034615. Bibcode: 2012PhRvC..85c4615P. doi:10.1103/PhysRevC.85.034615 2 May 2017閲覧。.
- ^ a b c d van der Schoor, K. (2016). Electronic structure of element 123 (PDF) (Thesis). Rijksuniversiteit Groningen.
- ^ Indelicato, Paul; Bieroń, Jacek; Jönsson, Per (2011). “Are MCDF calculations 101% correct in the super-heavy elements range?”. Theoretical Chemistry Accounts 129 (3–5): 495–505. doi:10.1007/s00214-010-0887-3. hdl:2043/12984.
- ^ a b c d e f g h i j k l m n o p q r s t u v w x y z aa ab ac ad ae af ag ah ai aj ak al am an ao ap aq ar as at au av aw ax “Archived copy”. www.primefan.ru. 5 March 2016時点のオリジナルよりアーカイブ。15 January 2022閲覧。