XIAP
XIAP(X-linked inhibitor of apoptosis)、IAP3(inhibitor of apoptosis protein)またはBIRC4(baculoviral IAP repeat-containing protein 4)は、アポトーシスによる細胞死を停止するタンパク質である。ヒトでは、XIAPはX染色体に位置するXIAP遺伝子にコードされる[4][5]。
XIAPはアポトーシス阻害因子(IAP)ファミリーのタンパク質である。IAPは当初バキュロウイルスで同定され、XIAPは哺乳類に存在するその相同タンパク質の1つである[6]。XIAPはIAP1とIAP2との間ほど保存性は高くないため、ILP(IAP-like protein)とも呼ばれる[4][7]。XIAPは現在同定されているヒトのIAPの中で最も強力な作用を示す[8]。
発見
[編集]バキュロウイルスのIAPのホモログとしてヒトで最初に同定されたのはNAIPである[4]。NAIPの配列データをもとにして、RINGフィンガードメインを持つ遺伝子配列がXq24-25に発見された[4]。PCRとクローニングによって、タンパク質は3つのBIRドメインと1つのRINGフィンガードメインを持つことが発見され、X-linked Inhibitor of Apoptosis Protein(XIAP)として知られるようになった。XIAP遺伝子の転写産物の長さは9.0 kbであり、オープンリーディングフレームの長さは1.8 kbである[4]。XIAPのmRNAは末梢のリンパ球を除く成人と胎児の全ての組織に存在する[4]。XIAPの配列をもとにIAPファミリーの他のメンバーの発見がもたらされた。
構造
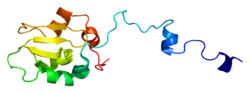
[編集]XIAPは3つの主要な構造エレメント(ドメイン)を持つ。1つ目は約70アミノ酸からなるBIRドメインであり、これは全てのIAPを特徴づけるものである[8]。2つ目はUBAドメインであり、XIAPのユビキチンへの結合を可能にする。3つ目はC末端RINGフィンガーとも呼ばれる亜鉛結合ドメインである[7]。XIAPは、N末端に3つのBIRドメイン、それに続いて1つのUBAドメイン、そして最後に1つのRINGドメインが存在する[9]。BIR1ドメインとBIR2ドメインの間にはリンカー領域が存在し、カスパーゼ分子と接触してXIAP/カスパーゼ-7複合体を形成することが確認されている[10]。溶液中では、全長型のXIAPは約114 kDaのホモ二量体を形成する[11]。
機能
[編集]XIAPは、ウイルス感染やカスパーゼの過剰産生によって誘導されたアポトーシスによる細胞死を停止させる。カスパーゼは細胞死に主要な役割を果たす酵素である[7]。XIAPはカスパーゼ-3、-7、-9に結合して阻害を行う[12]。XIAPのBIR2ドメインはカスパーゼ-3と-7を阻害し、BIR3はカスパーゼ-9に結合して阻害する[8]。RINGドメインはE3ユビキチンリガーゼ活性によって自身やカスパーゼ-3、-7へのユビキチン化を触媒し、プロテアソームによる分解をもたらす[13]。しかしながら、RINGフィンガーに影響を与える突然変異はアポトーシスに大きな影響を与えず、タンパク質の機能はBIRドメインで十分であることが示唆される[7]。カスパーゼ-3、-7の活性の阻害時には、XIAPのBIR2ドメインは活性部位の溝に結合し、アポトーシスをもたらす正常なタンパク質基質がここにアクセスすることを防いでいる[13][14]。
カスパーゼは、ミトコンドリアの機能異常時に細胞質基質に放出されるシトクロムcによって活性化される[7]。XIAPがシトクロムcに直接的に影響を与えることはないことが研究から示されている[7]。
XIAPは、TNF-α、Fas、紫外光、遺伝毒性物質による細胞死を効果的に防ぐことができる点でヒトの他のIAPとの差異がみられる[7]。
阻害
[編集]XIAPはDIABLO(Smac)とHTRA2(Omi)によって阻害される。この2つの細胞死シグナル伝達タンパク質はミトコンドリアから細胞質へ放出される[9]。XIAPの負の調節因子であるミトコンドリアタンパク質Smac/DIABLOは、XIAPに結合してXIAPのカスパーゼへの結合を防ぐことでアポトーシスを促進する。その結果、正常なカスパーゼ活性が進行する。Smac/DIABLOのXIAPへの結合とカスパーゼの放出には、保存された4ペプチドモチーフが必要である[13]。
臨床的意義
[編集]XIAPの調節異常はがん、神経変性疾患、自己免疫疾患を引き起こす場合がある[9]。XIAPの高値は腫瘍マーカーとして機能する可能性がある[8]。肺がん細胞NCI-H460では、XIAPの過剰発現はカスパーゼを阻害するだけでなく、シトクロムcの活性も停止させる。前立腺がんでは、XIAPは前立腺上皮で過剰発現している4つのIAPのうちの1つであり、効果的な治療には全てのIAPを阻害する分子が必要であることが示唆される[15]。IAPがショウジョウバエからヒトまで保存されていることからもわかるように、アポトーシスの調節は極めて重要な生物学的機能である[4]。
XIAP遺伝子の変異は重症で稀な型の炎症性腸疾患を引き起こす場合がある[16]。XIAP遺伝子の欠陥はX連鎖リンパ増殖症候群2型と呼ばれる極めて稀な疾患の原因となる場合もある[16][17][18]。
相互作用
[編集]XIAPは次に挙げる因子と相互作用することが示されている。
出典
[編集]- ^ a b c GRCm38: Ensembl release 89: ENSMUSG00000025860 - Ensembl, May 2017
- ^ Human PubMed Reference:
- ^ Mouse PubMed Reference:
- ^ a b c d e f g “Suppression of apoptosis in mammalian cells by NAIP and a related family of IAP genes”. Nature 379 (6563): 349–53. (January 1996). Bibcode: 1996Natur.379..349L. doi:10.1038/379349a0. PMID 8552191.
- ^ “A conserved family of cellular genes related to the baculovirus iap gene and encoding apoptosis inhibitors”. The EMBO Journal 15 (11): 2685–94. (June 1996). doi:10.1002/j.1460-2075.1996.tb00629.x. PMC 450204. PMID 8654366.
- ^ “Functional characterization of the X-linked inhibitor of apoptosis (XIAP) internal ribosome entry site element: role of La autoantigen in XIAP translation”. Molecular and Cellular Biology 20 (13): 4648–57. (July 2000). doi:10.1128/MCB.20.13.4648-4657.2000. PMC 85872. PMID 10848591.
- ^ a b c d e f g “Human IAP-like protein regulates programmed cell death downstream of Bcl-xL and cytochrome c”. Molecular and Cellular Biology 18 (1): 608–15. (January 1998). doi:10.1128/MCB.18.1.608. PMC 121528. PMID 9418907.
- ^ a b c d “IAP family proteins--suppressors of apoptosis”. Genes & Development 13 (3): 239–52. (February 1999). doi:10.1101/gad.13.3.239. PMID 9990849.
- ^ a b c “Upstream regulatory role for XIAP in receptor-mediated apoptosis”. Molecular and Cellular Biology 24 (16): 7003–14. (August 2004). doi:10.1128/MCB.24.16.7003-7014.2004. PMC 479745. PMID 15282301.
- ^ “Structural basis of caspase inhibition by XIAP: differential roles of the linker versus the BIR domain”. Cell 104 (5): 781–90. (March 2001). doi:10.1016/S0092-8674(01)00273-2. PMID 11257231.
- ^ “Conformational characterization of full-length X-chromosome-linked inhibitor of apoptosis protein (XIAP) through an integrated approach”. IUCrJ 6 (Pt 5): 948–957. (September 2019). doi:10.1107/S205225251901073X. PMC 6760453. PMID 31576227.
- ^ a b c “X-linked IAP is a direct inhibitor of cell-death proteases”. Nature 388 (6639): 300–4. (July 1997). Bibcode: 1997Natur.388..300D. doi:10.1038/40901. PMID 9230442.
- ^ a b c Gewies A (2003年). “Introduction to Apoptosis”. CellDeath.de. 2008年8月12日閲覧。
- ^ “Human inhibitor of apoptosis proteins: why XIAP is the black sheep of the family”. EMBO Reports 7 (10): 988–94. (October 2006). doi:10.1038/sj.embor.7400795. PMC 1618369. PMID 17016456.
- ^ “Targeting apoptosis in prostate cancer: focus on caspases and inhibitors of apoptosis proteins”. BJU International 96 Suppl 2: 30–4. (December 2005). doi:10.1111/j.1464-410X.2005.05944.x. PMID 16359436.
- ^ a b “Making a definitive diagnosis: successful clinical application of whole exome sequencing in a child with intractable inflammatory bowel disease”. Genetics in Medicine 13 (3): 255–62. (March 2011). doi:10.1097/GIM.0b013e3182088158. PMID 21173700.
- ^ “OMIM Entry - # 300635 - LYMPHOPROLIFERATIVE SYNDROME, X-LINKED, 2; XLP2” (英語). omim.org. 2021年7月17日閲覧。
- ^ “XIAP deficiency in humans causes an X-linked lymphoproliferative syndrome”. Nature 444 (7115): 110–4. (November 2006). Bibcode: 2006Natur.444..110R. doi:10.1038/nature05257. PMID 17080092.
- ^ a b “ILPIP, a novel anti-apoptotic protein that enhances XIAP-mediated activation of JNK1 and protection against apoptosis”. The Journal of Biological Chemistry 277 (34): 30454–62. (August 2002). doi:10.1074/jbc.M203312200. PMID 12048196.
- ^ a b “Structural basis for the inhibition of caspase-3 by XIAP”. Cell 104 (5): 791–800. (March 2001). doi:10.1016/S0092-8674(01)00274-4. PMID 11257232.
- ^ a b “The c-IAP-1 and c-IAP-2 proteins are direct inhibitors of specific caspases”. The EMBO Journal 16 (23): 6914–25. (December 1997). doi:10.1093/emboj/16.23.6914. PMC 1170295. PMID 9384571.
- ^ a b “X-linked inhibitor of apoptosis protein (XIAP) inhibits caspase-3 and -7 in distinct modes”. The Journal of Biological Chemistry 276 (29): 27058–63. (July 2001). doi:10.1074/jbc.M102415200. PMID 11359776.
- ^ “Ubiquitin-protein ligase activity of X-linked inhibitor of apoptosis protein promotes proteasomal degradation of caspase-3 and enhances its anti-apoptotic effect in Fas-induced cell death”. Proceedings of the National Academy of Sciences of the United States of America 98 (15): 8662–7. (July 2001). Bibcode: 2001PNAS...98.8662S. doi:10.1073/pnas.161506698. PMC 37492. PMID 11447297.
- ^ “The anti-apoptotic activity of XIAP is retained upon mutation of both the caspase 3- and caspase 9-interacting sites”. The Journal of Cell Biology 157 (1): 115–24. (April 2002). doi:10.1083/jcb.200108085. PMC 2173256. PMID 11927604.
- ^ “Towards a proteome-scale map of the human protein-protein interaction network”. Nature 437 (7062): 1173–8. (October 2005). Bibcode: 2005Natur.437.1173R. doi:10.1038/nature04209. PMID 16189514.
- ^ a b “Neuronal apoptosis-inhibitory protein does not interact with Smac and requires ATP to bind caspase-9”. The Journal of Biological Chemistry 279 (39): 40622–8. (September 2004). doi:10.1074/jbc.M405963200. PMID 15280366.
- ^ “IAPs block apoptotic events induced by caspase-8 and cytochrome c by direct inhibition of distinct caspases”. The EMBO Journal 17 (8): 2215–23. (April 1998). doi:10.1093/emboj/17.8.2215. PMC 1170566. PMID 9545235.
- ^ “Molecular cloning of ILP-2, a novel member of the inhibitor of apoptosis protein family”. Molecular and Cellular Biology 21 (13): 4292–301. (July 2001). doi:10.1128/MCB.21.13.4292-4301.2001. PMC 87089. PMID 11390657.
- ^ a b “HtrA2 promotes cell death through its serine protease activity and its ability to antagonize inhibitor of apoptosis proteins”. The Journal of Biological Chemistry 277 (1): 445–54. (January 2002). doi:10.1074/jbc.M109891200. PMID 11604410.
- ^ “A novel ubiquitin fusion system bypasses the mitochondria and generates biologically active Smac/DIABLO”. The Journal of Biological Chemistry 278 (9): 7494–9. (February 2003). doi:10.1074/jbc.C200695200. PMID 12511567.
- ^ “Direct interaction between survivin and Smac/DIABLO is essential for the anti-apoptotic activity of survivin during taxol-induced apoptosis”. The Journal of Biological Chemistry 278 (25): 23130–40. (June 2003). doi:10.1074/jbc.M300957200. PMID 12660240.
- ^ “Identification of DIABLO, a mammalian protein that promotes apoptosis by binding to and antagonizing IAP proteins”. Cell 102 (1): 43–53. (July 2000). doi:10.1016/S0092-8674(00)00009-X. PMID 10929712.
- ^ “The polypeptide chain-releasing factor GSPT1/eRF3 is proteolytically processed into an IAP-binding protein”. The Journal of Biological Chemistry 278 (40): 38699–706. (October 2003). doi:10.1074/jbc.M303179200. PMID 12865429.
- ^ “Neurotrophin receptor-interacting mage homologue is an inducible inhibitor of apoptosis protein-interacting protein that augments cell death”. The Journal of Biological Chemistry 276 (43): 39985–9. (October 2001). doi:10.1074/jbc.C100171200. PMID 11546791.
- ^ “XIAP regulates bi-phasic NF-kappaB induction involving physical interaction and ubiquitination of MEKK2”. Cellular Signalling 20 (11): 2107–12. (November 2008). doi:10.1016/j.cellsig.2008.08.004. PMID 18761086.
- ^ “XIAP, a cellular member of the inhibitor of apoptosis protein family, links the receptors to TAB1-TAK1 in the BMP signaling pathway”. The EMBO Journal 18 (1): 179–87. (January 1999). doi:10.1093/emboj/18.1.179. PMC 1171113. PMID 9878061.
- ^ “Identification of XAF1 as an antagonist of XIAP anti-Caspase activity”. Nature Cell Biology 3 (2): 128–33. (February 2001). doi:10.1038/35055027. PMID 11175744.
関連文献
[編集]- “Application of XIAP antisense to cancer and other proliferative disorders: development of AEG35156/ GEM640”. Annals of the New York Academy of Sciences 1058 (1): 215–34. (November 2005). Bibcode: 2005NYASA1058..215L. doi:10.1196/annals.1359.032. PMID 16394139.
- “Human inhibitor of apoptosis proteins: why XIAP is the black sheep of the family”. EMBO Reports 7 (10): 988–94. (October 2006). doi:10.1038/sj.embor.7400795. PMC 1618369. PMID 17016456.