ベンズアルデヒド
| ベンズアルデヒド | |
|---|---|
|
|
ベンズアルデヒド(許容慣用名) | |
ベンゼンカルバルデヒド | |
別称 フェニルメタナール ベンゼンカルボキサルデヒド ベンゼンアルデヒド | |
| 識別情報 | |
| CAS登録番号 | 100-52-7 |
| ChemSpider | 235 |
| KEGG | D02314 |
| |
| |
| 特性 | |
| 化学式 | C7H6O |
| モル質量 | 106.12 g mol−1 |
| 示性式 | C6H5CHO |
| 外観 | 無色液体 |
| 密度 | 1.0415 g/mL |
| 融点 |
−56.5 °C, 217 K, -70 °F ([1]) |
| 沸点 |
179 °C, 452 K, 354 °F ([1]) |
| 水への溶解度 | 難溶 (0.6 w/w%、20 ℃) |
| 屈折率 (nD) | 1.5456 (20 ℃, D)[1] |
| 粘度 | 1.4 cP (25 ℃) |
| 熱化学 | |
| 標準生成熱 ΔfH |
−86.8 kJ/mol |
| 標準燃焼熱 ΔcH |
−3525.1 kJ/mol |
| 危険性 | |
| EU分類 | Harmful (Xn) |
| NFPA 704 | |
| Rフレーズ | R22 |
| Sフレーズ | S2, S24 |
| 引火点 | 63 ℃ (Closed Cup) |
| 特記なき場合、データは常温 (25 °C)・常圧 (100 kPa) におけるものである。 | |
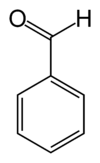
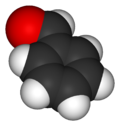
ベンズアルデヒド (benzaldehyde) は、芳香族アルデヒドに分類される有機化合物のひとつ。IUPAC系統名は、ベンゼンカルバルデヒド (benzenecarbaldehyde) 。ベンゼンの水素原子一つが、ホルミル基で置換された構造を持つ。
無色の液体。苦扁桃油(アーモンドの一種から取った薬用油)様の香気を持ち、揮発しやすい。芳香族アルデヒドは特異な臭いを有するものが多いが、ベンズアルデヒドはアーモンド、杏仁(アンズの種)の香り成分である。安価な香料として用いられるほか、抗炎症作用が認められている。酸化されやすく、酸化されると安息香酸になり、表面に膜状様物質として浮かぶ。
製法
[編集]トルエンを60%硫酸と二酸化マンガンによって穏やかに酸化することで得られる(酸化力が強い場合には安息香酸まで反応が進む)。ジクロロメチルベンゼン(塩化ベンザル)の加水分解によっても得られる。
1995年の実績では年間7000トンが生産され、大半は化学合成によるものであるが、天然品も100トンほど生産されている。ヤニタケ属のIschnoderma benzoinumにL-フェニルアラニンを添加し培養すると、培養液1リットルあたり1グラムのベンズアルデヒドと3-フェニル-1-プロパノールが生じる[2]。
反応
[編集]銀鏡反応に対しては陽性、フェーリング液に対しては陰性を示す。水酸化ナトリウムなどの強塩基とともに加熱すると、カニッツァーロ反応によりベンジルアルコールと安息香酸とに不均化する。触媒量のシアン化カリウムの存在下に加熱すると、ベンゾイン縮合によりベンゾイン(C6H5C(=O)CH(OH)C6H5)に変わる。
出典
[編集]- ^ a b c Merck Index 13th ed., 1057.
- ^ 井上重治『微生物と香り ミクロの世界のアロマの力』フレグランスジャーナル社、2002年8月1日、165頁。ISBN 4-89479-057-2。
外部リンク
[編集]- ベンズアルデヒド - 環境省

