レチナール
| 全トランス-レチナール | |
|---|---|

| |

| |
(2E,4E,6E,8E)-3,7-Dimethyl-9-(2,6,6-trimethylcyclohexen-1-yl)nona-2,4,6,8-tetraenal | |
別称
| |
| 識別情報 | |
| CAS登録番号 | 116-31-4 |
| PubChem | 638015 |
| ChemSpider | 553582 |
| UNII | RR725D715M |
| |
| |
| 特性 | |
| 化学式 | C20H28O |
| モル質量 | 284.44 g mol−1 |
| 外観 | 石油エーテルからのオレンジ色の結晶[1] |
| 融点 |
61 - 64 °C, 270 K, -22 °F [1] |
| 水への溶解度 | 溶けにくい |
| fatへの溶解度 | 可溶 |
| 関連する物質 | |
| 関連物質 | レチノール、レチノイン酸、β-カロテン、デヒドロレチナール、3-ヒドロキレチナール、4-ヒドロキレチナール |
| 特記なき場合、データは常温 (25 °C)・常圧 (100 kPa) におけるものである。 | |
レチナール(Retinal、レチンアルデヒドとも)は、ポリエンの発色団であり、オプシンと呼ばれるタンパク質に結合しており、動物の視覚の化学的基礎となる。
レチナールは、ある種の微生物が光を代謝エネルギーに変換することを可能にする。
ビタミンAには多くの形態があるが、その全てがレチナールに変換され、レチナールはビタミンAがなければ作ることができない。動物が摂取する際には、レチナール自身もビタミンAの1つの形態とみなされる。レチナールに変換できる異なる分子の数は生物種により異なる。レチナールはもともとレチネンと呼ばれていたが[2]、 ビタミンAアルデヒドであることが分かった後に改名された[3][4][5]。
脊椎動物は、肉から直接レチナールを摂取するか、カロテノイド(どちらもカロテンのα-カロテンまたはβ-カロテン)からレチナールを生成する。キサントフィルの一種であるβ-クリプトキサンチンからもレチナールが生成される。これらのカロテノイドは、植物などの光合成を行う生物から摂取しなければならない。他のカロテノイドを動物がレチナールに変換することはできない。肉食動物の中にはカロテノイドを全く変換することができない種もある。ビタミンAの他の主要な形態であるレチノールや部分的に活性のある形態のレチノイン酸は、いずれもレチナールから生成されることがある。
昆虫やイカなどの無脊椎動物は、他のキサントフィルから変換されたヒドロキシル化されたレチナールを視覚系に使用している。
ビタミンA代謝
[編集]生物は、カロテノイドの不可逆的な酸化的開裂によりレチナール(RAL)を生成する[6]。例えば、
- β-カロテン + O2 → 2 レチナール
これは、β-カロテン-15,15'-モノオキシゲナーゼ[7]またはβ-カロテン-15,15'-ジオキシゲナーゼにより触媒される[8]。カロテノイドがレチナールの前駆体であるように、レチナールは他の形態のビタミンAの前駆体である。レチナールは、ビタミンAの輸送及び貯蔵の形態であるレチノール(ROL)と相互変換が可能である。
これらの反応は、レチノールデヒドロゲナーゼ(RDHs)[9]及びアルコールデヒドロゲナーゼ(ADHs)により触媒される[10]。レチノールはビタミンAアルコールと呼ばれたり、単にビタミンAと呼ばれることも多い。レチノールは酸化されてレチノイン酸(RA)になることもある。
- レチナール + NAD+ + H2O → レチノイン酸 + NADH + H+ (RALDHにより触媒)
- レチノール + O2 + H2O → レチノイン酸 + H2O2 (レチノールデヒドロゲナーゼにより触媒)
これらの反応はレチンアルデヒドデヒドロゲナーゼ(RALDHs)[10]やレチナールオキシダーゼとしても知られるレチノールデヒドロゲナーゼ[11]により触媒される[12]。レチノイン酸は、ビタミンA酸と呼ばれることもあり、脊椎動物の重要なシグナル伝達分子であり、ホルモンでもある。
視覚
[編集]レチナールは、共役型の発色団である。ヒトの目においては、レチナールは、11-シス-レチナールの構成で始まり正しい波長の光子を取り込むと、まっすぐになり全-トランス-レチナールの構成になる。この構成の変化が網膜のオプシンタンパク質に押し付けられ、化学的なシグナル伝達カスケードが引き起こされ、結果としてヒトの脳が光や画像を認識する。発色団の吸光スペクトルは結合しているオプシンタンパク質との相互作用に依存するため、レチナール-オプシン複合体により異なる波長(すなわち、光の異なる色)の光子を吸収する。
オプシン
[編集]
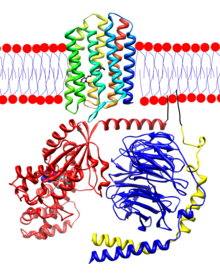
オプシンは、目の網膜にある視細胞に存在するタンパク質であり、レチナールに結合する視覚色素である。オプシンは、7つの膜貫通αヘリックスが6つのループで結ばれた束になっている。桿体細胞では、オプシン分子は細胞の内側にある円板膜に埋め込まれている。分子のN末端の頭部は、円板の内部に伸び、C末端の尾部は細胞の細胞質内に伸びている。錐体細胞では、円板は細胞膜により規定されているため、N末端の頭部は細胞の外側に伸びている。レチナールは、タンパク質のC末端に近い膜貫通ヘリックス上のリシンとシッフ塩基結合により共有結合する。シッフ塩基結合の形成には、レチナールから酸素原子が、リシンの遊離アミノ基から2つの水素原子が取り除かれH2Oが生じる。レチニリデンは、レチナールから酸素原子を取り除いてできた2価の官能基であり、ゆえにオプシンはレチニリデンタンパク質と呼ばれる。
オプシンは、典型的なGタンパク質共役受容体(GPCR)である[13]。ウシの桿体細胞のオプシンであるウシロドプシンは、初めてX線構造が決定されたGPCRである[14]。ウシロドプシンは、348個のアミノ酸残基を持つ。レチナール発色団はLys296に結合する。
哺乳類はオプシンの発色団としてレチノールのみを使用しているが、他の種類の動物はレチノールに近い他の4つの発色団(3,4-ジデヒドロレチナール (ビタミンA2), (3R)-3-ヒドロキシレチナール, (3S)-3-ヒドロキシレチナール (ともにビタミンA3), (4R)-4-ヒドロキシレチナール (ビタミンA4))を使用している。多くの魚類や両生類は3,4-ジデヒドロレチナール(デヒドロレチナールとも呼ばれる)を使用している。ハエ目の環縫類(いわゆる高等バエ)を除き、調べられたすべての昆虫は3-ヒドロキシレチナールの(R)-エナンチオマーを使用している。キサントフィルカロテノイドから直接3-ヒドロキシレチナールが作られる場合、(R)-エナンチオマーが予想される。ショウジョウバエなどの環縫類の虫は、(3S)-3-ヒドロキシレチナールを用いる[15][16]。ホタルイカは、(4R)-4-ヒドロキシレチナールを用いることが分かっている。
視覚サイクル
[編集]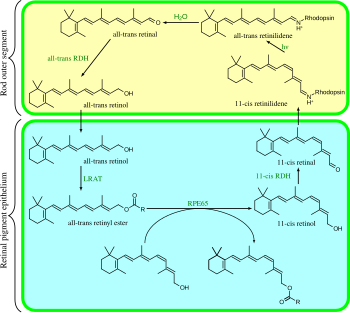
視覚サイクルは、光伝達の前段に位置する循環型の酵素経路である。これは11-cis-レチナールを再生する。例えば、哺乳類の桿体細胞の視覚サイクルは以下の通りである。
- 全トランスレチニルエステル + H2O → 11-シス-レチノール + 脂肪酸; RPE65 イソメロヒドロラーゼ[17]
- 11-シス-レチノール + NAD+ → 11-シス-レチナール + NADH + H+; 11-シス-レチノールデヒドロゲナーゼ
- 11-シス-レチナール + アポロドプシン → ロドプシン + H2O; リシン-CH=N+H-へのシッフ塩基結合を形成する
- ロドプシン + hν → メタロドプシン II, i.e. 11-シスが光異化し全トランスになる
- ロドプシン + hν → フォトロドプシン → バソロドプシン → ルミロドプシン → メタロドプシン I → メタロドプシン II,
- メタロドプシン II + H2O → アポロドプシン + 全トランスレチナール
- 全トランスレチナール + NADPH + H+ → 全トランスレチノール + NADP+; 全トランスレチノールのデヒドロゲナーゼ
- 全トランスレチノール + 脂肪酸 → 全トランスレチニルエステル + H2O; レシチンレチノールアシルトランスフェラーゼ(LRAT).[18]
ステップ3, 4, 5, 6は桿体細胞外層で、1, 2, 7は網膜色素上皮(RPE)細胞で起こる。
RPE65のイソメロヒドロラーゼは、β-カロテンモノオキシゲナーゼと相同である[6]。ショウジョウバエにおいて相同であるninaB酵素は、レチナール形成カロテノイドオキシゲナーゼ活性と全トランスから11-シスへのイソメラーゼ活性を併せ持つ[19]。
細菌ロドプシン
[編集]全-トランス-レチナールは、バクテリオロドプシン、チャネルロドプシン、ハロロドプシンなどの細菌のオプシンの不可欠な成分である。これらの分子においては、光により全-トランス-レチナールが13-シスレチナールに変化し、暗い状態では全-トランス-レチナールに戻るというサイクルを繰り返している。これらのタンパク質は、動物のオプシンとは進化的に関係がなくGPCRでもないため、両方ともレチナールを使用しているのは収斂進化の結果である[20]。
歴史
[編集]アメリカの生化学者ジョージ・ワルドらは、1958年までに視覚サイクルの概要を記述した。彼はこの研究により、ラグナー・グラニト、ハルダン・ケファー・ハートラインとともに1967年にノーベル生理学・医学賞を受賞した[21]。
関連項目
[編集]出典
[編集]- ^ a b Merck Index, 13th Edition, 8249
- ^ WALD, GEORGE (14 July 1934). “Carotenoids and the Vitamin A Cycle in Vision”. Nature 134 (3376): 65. Bibcode: 1934Natur.134...65W. doi:10.1038/134065a0.
- ^ Wald, G (11 October 1968). “Molecular basis of visual excitation.”. Science 162 (3850): 230–9. Bibcode: 1968Sci...162..230W. doi:10.1126/science.162.3850.230. PMID 4877437.
- ^ MORTON, R. A.; GOODWIN, T. W. (1 April 1944). “Preparation of Retinene in Vitro”. Nature 153 (3883): 405–406. Bibcode: 1944Natur.153..405M. doi:10.1038/153405a0.
- ^ BALL, S; GOODWIN, TW; MORTON, RA (1946). “Retinene1-vitamin A aldehyde.”. The Biochemical Journal 40 (5–6): lix. PMID 20341217.
- ^ a b von Lintig, Johannes; Vogt, Klaus (2000). “Filling the Gap in Vitamin A Research: Molecular Identification of An Enzyme Cleaving Beta-carotene to Retinal”. Journal of Biological Chemistry 275 (16): 11915–11920. doi:10.1074/jbc.275.16.11915. PMID 10766819.
- ^ Woggon, Wolf-D. (2002). “Oxidative cleavage of carotenoids catalyzed by enzyme models and beta-carotene 15,15´-monooxygenase”. Pure and Applied Chemistry 74 (8): 1397–1408. doi:10.1351/pac200274081397.
- ^ Kim, Yeong-Su; Kim, Nam-Hee; Yeom, Soo-Jin; Kim, Seon-Won; Oh, Deok-Kun (2009). “In Vitro Characterization of a Recombinant Blh Protein from an Uncultured Marine Bacterium as a β-Carotene 15,15′-Dioxygenase”. Journal of Biological Chemistry 284 (23): 15781–93. doi:10.1074/jbc.M109.002618. PMC 2708875. PMID 19366683.
- ^ Lidén, Martin; Eriksson, Ulf (2006). “Understanding Retinol Metabolism: Structure and Function of Retinol Dehydrogenases”. Journal of Biological Chemistry 281 (19): 13001–13004. doi:10.1074/jbc.R500027200. PMID 16428379.
- ^ a b Duester, G (September 2008). “Retinoic Acid Synthesis and Signaling during Early Organogenesis”. Cell 134 (6): 921–31. doi:10.1016/j.cell.2008.09.002. PMC 2632951. PMID 18805086.
- ^ Lin, Min; Zhang, Min; Abraham, Michael; Smith, Susan M.; Napoli, Joseph L. (2003). “Mouse Retinal Dehydrogenase 4 (RALDH4), Molecular Cloning, Cellular Expression, and Activity in 9-cis-Retinoic Acid Biosynthesis in Intact Cells”. Journal of Biological Chemistry 278 (11): 9856–9861. doi:10.1074/jbc.M211417200. PMID 12519776.
- ^ “KEGG ENZYME: 1.2.3.11 retinal oxidase”. 2009年3月10日閲覧。
- ^ Lamb, T D (1996). “Gain and kinetics of activation in the G-protein cascade of phototransduction”. Proceedings of the National Academy of Sciences 93 (2): 566–570. Bibcode: 1996PNAS...93..566L. doi:10.1073/pnas.93.2.566. PMC 40092. PMID 8570596.
- ^ Palczewski, Krzysztof; Kumasaka, Takashi; Hori, T; Behnke, CA; Motoshima, H; Fox, BA; Le Trong, I; Teller, DC et al. (2000). “Crystal Structure of Rhodopsin: A G Protein-Coupled Receptor”. Science 289 (5480): 739–745. Bibcode: 2000Sci...289..739P. doi:10.1126/science.289.5480.739. PMID 10926528.
- ^ Seki, Takaharu; Isono, Kunio; Ito, Masayoshi; Katsuta, Yuko (1994). “Flies in the Group Cyclorrhapha Use (3S)-3-Hydroxyretinal as a Unique Visual Pigment Chromophore”. European Journal of Biochemistry 226 (2): 691–696. doi:10.1111/j.1432-1033.1994.tb20097.x. PMID 8001586.
- ^ Seki, Takaharu; Isono, Kunio; Ozaki, Kaoru; Tsukahara, Yasuo; Shibata-Katsuta, Yuko; Ito, Masayoshi; Irie, Toshiaki; Katagiri, Masanao (1998). “The metabolic pathway of visual pigment chromophore formation in Drosophila melanogaster: All-trans (3S)-3-hydroxyretinal is formed from all-trans retinal via (3R)-3-hydroxyretinal in the dark”. European Journal of Biochemistry 257 (2): 522–527. doi:10.1046/j.1432-1327.1998.2570522.x. PMID 9826202.
- ^ Moiseyev, Gennadiy; Chen, Ying; Takahashi, Yusuke; Wu, Bill X.; Ma, Jian-xing (2005). “RPE65 is the isomerohydrolase in the retinoid visual cycle”. Proceedings of the National Academy of Sciences 102 (35): 12413–12418. Bibcode: 2005PNAS..10212413M. doi:10.1073/pnas.0503460102. PMC 1194921. PMID 16116091.
- ^ Jin, Minghao; Yuan, Quan; Li, Songhua; Travis, Gabriel H. (2007). “Role of LRAT on the Retinoid Isomerase Activity and Membrane Association of Rpe65”. Journal of Biological Chemistry 282 (29): 20915–20924. doi:10.1074/jbc.M701432200. PMC 2747659. PMID 17504753.
- ^ Oberhauser, Vitus; Voolstra, Olaf; Bangert, Annette; von Lintig, Johannes; Vogt, Klaus (2008). “NinaB combines carotenoid oxygenase and retinoid isomerase activity in a single polypeptide”. Proceedings of the National Academy of Sciences 105 (48): 19000–5. Bibcode: 2008PNAS..10519000O. doi:10.1073/pnas.0807805105. PMC 2596218. PMID 19020100.
- ^ Chen, De-Liang; Wang, Guang-yu; Xu, Bing; Hu, Kun-Sheng (2002). “All-trans to 13-cis retinal isomerization in light-adapted bacteriorhodopsin at acidic pH”. Journal of Photochemistry and Photobiology B: Biology 66 (3): 188–194. doi:10.1016/S1011-1344(02)00245-2. PMID 11960728.
- ^ 1967 Nobel Prize in Medicine
関連文献
[編集]- Prado-Cabrero, Alfonso; Scherzinger, Daniel; Avalos, Javier; Al-Babili, Salim (2007). “Retinal Biosynthesis in Fungi: Characterization of the Carotenoid Oxygenase CarX from Fusarium fujikuroi”. Eukaryotic Cell 6 (4): 650–657. doi:10.1128/EC.00392-06. PMC 1865656. PMID 17293483.
- Kloer, Daniel P.; Ruch, Sandra; Al-Babili, Salim; Beyer, Peter; Schulz, Georg E. (2005). “The Structure of a Retinal-Forming Carotenoid Oxygenase”. Science 308 (5719): 267–269. Bibcode: 2005Sci...308..267K. doi:10.1126/science.1108965. PMID 15821095.
- Schmidt, Holger; Kurtzer, Robert; Eisenreich, Wolfgang; Schwab, Wilfried (2006). “The Carotenase AtCCD1 from Arabidopsis thaliana Is a Dioxygenase”. Journal of Biological Chemistry 281 (15): 9845–9851. doi:10.1074/jbc.M511668200. PMID 16459333.
- Wang, Tao; Jiao, Yuchen; Montell, Craig (2007). “Dissection of the pathway required for generation of vitamin A and for Drosophila phototransduction”. Journal of Cell Biology 177 (2): 305–316. doi:10.1083/jcb.200610081. PMC 2064138. PMID 17452532.
- Wald, George (1967年). “Nobel Lecture: The Molecular Basis of Visual Excitation”. 2009年2月23日閲覧。
- Fernald, Russell D. (2006). “Casting a Genetic Light on the Evolution of Eyes”. Science 313 (5795): 1914–1918. Bibcode: 2006Sci...313.1914F. doi:10.1126/science.1127889. PMID 17008522.
- Briggs, Winslow R.; Spudich, John L., eds (2005). Handbook of Photosensory Receptors. Wiley. ISBN 978-3-527-31019-7
- Baylor, D A; Lamb, T D; Yau, K W (1979). “Responses of retinal rods to single photons”. Journal of Physiology 288: 613–634. doi:10.1113/jphysiol.1979.sp012716. PMC 1281447. PMID 112243.
- Hecht, Selig; Shlaer, Simon; Pirenne, Maurice Henri (1942). “Energy, Quanta, and Vision”. Journal of General Physiology 25 (6): 819–840. doi:10.1085/jgp.25.6.819. PMC 2142545. PMID 19873316.
- Barlow, H.B.; Levick, W.R.; Yoon, M. (1971). “Responses to single quanta of light in retinal ganglion cells of the cat”. Vision Research 11 (Supplement 3): 87–101. doi:10.1016/0042-6989(71)90033-2. PMID 5293890.
- Venter, J. Craig; Remington, K; Heidelberg, JF; Halpern, AL; Rusch, D; Eisen, JA; Wu, D; Paulsen, I et al. (2004). “Environmental Genome Shotgun Sequencing of the Sargasso Sea”. Science 304 (5667): 66–74. Bibcode: 2004Sci...304...66V. doi:10.1126/science.1093857. PMID 15001713. The oceans are full of type 1 rhodopsin.
- Waschuk, Stephen A.; Bezerra, Arandi G.; Shi, Lichi; Brown, Leonid S. (2005). “Leptosphaeria rhodopsin: Bacteriorhodopsin-like proton pump from a eukaryote”. Proceedings of the National Academy of Sciences 102 (19): 6879–6883. Bibcode: 2005PNAS..102.6879W. doi:10.1073/pnas.0409659102. PMC 1100770. PMID 15860584.
- Su, Chih-Ying; Luo, Dong-Gen; Terakita, Akihisa; Shichida, Yoshinori; Liao, Hsi-Wen; Kazmi, Manija A.; Sakmar, Thomas P.; Yau, King-Wai (2006). “Parietal-Eye Phototransduction Components and Their Potential Evolutionary Implications”. Science 311 (5767): 1617–1621. Bibcode: 2006Sci...311.1617S. doi:10.1126/science.1123802. PMID 16543463.
- Luo, Dong-Gen; Xue, Tian; Yau, King-Wai (2008). “How vision begins: An odyssey”. Proceedings of the National Academy of Sciences 105 (29): 9855–9862. Bibcode: 2008PNAS..105.9855L. doi:10.1073/pnas.0708405105. PMC 2481352. PMID 18632568. Good historical review.
- Schäfer, Günter; Engelhard, Martin; Müller, Volker (1999). “Bioenergetics of the Archaea”. Microbiology and Molecular Biology Reviews 63 (3): 570–620. doi:10.1128/MMBR.63.3.570-620.1999. PMC 103747. PMID 10477309.
- Fan, Jie; Woodruff, Michael L; Cilluffo, Marianne C; Crouch, Rosalie K; Fain, Gordon L (2005). “Opsin activation of transduction in the rods of dark-reared Rpe65 knockout mice”. Journal of Physiology 568 (1): 83–95. doi:10.1113/jphysiol.2005.091942. PMC 1474752. PMID 15994181.
- Sadekar, Sumedha; Raymond, Jason; Blankenship, Robert E. (2006). “Conservation of Distantly Related Membrane Proteins: Photosynthetic Reaction Centers Share a Common Structural Core”. Molecular Biology and Evolution 23 (11): 2001–2007. doi:10.1093/molbev/msl079. PMID 16887904.
- Yokoyama, Shozo; Radlwimmer, F. Bernhard (2001). “The molecular genetics and evolution of red and green color vision in vertebrates”. Genetics 158 (4): 1697–1710. PMC 1461741. PMID 11545071.
- Racker, Efraim; Stoeckenius, Walther (1974). “Reconstitution of Purple Membrane Vesicles Catalyzing Light-driven Proton Uptake and Adenosine Triphosphate Formation”. Journal of Biological Chemistry 249 (2): 662–663. doi:10.1016/S0021-9258(19)43080-9. PMID 4272126.
- Kawaguchi, Riki; Yu, Jiamei; Honda, Jane; Hu, Jane; Whitelegge, Julian; Ping, Peipei; Wiita, Patrick; Bok, Dean et al. (2007). “A Membrane Receptor for Retinol Binding Protein Mediates Cellular Uptake of Vitamin A”. Science 315 (5813): 820–825. Bibcode: 2007Sci...315..820K. doi:10.1126/science.1136244. PMID 17255476.
- Amora, Tabitha L.; Ramos, Lavoisier S.; Galan, Jhenny F.; Birge, Robert R. (2008). “Spectral Tuning of Deep Red Cone Pigments”. Biochemistry 47 (16): 4614–20. doi:10.1021/bi702069d. PMC 2492582. PMID 18370404.
- Send, Robert; Sundholm, Dage (2007). “Stairway to the conical intersection: A computational study of retinal isomerization”. Journal of Physical Chemistry A 111 (36): 8766–8773. Bibcode: 2007JPCA..111.8766S. doi:10.1021/jp073908l. PMID 17713894.
- Salom, David; Lodowski, David T.; Stenkamp, Ronald E.; Le Trong, Isolde; Golczak, Marcin; Jastrzebska, Beata; Harris, Tim; Ballesteros, Juan A. et al. (2006). “Crystal structure of a photoactivated deprotonated intermediate of rhodopsin”. Proceedings of the National Academy of Sciences 103 (44): 16123–16128. Bibcode: 2006PNAS..10316123S. doi:10.1073/pnas.0608022103. PMC 1637547. PMID 17060607.
外部リンク
[編集]- First Steps of Vision - National Health Museum
- Vision and Light-Induced Molecular Changes
- Retinal Anatomy and Visual Capacities
- Retinal
