Fas受容体
Fas受容体(Fasじゅようたい、英: Fas receptor、Fas、FasR)は、ヒトではFAS遺伝子にコードされるタンパク質であり、APO-1(apoptosis antigen 1、APT)、CD95(cluster of differentiation 95)、TNFRSF6(tumor necrosis factor receptor superfamily member 6)という名称でも知られる[5][6]。Fasはヒト線維芽細胞株FS-7によって免疫化を行ったマウスによって産生されたモノクローナル抗体を用いて最初に同定された。そのため、Fasという名称はFS-7-associated surface antigenの略称に由来する[7]。
Fas受容体は細胞表面に位置する細胞死受容体であり、そのリガンドであるFasリガンド(FasL)が結合した場合にプログラム細胞死(アポトーシス)をもたらす。この経路は2つのアポトーシス経路のうちの1つであり、もう1つはミトコンドリアを介した経路である[8]。
遺伝子
[編集]Fas受容体をコードする遺伝子は、ヒトでは10番染色体の長腕(10q24.1)、マウスでは19番染色体に位置する。ヒトの遺伝子は+鎖に位置し、長さは25,255塩基対で、タンパク質をコードする9つのエクソンからなる構成をしている。進化的に関連した類似の配列(オルソログ)は、大部分の哺乳類に存在している[9]。
タンパク質
[編集]8種類のスプライスバリアントが同定されており、7種類のアイソフォームへと翻訳される。アポトーシスを誘導するFas受容体がアイソフォーム1とされており、I型膜貫通タンパク質である。他のアイソフォームの多くは稀なハプロタイプであり、多くの場合は疾患と関係している。アポトーシスを誘導する膜貫通型アイソフォームと可溶型アイソフォームは正常な産物であり、選択的スプライシングによるこれらのアイソフォームの産生は細胞毒性を有するRNA結合タンパク質TIA1によって調節される[10]。
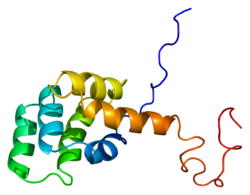
成熟型Fasタンパク質は319アミノ酸からなり、48 kDaと予測され、細胞外ドメイン、膜貫通ドメイン、細胞質ドメインの3つのドメインに分けられる。細胞外ドメインは157アミノ酸からなり、システイン残基に富む。膜貫通ドメインと細胞質ドメインはそれぞれ17アミノ酸、145アミノ酸からなる。エクソン1からエクソン5が細胞外領域をコードする。エクソン6は膜貫通領域、エクソン7からエクソン9は細胞内領域をコードする。
機能
[編集]Fasはリガンドの結合に伴って細胞死誘導性シグナル伝達複合体(death-inducing signaling complex、DISC)を形成する。隣接する細胞の表面の膜に固定されたFasリガンド三量体は、Fasのオリゴマー化を引き起こす。DISC中では、最大5分子から7分子のFasがオリゴマー化することが示唆されている[11]。
その後のデスドメイン(DD)の凝集に伴って、受容体複合体は細胞のエンドソーム装置を介してインターナリゼーションされる。その結果、アダプター分子であるFADDは自身のDDを介してFasのDDに結合できるようになる[12]。
FADDのN末端近傍にはデスエフェクタードメイン(DED)も存在し[13]、カスパーゼ-8(FLICE)のDEDへの結合を促進する。その後、カスパーゼ-8はp10サブユニットとp18サブユニットへの切断によって自身を活性化し、これら2つのサブユニットは活性型のヘテロ四量体酵素を形成する。活性型のカスパーゼ-8はDISCから細胞質基質へ放出されて他のエフェクターカスパーゼを切断し、最終的にはDNAの分解、膜のブレブの形成やその他アポトーシスの顕著な特徴が引き起こされる。
発がんプログレッションの過程でFasは高頻度でダウンレギュレーションされるか、細胞はアポトーシス抵抗性を獲得するが、Fasは腫瘍の成長を促進することも示されている。Fasはアポトーシス感受性をもたらすにもかかわらず、がん細胞は一般的にFasの構成的活性に依存しており、がんが産生するFasリガンドによって刺激されている[14]。
マウスモデルではこうしたFasの腫瘍成長促進が示されているが、ヒトのがんゲノミクスデータベースの解析では、FASは3131の腫瘍のデータセットで有意な局所的増幅はみられず、有意な局所的欠失がみられることから[15]、ヒトではがん抑制因子として機能していることが示唆される。
培養細胞では、FasリガンドはFas受容体を介してさまざまな種類のがん細胞でアポトーシスを誘導する。AOM/DSS誘発性結腸がんやMCA誘発性肉腫のマウスモデルでは、Fasががん抑制因子として作用することが示されている[16]。さらに、Fas受容体は腫瘍特異的細胞傷害性T細胞(CTL)による抗腫瘍細胞傷害も媒介する[17]。よく知られた標的に対するCTLの抗腫瘍細胞傷害に加えて、Fasは標的抗原を発現していない(バイスタンダー)細胞に対しても腫瘍細胞死を誘導する別の機能を持つとされる。CTLを介したバイスタンダー細胞死は1986年に報告され[18]、その後Fasを介した細胞溶解が原因であることがin vitroで示された[19]。また、二重特異性抗体を用いたin vitroでの研究や[20]、T細胞とCAR-T細胞を用いたin vivoでの研究でもFasを介したバイスタンダー腫瘍細胞の細胞死が実証されている[21]。
相互作用
[編集]FASは次に挙げる因子と相互作用することが示されている。
- CASP8[22][23][24]
- CASP10[25]
- CFLAR[23][24]
- FADD[22][23][26][27][28][29]
- FASLG[22][30][31][32]
- PDCD6[33]
- SUMO1[34][35]
出典
[編集]- ^ a b c GRCh38: Ensembl release 89: ENSG00000026103 - Ensembl, May 2017
- ^ a b c GRCm38: Ensembl release 89: ENSMUSG00000024778 - Ensembl, May 2017
- ^ Human PubMed Reference:
- ^ Mouse PubMed Reference:
- ^ “The human APO-1 (APT) antigen maps to 10q23, a region that is syntenic with mouse chromosome 19”. Genomics 14 (1): 179–80. (September 1992). doi:10.1016/S0888-7543(05)80302-7. PMID 1385299.
- ^ “Assignment of the human Fas antigen gene (Fas) to 10q24.1”. Genomics 14 (3): 821–2. (November 1992). doi:10.1016/S0888-7543(05)80200-9. PMID 1385309.
- ^ “Early work on the function of CD95, an interview with Shige Nagata”. Cell Death and Differentiation 11 Suppl 1 (Suppl 1): S23-7. (July 2004). doi:10.1038/sj.cdd.4401453. PMID 15143352.
- ^ “The Fas signaling pathway: more than a paradigm”. Science 296 (5573): 1635–6. (May 2002). Bibcode: 2002Sci...296.1635W. doi:10.1126/science.1071553. PMID 12040174.
- ^ “ENSG00000026103_FAS”. orthomam.mbb.cnrs.fr. 2021年11月13日閲覧。
- ^ “Regulation of Fas alternative splicing by antagonistic effects of TIA-1 and PTB on exon definition”. Molecular Cell 19 (4): 475–84. (August 2005). doi:10.1016/j.molcel.2005.06.015. PMID 16109372.
- ^ “The Fas-FADD death domain complex structure reveals the basis of DISC assembly and disease mutations”. Nature Structural & Molecular Biology 17 (11): 1324–9. (November 2010). doi:10.1038/nsmb.1920. PMC 2988912. PMID 20935634.
- ^ “NMR structure and mutagenesis of the Fas (APO-1/CD95) death domain”. Nature 384 (6610): 638–41. (1996). Bibcode: 1996Natur.384..638H. doi:10.1038/384638a0. PMID 8967952.
- ^ “NMR structure and mutagenesis of the FADD (Mort1) death-effector domain”. Nature 392 (6679): 941–5. (April 1998). Bibcode: 1998Natur.392..941E. doi:10.1038/31972. PMID 9582077.
- ^ “CD95 promotes tumour growth”. Nature 465 (7297): 492–6. (May 2010). Bibcode: 2010Natur.465..492C. doi:10.1038/nature09075. PMC 2879093. PMID 20505730.
- ^ “Tumorscape”. The Broad Institute. 2012年4月14日時点のオリジナルよりアーカイブ。2012年7月5日閲覧。
- ^ “NF-κB directly regulates Fas transcription to modulate Fas-mediated apoptosis and tumor suppression”. The Journal of Biological Chemistry 287 (30): 25530–40. (July 2012). doi:10.1074/jbc.M112.356279. PMC 3408167. PMID 22669972.
- ^ “Decitabine and vorinostat cooperate to sensitize colon carcinoma cells to Fas ligand-induced apoptosis in vitro and tumor suppression in vivo”. Journal of Immunology 188 (9): 4441–9. (May 2012). doi:10.4049/jimmunol.1103035. PMC 3398838. PMID 22461695.
- ^ “Lysis of bystander target cells after triggering of human cytotoxic T lymphocytes”. European Journal of Immunology 16 (8): 1021–4. (August 1986). doi:10.1002/eji.1830160826. PMID 3488908.
- ^ “Fas ligand-mediated lysis of self bystander targets by human papillomavirus-specific CD8+ cytotoxic T lymphocytes”. Journal of Virology 72 (7): 5948–54. (July 1998). doi:10.1128/JVI.72.7.5948-5954.1998. PMC 110399. PMID 9621057.
- ^ “Bispecific T cell engager (BiTE®) antibody constructs can mediate bystander tumor cell killing”. PLOS ONE 12 (8): e0183390. (2017-08-24). Bibcode: 2017PLoSO..1283390R. doi:10.1371/journal.pone.0183390. PMC 5570333. PMID 28837681.
- ^ “A critical role for fas-mediated off-target tumor killing in T cell immunotherapy”. Cancer Discovery 11 (3): 599–613. (December 2020). doi:10.1158/2159-8290.CD-20-0756. PMC 7933082. PMID 33334730.
- ^ a b c “Cytoskeleton-mediated death receptor and ligand concentration in lipid rafts forms apoptosis-promoting clusters in cancer chemotherapy”. The Journal of Biological Chemistry 280 (12): 11641–7. (March 2005). doi:10.1074/jbc.M411781200. PMID 15659383.
- ^ a b c “Identification and molecular cloning of two novel receptors for the cytotoxic ligand TRAIL”. The Journal of Biological Chemistry 272 (41): 25417–20. (October 1997). doi:10.1074/jbc.272.41.25417. PMID 9325248.
- ^ a b “Casper is a FADD- and caspase-related inducer of apoptosis”. Immunity 6 (6): 751–63. (June 1997). doi:10.1016/S1074-7613(00)80450-1. PMID 9208847.
- ^ “Fas-associated death domain protein interleukin-1beta-converting enzyme 2 (FLICE2), an ICE/Ced-3 homologue, is proximally involved in CD95- and p55-mediated death signaling”. The Journal of Biological Chemistry 272 (10): 6578–83. (March 1997). doi:10.1074/jbc.272.10.6578. PMID 9045686.
- ^ “The receptor for the cytotoxic ligand TRAIL”. Science 276 (5309): 111–3. (April 1997). doi:10.1126/science.276.5309.111. PMID 9082980.
- ^ “NMR structure and mutagenesis of the Fas (APO-1/CD95) death domain”. Nature 384 (6610): 638–41. (1996). Bibcode: 1996Natur.384..638H. doi:10.1038/384638a0. PMID 8967952.
- ^ “FADD, a novel death domain-containing protein, interacts with the death domain of Fas and initiates apoptosis”. Cell 81 (4): 505–12. (May 1995). doi:10.1016/0092-8674(95)90071-3. PMID 7538907.
- ^ “Regulation of Fas-associated death domain interactions by the death effector domain identified by a modified reverse two-hybrid screen”. The Journal of Biological Chemistry 277 (37): 34343–8. (September 2002). doi:10.1074/jbc.M204169200. PMID 12107169.
- ^ “Induction of TNF receptor I-mediated apoptosis via two sequential signaling complexes”. Cell 114 (2): 181–90. (July 2003). doi:10.1016/S0092-8674(03)00521-X. PMID 12887920.
- ^ “Identification of amino acid residues important for ligand binding to Fas”. The Journal of Experimental Medicine 185 (8): 1487–92. (April 1997). doi:10.1084/jem.185.8.1487. PMC 2196280. PMID 9126929.
- ^ “Characterization of Fas (Apo-1, CD95)-Fas ligand interaction”. The Journal of Biological Chemistry 272 (30): 18827–33. (July 1997). doi:10.1074/jbc.272.30.18827. PMID 9228058.
- ^ “Apoptosis-linked gene 2 binds to the death domain of Fas and dissociates from Fas during Fas-mediated apoptosis in Jurkat cells”. Biochemical and Biophysical Research Communications 288 (2): 420–6. (October 2001). doi:10.1006/bbrc.2001.5769. PMID 11606059.
- ^ “Protection against Fas/APO-1- and tumor necrosis factor-mediated cell death by a novel protein, sentrin”. Journal of Immunology 157 (10): 4277–81. (November 1996). PMID 8906799.
- ^ “Interaction of Daxx, a Fas binding protein, with sentrin and Ubc9”. Biochemical and Biophysical Research Communications 279 (1): 6–10. (December 2000). doi:10.1006/bbrc.2000.3882. PMID 11112409.
関連文献
[編集]- “Apoptosis by death factor”. Cell 88 (3): 355–65. (February 1997). doi:10.1016/S0092-8674(00)81874-7. PMID 9039262.
- “Soluble Fas/Apo-1 splicing variants and apoptosis”. Frontiers in Bioscience 1 (4): d12-8. (January 1996). doi:10.2741/A112. PMID 9159204.
- “Bruton's tyrosine kinase (BTK) as a dual-function regulator of apoptosis”. Biochemical Pharmacology 56 (6): 683–91. (September 1998). doi:10.1016/S0006-2952(98)00122-1. PMID 9751072.
- “CD95's deadly mission in the immune system”. Nature 407 (6805): 789–95. (October 2000). Bibcode: 2000Natur.407..789K. doi:10.1038/35037728. PMID 11048730.
- “The multifaceted role of Fas signaling in immune cell homeostasis and autoimmunity”. Nature Immunology 1 (6): 469–74. (December 2000). doi:10.1038/82712. PMID 11101867.
- “Death receptor Fas and autoimmune disease: from the original generation to therapeutic application of agonistic anti-Fas monoclonal antibody”. Cytokine & Growth Factor Reviews 13 (4–5): 393–402. (2003). doi:10.1016/S1359-6101(02)00024-2. PMID 12220552.
- “Fas ligand/Fas system in the brain: regulator of immune and apoptotic responses”. Brain Research. Brain Research Reviews 44 (1): 65–81. (January 2004). doi:10.1016/j.brainresrev.2003.08.007. PMID 14739003.
- “Development of lymphoma in Autoimmune Lymphoproliferative Syndrome (ALPS) and its relationship to Fas gene mutations”. Leukemia & Lymphoma 45 (3): 423–31. (March 2004). doi:10.1080/10428190310001593166. PMID 15160902.
外部リンク
[編集]- FAS Receptor - MeSH・アメリカ国立医学図書館・生命科学用語シソーラス
- Overview of all the structural information available in the PDB for UniProt: P25445 (Human Tumor necrosis factor receptor superfamily member 6) at the PDBe-KB.
- Overview of all the structural information available in the PDB for UniProt: P25446 (Mouse Tumor necrosis factor receptor superfamily member 6) at the PDBe-KB.