Alu要素
Alu要素(Aluようそ、英: Alu element)とは、ヒトをはじめとする霊長類のゲノムに見られる遺伝因子の一つである。Alu配列とも[1]。Arthrobacter luteus (Alu) の制限エンドヌクレアーゼ活性により最初に特徴づけられた[2]。
Alu要素は最も頻繁にみられるトランスポゾンであり、ヒトゲノム全体では100万以上のコピーが散在する[3]。その機能として自己複製のみが知られているため、Aluは利己的または寄生的なDNAであると考えられてきた。しかし、進化において役割を果たしている可能性が高く、遺伝的マーカーとしても使用されている[4][5]。Alu 要素はシグナル認識粒子の成分である、小さな細胞質7SL RNAに由来する。Alu要素は霊長類ゲノム間で高度に保存されており、超霊長類の祖先のゲノムに起源を発する[6]。
Alu要素の挿入は、いくつかの遺伝性の人間の病気やさまざまな形態のがんと関連がある[要出典]。
Alu要素についての研究は、ヒトの集団遺伝学上および人類を含む霊長類の進化の解明上も重要である[要出典]。
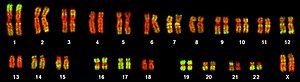
Aluファミリー
[編集]Aluファミリーはヒトを含む霊長類のゲノム上に見られる反復配列要素である[7]。現代のAlu要素は長さ300塩基対ほどで、反復配列要素の中でも短鎖散在核要素 (SINE) に分類される。典型的には 5′- Part A - A5TACA6 - Part B - PolyA Tail - 3′ の構造をとる。ここで、Part AとPart B("left arm"〈左腕〉および "right arm"〈右腕〉とも)は類似したヌクレオチド配列である。現代のAlu要素は類似するものの異なるfossil antique monomer (FAM) のhead to tail融合により発生したと考えられており、そのため似た別々のモノマー("left arm" と "right arm")がAリッチなリンカーにより結合された二量体構造をとる。どちらのモノマーもシグナル認識粒子RNA、別名7SL RNAから進化したと考えられている[8]。ポリA尾部の長さは、Aluファミリーによって異なる。
ヒトゲノム全体には100万を超えるAlu要素が散在しており、ヒトゲノムの約10.7%がAlu配列からなると推定されている。しかし、遺伝的多形をもつものは0.5%以下である[9]。1988年、イェジ・ユルカとテンプル・スミスによりAlu要素がAluJ(Jurkaにちなむ)とAluS(Smithにちなむ)と呼ばれる2つの主要なサブファミリーに分けられることが発見され、いくつかのグループによって独立に別の複数のサブファミリーも発見された[10]。その後、活動中のAlu要素を含むAluSのサブサブファミリーはAluYと名付けられた。AluJ系統は6500万年前まで遡り、ヒトゲノムの中で最も古くかつ最も活動性が低い。比較的新しいAluS系統はおよそ3000万年前のもので、まだいくつか活動中の要素を含む。AluY要素はこれら3つの中で最も新しく、ヒトゲノム中を移動する傾向が最も高い[11]。Aluサブファミリーの発見されたことでマスター/ソース遺伝子仮説につながり、転移可能要素(活動的要素)と散在反復配列(活動的要素の変異コピー)との間の明確なつながりが提供された[12]。
関連要素
[編集]ラットとマウスにみられるB1要素は、7SL RNAから進化したという点でAlu要素と類似するが、left armモノマー1つのみを持つ。ヒトにみられるAlu要素の95%はチンパンジーにもみられ、マウスにみられるB要素の50%はラットにも見られる。これらの要素は主に遺伝子のイントロン中および上流の調節要素中にみられる[13]。
AluとB1の祖先形式はfossil antique monomer (FAM) と呼ばれる。Left armとright armそれぞれの自由浮動形態が存在し、それぞれfree left Alu monomer (FLAM) およびfree right Alu monomer (FRAM) と呼ばれる[14]。霊長類が持つFLAMのひとつ、BC200 lncRNAは注目に値する。
配列の特徴
[編集]
Alu要素には、2つの主要プロモーター「ボックス」、すなわち共通配列TGGCTCACGCCを持つ5′Aボックス、および共通配列GTTCGAGAC(IUPAC核酸表記法)を持つ3′Bボックスがある。RNAポリメラーゼIIIにより転写されるtRNAには、類似するもののより強力なプロモーター構造がある[15]。これらの両方がleft armに存在する[8]。
Alu要素の内部プロモーター領域には、4か所もしくはそれ以下のレチノイン酸応答要素六量体部位があり、最後の1つは「Bボックス」と重なる[16]。以下に例示する7SL (SRP) RNAでは、機能する六量体に実線で下線が、機能しない3番目の六量体に点線で下線を引いてある。
GCCGGGCGCGGTGGCGCGTGCCTGTAGTCCCAGCTACTCGGGAGGCTGAGGCTGGAGGATCGCTTGAGTCCAGGAGTTCTGGGCTGTAGTGCGCTATGCCGATCGGAATAGCCACTGCACTCCAGCCTGGGCAACATAGCGAGACCCCGTCTC
Alu Iエンドヌクレアーゼの認識配列は5 ′ ag/ct 3′、すなわち上例中の小文字で示された配列のグアニン残基とシトシン残基の間でDNAを切断する[17]。
Alu要素
[編集]Alu要素は、遺伝子の組織固有的調節を担っている。また、近傍遺伝子の転写にも関与しており、遺伝子の発現方法を変える場合がある[18]。
Alu要素はレトロトランスポゾンであり、RNAポリメラーゼIIIによってコードされるRNAから作られたDNAコピーのように見える。Alu要素はタンパク質をコードせず、他のDNA配列と同じように複製されるが、新しい要素の生成はLINEレトロトランスポゾンに依存する[19]。
Alu要素の複製および移動の最初の段階は、新たに翻訳されたタンパク質が最終目的地に到達するのを助けるシグナル認識粒子 (SRP) との相互作用である[20]。Alu RNAは、SRP9およびSRP14からなるタンパク質ヘテロダイマーと共にRNA:タンパク質複合体を形成する。SRP9/14の媒介によりAluは新生L1タンパク質を捕捉するリボソームに付着する。そして、Alu要素によりL1タンパク質の逆転写酵素が乗っ取られ、L1 mRNAのかわりにAlu RNA配列がゲノム上にコピーされる[11]。
霊長類において、Alu要素は解読が比較的容易な遺伝的化石記録を形成する。この理由は、Alu要素の挿入事象により、読みやすくかつ世代を超えてゲノムに忠実に記録される特徴的な兆候が残されるためである。Alu Y要素は進化した年代が最も浅いため、これを研究することにより詳細な祖先関係を明らかすることができる[要出典]。これは、Alu要素の挿入が100万年に100から200回の低頻度でしか発生せず、削除機構が発見されていないことによる。したがって、ある要素を持つ複数の個体は共通の祖先の子孫である可能性が高く、要素がない場合はその逆がいえる。そのため、遺伝学で人間の進化を研究する上で、最近挿入されたAlu要素の有無は人類の進化を研究する際に考慮すべき良い特性であるかもしれない[21]。
ほとんどのヒトAlu要素は他の霊長類のゲノムでも対応する位置にみられるが、約7000個のAluは人間に固有である[22]。
ヒトにおけるAluの影響
[編集]Alu要素は遺伝子発現に影響を与えることが提唱されており、ステロイドホルモン受容体の機能的プロモーター領域を含むことが知られている[16][23]。Alu要素にはメチル化の部位として機能するCpGジヌクレオチドが豊富に含まれており、これらの領域がヒトゲノムのメチル化サイトの最大30%を構成する[24]。Alu要素は、ヒトにおける突然変異の原因となることも多いが、そのような突然変異はpre-mRNAの非コード領域(イントロン)に限られていることが多く、保有者に目に見える影響を与えることはほぼない[25]。イントロン(もしくはノンコーディングRNA領域)に起こる変異は、個体のゲノムのコーディング領域に変異が含まれていない場合、個体の表現型にほとんどあるいはまったく影響を与えない。人体に有害である可能性があるのは、スプライシング処理後にコーディング領域(エクソン)またはmRNAに挿入される Alu挿入である[26]。
ただし、生成された変異は、人類集団の移動および祖先の研究に使用でき[27]、 Alu[28]およびレトロトランスポゾン一般の変異原性作用[29]は、近年におけるヒトゲノム進化に大きな役割を果たしている[要出典]。Alu挿入または削除がおよぼすヒトへの影響が数多く知られている。
人間の病気との関連
[編集]Alu挿入は時として破壊的であり、遺伝性疾患を引き起こす可能性がある。ただし、ほとんどのAlu変異は疾患と分離するマーカーとして機能するため[訳語疑問点]、特定のAluアレルの保有者が確実に疾患に罹患するとは限らない。Aluが媒介する組み換えにより頻度の高いがんの遺伝的素因が生じていることは、遺伝性非ポリポーシス大腸癌に関して1995年に初めて報告されている[30]。ヒトゲノムにおいて、近年でも活動が見られるのは22 個のAluYおよび6個のAluSであり、これらにより様々ながんに繋がる遺伝的影響が生じうる。このように大きな遺伝性損傷が生じうるため、Aluの転移活動に影響を与える原因の理解が重要視されている[31]。
以下にAlu挿入との関連が知られているヒト疾患を挙げる[27][32]。
また、以下に挙げる疾患は、転写レベルに影響を与えるAlu要素の1塩基変異に関連することが知られている。
Alu関連のヒト遺伝子変異
[編集]アンジオテンシン変換酵素をコードするACE遺伝子には、Aluが挿入されているもの (ACE-I) とAluが削除されているもの (ACE-D) の2つの一般的な変異型がある。Alu要素が存在することにより、持久力志向の競技(トライアスロンなど)でのパフォーマンスの向上する傾向が指摘されている[34]。
ヒトを含む旧世界ザルにおける3色型色覚の再獲得をもたらしたオプシン遺伝子の重複に隣接してAlu要素が存在し、3色型色覚の進化においてAluが役割を果たしたことを示唆している[35]。
参考文献
[編集]- ^ “Alu配列”. J-GLOBAL 科学技術用語情報. 科学技術振興機構. 2020年6月12日閲覧。
- ^ Schmid, Carl W; Deininger, Prescott L (1975). “Sequence organization of the human genome”. Cell 6 (3): 345–58. doi:10.1016/0092-8674(75)90184-1. PMID 1052772.
- ^ Szmulewicz, Martin N; Novick, Gabriel E; Herrera, Rene J (1998). “Effects of Alu insertions on gene function”. Electrophoresis 19 (8–9): 1260–4. doi:10.1002/elps.1150190806. PMID 9694261.
- ^ Kidwell, Margaret G; Lisch, Damon R (2001). “Perspective: Transposable Elements, Parasitic Dna, and Genome Evolution”. Evolution 55 (1): 1–24. doi:10.1554/0014-3820(2001)055[0001:ptepda]2.0.co;2. PMID 11263730.
- ^ Pray (2008年). “Functions and Utility of Alu Jumping Genes”. Scitable.com. Nature. 26 June 2019閲覧。
- ^ Kriegs, Jan Ole; Churakov, Gennady; Jurka, Jerzy; Brosius, Jürgen; Schmitz, Jürgen (2007). “Evolutionary history of 7SL RNA-derived SINEs in Supraprimates”. Trends in Genetics 23 (4): 158–61. doi:10.1016/j.tig.2007.02.002. PMID 17307271.
- ^ Arcot, Santosh S.; Wang, Zhenyuan; Weber, James L.; Deininger, Prescott L.; Batzer, Mark A. (September 1995). “Alu Repeats: A Source for the Genesis of Primate Microsatellites”. Genomics 29 (1): 136–144. doi:10.1006/geno.1995.1224. ISSN 0888-7543. PMID 8530063.
- ^ a b Häsler, Julien; Strub, Katharina (2006). “Alu elements as regulators of gene expression”. Nucleic Acids Research 34 (19): 5491–7. doi:10.1093/nar/gkl706. PMC 1636486. PMID 17020921.
- ^ Roy-Engel, A. M; Carroll, M. L; Vogel, E; Garber, R. K; Nguyen, S. V; Salem, A. H; Batzer, M. A; Deininger, P. L (2001). “Alu insertion polymorphisms for the study of human genomic diversity”. Genetics 159 (1): 279–90. PMC 1461783. PMID 11560904.
- ^ Jurka, J; Smith, T (1988). “A fundamental division in the Alu family of repeated sequences”. Proceedings of the National Academy of Sciences 85 (13): 4775–8. Bibcode: 1988PNAS...85.4775J. doi:10.1073/pnas.85.13.4775. PMC 280518. PMID 3387438.
- ^ a b Bennett, E. A; Keller, H; Mills, R. E; Schmidt, S; Moran, J. V; Weichenrieder, O; Devine, S. E (2008). “Active Alu retrotransposons in the human genome”. Genome Research 18 (12): 1875–83. doi:10.1101/gr.081737.108. PMC 2593586. PMID 18836035.
- ^ Richard Shen, M; Batzer, Mark A; Deininger, Prescott L (1991). “Evolution of the master Alu gene(s)”. Journal of Molecular Evolution 33 (4): 311–20. Bibcode: 1991JMolE..33..311R. doi:10.1007/bf02102862. PMID 1774786.
- ^ Tsirigos, Aristotelis; Rigoutsos, Isidore; Stormo, Gary D. (18 December 2009). “Alu and B1 Repeats Have Been Selectively Retained in the Upstream and Intronic Regions of Genes of Specific Functional Classes”. PLOS Computational Biology 5 (12): e1000610. doi:10.1371/journal.pcbi.1000610. PMC 2784220. PMID 20019790.
- ^ Kojima, K. K. (16 August 2010). “Alu Monomer Revisited: Recent Generation of Alu Monomers”. Molecular Biology and Evolution 28 (1): 13–15. doi:10.1093/molbev/msq218. PMID 20713470.
- ^ Conti, A; Carnevali, D; Bollati, V; Fustinoni, S; Pellegrini, M; Dieci, G (January 2015). “Identification of RNA polymerase III-transcribed Alu loci by computational screening of RNA-Seq data.”. Nucleic Acids Research 43 (2): 817–35. doi:10.1093/nar/gku1361. PMC 4333407. PMID 25550429.
- ^ a b Vansant, G; Reynolds, W. F (1995). “The consensus sequence of a major Alu subfamily contains a functional retinoic acid response element”. Proceedings of the National Academy of Sciences 92 (18): 8229–33. Bibcode: 1995PNAS...92.8229V. doi:10.1073/pnas.92.18.8229. PMC 41130. PMID 7667273.
- ^ Ullu E, Tschudi C (1984). “Alu sequences are processed 7SL RNA genes”. Nature 312 (5990): 171–2. Bibcode: 1984Natur.312..171U. doi:10.1038/312171a0. PMID 6209580.
- ^ Britten, R. J (1996). “DNA sequence insertion and evolutionary variation in gene regulation”. Proceedings of the National Academy of Sciences of the United States of America 93 (18): 9374–7. Bibcode: 1996PNAS...93.9374B. doi:10.1073/pnas.93.18.9374. PMC 38434. PMID 8790336.
- ^ Kramerov, D; Vassetzky, N (2005). “Short Retroposons in Eukaryotic Genomes”. International Review of Cytology 247: 165–221. doi:10.1016/S0074-7696(05)47004-7. PMID 16344113.
- ^ Weichenrieder, Oliver; Wild, Klemens; Strub, Katharina; Cusack, Stephen (2000). “Structure and assembly of the Alu domain of the mammalian signal recognition particle”. Nature 408 (6809): 167–73. Bibcode: 2000Natur.408..167W. doi:10.1038/35041507. PMID 11089964.
- ^ Terreros, Maria C.; Alfonso-Sanchez, Miguel A.; Novick; Luis; Lacau; Lowery; Regueiro; Herrera (September 11, 2009). “Insights on human evolution: an analysis of Alu insertion polymorphisms”. Journal of Human Genetics 54 (10): 603–611. doi:10.1038/jhg.2009.86. PMID 19745832.
- ^ Chimpanzee Sequencing Analysis Consortium (2005). “Initial sequence of the chimpanzee genome and comparison with the human genome”. Nature 437 (7055): 69–87. Bibcode: 2005Natur.437...69.. doi:10.1038/nature04072. PMID 16136131.
- ^ Norris, J; Fan, D; Aleman, C; Marks, J. R; Futreal, P. A; Wiseman, R. W; Iglehart, J. D; Deininger, P. L et al. (1995). “Identification of a new subclass of Alu DNA repeats that can function as estrogen receptor-dependent transcriptional enhancers”. The Journal of Biological Chemistry 270 (39): 22777–82. doi:10.1074/jbc.270.39.22777. PMID 7559405.
- ^ Schmid, C. W (1998). “Does SINE evolution preclude Alu function?”. Nucleic Acids Research 26 (20): 4541–50. doi:10.1093/nar/26.20.4541. PMC 147893. PMID 9753719.
- ^ Lander, Eric S; Linton, Lauren M; Birren, Bruce; Nusbaum, Chad; Zody, Michael C; Baldwin, Jennifer; Devon, Keri; Dewar, Ken et al. (2001). “Initial sequencing and analysis of the human genome”. Nature 409 (6822): 860–921. Bibcode: 2001Natur.409..860L. doi:10.1038/35057062. PMID 11237011.
- ^ Deininger, Prescott L; Batzer, Mark A (1999). “Alu Repeats and Human Disease”. Molecular Genetics and Metabolism 67 (3): 183–93. doi:10.1006/mgme.1999.2864. PMID 10381326.
- ^ a b Batzer, Mark A; Deininger, Prescott L (2002). “Alu Repeats and Human Genomic Diversity”. Nature Reviews Genetics 3 (5): 370–9. doi:10.1038/nrg798. PMID 11988762.
- ^ Shen, S; Lin, L; Cai, J. J; Jiang, P; Kenkel, E. J; Stroik, M. R; Sato, S; Davidson, B. L et al. (2011). “Widespread establishment and regulatory impact of Alu exons in human genes”. Proceedings of the National Academy of Sciences 108 (7): 2837–42. Bibcode: 2011PNAS..108.2837S. doi:10.1073/pnas.1012834108. PMC 3041063. PMID 21282640.
- ^ Cordaux, Richard; Batzer, Mark A (2009). “The impact of retrotransposons on human genome evolution”. Nature Reviews Genetics 10 (10): 691–703. doi:10.1038/nrg2640. PMC 2884099. PMID 19763152.
- ^ Nyström-Lahti, Minna; Kristo, Paula; Nicolaides, Nicholas C; Chang, Sheng-Yung; Aaltonen, Lauri A; Moisio, Anu-Liisa; Järvinen, Heikki J; Mecklin, Jukka-Pekka et al. (1995). “Founding mutations and Alu-mediated recombination in hereditary colon cancer”. Nature Medicine 1 (11): 1203–6. doi:10.1038/nm1195-1203. PMID 7584997.
- ^ Jin, Lingling; McQuillan, Ian; Li, Longhai (2017). “Computational identification of harmful mutation regions to the activity of transposable elements”. BMC Genomics 18 (Suppl 9): 862. doi:10.1186/s12864-017-4227-z. PMC 5773891. PMID 29219079.
- ^ Deininger, Prescott (2011). “Alu elements: Know the SINEs”. Genome Biology 12 (12): 236. doi:10.1186/gb-2011-12-12-236. PMC 3334610. PMID 22204421.
- ^ Fukuda, Shinichi; Varshney, Akhil; Fowler, Benjamin J.; Wang, Shao-bin; Narendran, Siddharth; Ambati, Kameshwari; Yasuma, Tetsuhiro; Magagnoli, Joseph et al. (2021-02-09). “Cytoplasmic synthesis of endogenous Alu complementary DNA via reverse transcription and implications in age-related macular degeneration” (英語). Proceedings of the National Academy of Sciences 118 (6): e2022751118. Bibcode: 2021PNAS..11822751F. doi:10.1073/pnas.2022751118. ISSN 0027-8424. PMC 8017980. PMID 33526699.
- ^ Puthucheary, Zudin; Skipworth, James R.A; Rawal, Jai; Loosemore, Mike; Van Someren, Ken; Montgomery, Hugh E (2011). “The ACE Gene and Human Performance”. Sports Medicine 41 (6): 433–48. doi:10.2165/11588720-000000000-00000. PMID 21615186.
- ^ Dulai, K. S; von Dornum, M; Mollon, J. D; Hunt, D. M (1999). “The evolution of trichromatic color vision by opsin gene duplication in New World and Old World primates”. Genome Research 9 (7): 629–38. doi:10.1101/gr.9.7.629. PMID 10413401.
外部リンク
[編集]- Alu Repetitive Sequences - MeSH・アメリカ国立医学図書館・生命科学用語シソーラス
- “NCBI Genbank DNA encoding 7SL RNA”. National Center for Biotechnology Information. (2018-05-12).
