HNF1A
HNF1A(hepatocyte nuclear factor 1 homeobox A)は、ヒトでは12番染色体に位置するHNF1A遺伝子によってコードされる転写因子である[5][6][7]。HNF1Aは多くの組織や細胞種において普遍的に発現している[8]。HNF1Aは肝臓で高度に発現している転写因子であり、いくつかの肝特異的遺伝子の発現調節に関与している[9]。HNF1A遺伝子の変異は糖尿病の原因となることが知られている[10]。また、HNF1A遺伝子には冠動脈疾患のリスクの増加と関係する27のSNPのうちの1つが含まれる[11]。
構造
[編集]遺伝子
[編集]HNF1A遺伝子は12番染色体のバンド12q24.2に位置し、10個のエクソンを持つ[7][12]。この遺伝子からは、選択的スプライシングによって8種類のアイソフォームが産生される[13]。
タンパク質
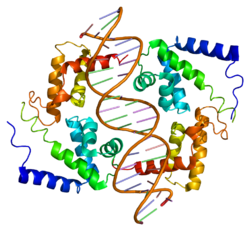
[編集]HNF1Aタンパク質はHNF1ホメオボックスファミリーに属する。N末端の二量体化ドメイン(1–32番残基)、非典型的POUホメオドメインを含む二分節型DNA結合ドメイン(98–280番残基)、C末端のトランス活性化ドメイン(281–631番残基)の3つの機能的ドメインを持つ[14][15]。また、二量体化ドメインとDNA結合ドメインを連結する柔軟なリンカー領域(33–97番残基)も存在する[15]。結晶構造はいくつか解かれており、二量体化ドメインはターン構造で隔てられた2つのαヘリックスが二量体化することで4ヘリックスバンドルを形成している。DNA結合モチーフはヘリックスターンヘリックスを形成しており、モチーフには3本のαヘリックスからなるPOUホメオドメインが含まれている。このホメオドメインは、典型的ホメオドメインフォールドと比較して、2番目と3番目のヘリックスの間に伸長したループが挿入された非典型的構造をしている。この非典型的挿入部は相互作用面を安定化して転写効率を改善していると考えられている[14]。二量体化ドメインはホモまたはヘテロ二量体化を担う。形成された二量体にはαヘリックス1と1′からなる固い「ミニジッパー」構造が含まれ、αヘリックス2と2′からなる柔軟なC末端部分とは非典型的な強固なターン構造で連結されている[15]。
機能
[編集]HNF1Aは肝臓、腎臓、膵臓、腸、胃、脾臓、胸腺、精巣、皮膚のケラチノサイトやメラノサイトで発現している転写因子である[16]。腸管上皮細胞の成長や細胞系統の分化に影響を与えることが示されている。また、HNF1Aは成熟B細胞形成における重要な細胞内因性転写因子である[17][18][19]。グルコース代謝や糖尿病に対するHNF1Aの関与も報告されており、膵臓β細胞におけるグルコーストランスポーターGLUT1やGLUT2の発現や、膵島におけるACE2の発現に関与している[20][21]。HNF1Aは、DPP-4(CD26)など2型糖尿病の管理に関与するいくつかのタンパク質の転写を促進する[22][23]。HNF1Aは他の器官においてもさまざまな代謝経路に関与しており、腸や腎臓では胆汁酸トランスポーターの転写調節因子である[24]。HNF1Aは肝臓の有機カチオントランスポーターの促進に関与しており、これらは特定の種類の薬剤の取り込みを担うため、その機能の喪失は薬物代謝の問題を引き起こす場合がある[25]。さらに、HNF1Aはフィブリノゲン、C反応性タンパク、IL-1受容体など炎症に関与する急性期タンパク質の発現を調節する[26]。膵臓腫瘍や肝細胞腺腫では、正常な隣接組織と比較してHNF1Aの発現レベルが有意に低いことが観察されており、HNF1Aが腫瘍の抑制に関与している可能性が示唆されている[27][28]。
臨床的意義
[編集]HNF1Aの変異は、「単一遺伝子糖尿病」の1種である若年発症成人型糖尿病3型(MODY3)[6]や肝細胞腺腫の原因となる場合がある。HNF1タンパク質は卵巣の明細胞がんにも存在する[29][30]。
ヒトでは、HNF1Aの変異は低用量スルホニル尿素薬応答性の糖尿病を引き起こす[31]。HNF1Aのヘテロ接合型変異を原因とする糖尿病患者でみられる極度のスルホニル尿素感受性は、糖尿病患者におけるHNF1Aの重要性を示すとともに、患者管理に遺伝薬理学がいかに寄与するかの明確な例となっている[32]。HNF1Aの変異を原因とするMODYの患者(30歳以下の糖尿病診断症例の約3%を占める)はスルホニル尿素薬治療に対して極めて高い感受性を示し、インスリン治療から移行できる[10]。HNF1A変異を原因とする糖尿病の患者はスルホニル尿素薬の血糖降下作用に対する感受性が高いことが記録されており、これは血糖降下薬に対する応答の変化が原因のようである。この効果はHNF1A欠乏モデルと一致しており、高血糖患者の管理における遺伝的基礎の重要性を示唆している[10]。HNF1Aに広くみられる遺伝的多様性も2型糖尿病発症のリスクや若年発症型糖尿病の浸透度の増加と関係している[33]。
臨床マーカー
[編集]多遺伝子座による遺伝的リスクスコア研究では、HNF1A遺伝子を含む27の遺伝子座の組み合わせに基づいて、冠動脈疾患イベントの発生と再発のリスクの高い人物の特定が行われており、高リスク群ではスタチン治療の臨床的有効性が最も大きいことが示されている。この研究はコミュニティコホート研究(the Malmo Diet and Cancer study)と、一次予防コホート(JUPITER、ASCOT)と二次予防コホート(CARE、PROVE IT-TIMI 22)の4つのランダム化比較試験に基づいたものである[11]。
相互作用
[編集]HNF1Aは次に挙げる因子と相互作用することが示されている。
出典
[編集]- ^ a b c GRCh38: Ensembl release 89: ENSG00000135100 - Ensembl, May 2017
- ^ a b c GRCm38: Ensembl release 89: ENSMUSG00000029556 - Ensembl, May 2017
- ^ Human PubMed Reference:
- ^ Mouse PubMed Reference:
- ^ “Chromosomal localization in man and rat of the genes encoding the liver-enriched transcription factors C/EBP, DBP, and HNF1/LFB-1 (CEBP, DBP, and transcription factor 1, TCF1, respectively) and of the hepatocyte growth factor/scatter factor gene (HGF)”. Genomics 13 (2): 293–300. (June 1992). doi:10.1016/0888-7543(92)90245-N. PMID 1535333.
- ^ a b “A gene for maturity onset diabetes of the young (MODY) maps to chromosome 12q”. Nature Genetics 9 (4): 418–23. (April 1995). doi:10.1038/ng0495-418. PMID 7795649.
- ^ a b “HNF1A HNF1 homeobox A [Homo sapiens (human) - Gene - NCBI]”. www.ncbi.nlm.nih.gov. 2016年10月11日閲覧。
- ^ “BioGPS - your Gene Portal System”. biogps.org. 2016年10月11日閲覧。
- ^ “Interaction of a liver-specific nuclear factor with the fibrinogen and alpha 1-antitrypsin promoters”. Science 238 (4827): 688–92. (October 1987). Bibcode: 1987Sci...238..688C. doi:10.1126/science.3499668. PMID 3499668.
- ^ a b c “Genetic cause of hyperglycaemia and response to treatment in diabetes”. Lancet 362 (9392): 1275–81. (October 2003). doi:10.1016/S0140-6736(03)14571-0. PMID 14575972.
- ^ a b “Genetic risk, coronary heart disease events, and the clinical benefit of statin therapy: an analysis of primary and secondary prevention trials”. Lancet 385 (9984): 2264–71. (June 2015). doi:10.1016/S0140-6736(14)61730-X. PMC 4608367. PMID 25748612.
- ^ “Homo sapiens HNF1 homeobox A (HNF1A), RefSeqGene (LRG_522) on chromosome 12”. 2023年9月20日閲覧。
- ^ “HNF1A - Hepatocyte nuclear factor 1-alpha - Homo sapiens (Human) - HNF1A gene & protein”. www.uniprot.org. 2016年10月11日閲覧。
- ^ a b “Diabetes mutations delineate an atypical POU domain in HNF-1alpha”. Molecular Cell 10 (5): 1129–37. (November 2002). doi:10.1016/s1097-2765(02)00704-9. PMID 12453420.
- ^ a b c “Diabetes mellitus due to misfolding of a beta-cell transcription factor: stereospecific frustration of a Schellman motif in HNF-1alpha”. Journal of Molecular Biology 362 (3): 414–29. (September 2006). doi:10.1016/j.jmb.2006.06.086. PMID 16930618.
- ^ “Berry Phenolic Compounds Increase Expression of Hepatocyte Nuclear Factor-1α (HNF-1α) in Caco-2 and Normal Colon Cells Due to High Affinities with Transcription and Dimerization Domains of HNF-1α”. PLOS ONE 10 (9): e0138768. (2015-01-01). Bibcode: 2015PLoSO..1038768R. doi:10.1371/journal.pone.0138768. PMC 4587667. PMID 26413797.
- ^ “Loss of hepatocyte-nuclear-factor-1alpha impacts on adult mouse intestinal epithelial cell growth and cell lineages differentiation”. PLOS ONE 5 (8): e12378. (2010-01-01). Bibcode: 2010PLoSO...512378L. doi:10.1371/journal.pone.0012378. PMC 2927538. PMID 20808783.
- ^ “Hepatocyte nuclear factor 1alpha and beta control terminal differentiation and cell fate commitment in the gut epithelium”. Development 137 (9): 1573–82. (May 2010). doi:10.1242/dev.044420. PMID 20388655.
- ^ “Hepatocyte Nuclear Factor 1A Is a Cell-Intrinsic Transcription Factor Required for B Cell Differentiation and Development in Mice”. Journal of Immunology 196 (4): 1655–65. (February 2016). doi:10.4049/jimmunol.1500897. PMID 26800876.
- ^ “Computational modeling of glucose transport in pancreatic β-cells identifies metabolic thresholds and therapeutic targets in diabetes”. PLOS ONE 7 (12): e53130. (2012-01-01). Bibcode: 2012PLoSO...753130L. doi:10.1371/journal.pone.0053130. PMC 3531366. PMID 23300881.
- ^ “The transcription factor HNF1α induces expression of angiotensin-converting enzyme 2 (ACE2) in pancreatic islets from evolutionarily conserved promoter motifs”. Biochimica et Biophysica Acta (BBA) - Gene Regulatory Mechanisms 1829 (11): 1225–35. (November 2013). doi:10.1016/j.bbagrm.2013.09.007. PMC 3838857. PMID 24100303.
- ^ “Mutant HNF-1alpha and mutant HNF-1beta identified in MODY3 and MODY5 downregulate DPP-IV gene expression in Caco-2 cells”. Biochemical and Biophysical Research Communications 346 (3): 1016–23. (August 2006). doi:10.1016/j.bbrc.2006.06.010. PMID 16781669.
- ^ “Glucose regulation of dipeptidyl peptidase IV gene expression is mediated by hepatocyte nuclear factor-1alpha in epithelial intestinal cells”. Clinical and Experimental Pharmacology & Physiology 35 (12): 1433–9. (December 2008). doi:10.1111/j.1440-1681.2008.05015.x. PMID 18671716.
- ^ “Hepatocyte nuclear factor-1alpha is an essential regulator of bile acid and plasma cholesterol metabolism”. Nature Genetics 27 (4): 375–82. (April 2001). doi:10.1038/86871. PMID 11279518.
- ^ “Hepatocyte nuclear factor 1 regulates the expression of the organic cation transporter 1 via binding to an evolutionary conserved region in intron 1 of the OCT1 gene”. The Journal of Pharmacology and Experimental Therapeutics 347 (1): 181–92. (October 2013). doi:10.1124/jpet.113.206359. PMC 3781413. PMID 23922447.
- ^ “Hepatic nuclear factor 1-alpha: inflammation, genetics, and atherosclerosis”. Current Opinion in Lipidology 20 (2): 106–11. (April 2009). doi:10.1097/mol.0b013e3283295ee9. PMID 19280766.
- ^ “Hepatocyte nuclear factor 1A (HNF1A) as a possible tumor suppressor in pancreatic cancer”. PLOS ONE 10 (3): e0121082. (2015-01-01). Bibcode: 2015PLoSO..1021082L. doi:10.1371/journal.pone.0121082. PMC 4368635. PMID 25793983.
- ^ “Bi-allelic inactivation of TCF1 in hepatic adenomas”. Nature Genetics 32 (2): 312–5. (October 2002). doi:10.1038/ng1001. PMID 12355088.
- ^ “A limited panel of immunomarkers can reliably distinguish between clear cell and high-grade serous carcinoma of the ovary”. The American Journal of Surgical Pathology 33 (1): 14–21. (January 2009). doi:10.1097/PAS.0b013e3181788546. PMID 18830127.
- ^ “Clear cell carcinoma of the female genital tract (not everything is as clear as it seems)”. Advances in Anatomic Pathology 19 (5): 296–312. (September 2012). doi:10.1097/PAP.0b013e31826663b1. PMID 22885379.
- ^ “Treating young adults with type 2 diabetes or monogenic diabetes”. Best Practice & Research. Clinical Endocrinology & Metabolism 30 (3): 455–67. (June 2016). doi:10.1016/j.beem.2016.05.002. PMID 27432078.
- ^ “Pharmacogenomics in diabetes mellitus: insights into drug action and drug discovery”. Nature Reviews. Endocrinology 12 (6): 337–46. (June 2016). doi:10.1038/nrendo.2016.51. PMID 27062931.
- ^ Locke, Jonathan M.; Saint-Martin, Cécile; Laver, Thomas W.; Patel, Kashyap A.; Wood, Andrew R.; Sharp, Seth A.; Ellard, Sian; Bellanné-Chantelot, Christine et al. (2018-09). “The Common HNF1A Variant I27L Is a Modifier of Age at Diabetes Diagnosis in Individuals With HNF1A-MODY”. Diabetes 67 (9): 1903–1907. doi:10.2337/db18-0133. ISSN 1939-327X. PMC 6109380. PMID 29895593.
- ^ a b c d “Transcriptional activation by hepatocyte nuclear factor-1 requires synergism between multiple coactivator proteins”. The Journal of Biological Chemistry 275 (17): 12515–20. (April 2000). doi:10.1074/jbc.275.17.12515. PMID 10777539.
- ^ “Hepatocyte nuclear factor-1alpha recruits the transcriptional co-activator p300 on the GLUT2 gene promoter”. Diabetes 51 (5): 1409–18. (May 2002). doi:10.2337/diabetes.51.5.1409. PMID 11978637.
- ^ “Large-scale mapping of human protein-protein interactions by mass spectrometry”. Molecular Systems Biology 3: 89. (2007). doi:10.1038/msb4100134. PMC 1847948. PMID 17353931.
- ^ “The bifunctional DCOH protein binds to HNF1 independently of its 4-alpha-carbinolamine dehydratase activity”. Nucleic Acids Research 25 (8): 1476–84. (April 1997). doi:10.1093/nar/25.8.1476. PMC 146627. PMID 9092652.
関連文献
[編集]- “Regulation of LEF-1/TCF transcription factors by Wnt and other signals”. Current Opinion in Cell Biology 11 (2): 233–40. (April 1999). doi:10.1016/S0955-0674(99)80031-3. PMID 10209158.
- “Genotype phenotype classification of hepatocellular adenoma”. World Journal of Gastroenterology 13 (19): 2649–54. (May 2007). doi:10.3748/wjg.v13.i19.2649. PMC 4147112. PMID 17569132.