シアノ水素化ホウ素ナトリウム
表示
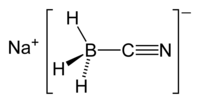
| シアノ水素化ホウ素ナトリウム | |
|---|---|
| |
別称 ナトリウムシアノボロヒドリドシアノトリヒドリドホウ酸ナトリウム | |
| 識別情報 | |
| CAS登録番号 | 25895-60-7 |
| PubChem | 24849595 |
| EC番号 | 247-317-2 |
| 特性 | |
| 化学式 | NaBH3CN |
| モル質量 | 62.84 g/mol |
| 外観 | 白色粉末 |
| 密度 | 1.20 g/cm3 |
| 融点 |
241 ℃(分解) |
| 水への溶解度 | 可溶、反応 |
| 危険性 | |
| 安全データシート(外部リンク) | MSDS |
| NFPA 704 | |
| 特記なき場合、データは常温 (25 °C)・常圧 (100 kPa) におけるものである。 | |
シアノ水素化ホウ素ナトリウム(シアノすいそかほうそナトリウム、sodium cyanoborohydride)は、化学式が NaBH3CN と表される無機化合物。無色の塩で、有機合成化学においてイミンの還元に用いられる。
合成と利用
[編集]シアノ水素化ホウ素ナトリウムを合成するためには、ボランとシアン化ナトリウムを反応させるか、もしくは水素化ホウ素ナトリウムとシアン化水銀(II)を反応させる。電子求引基であるシアノ基を持つことから、 アニオンの求核性は アニオンよりも弱められている[1]。
シアノ水素化ホウ素ナトリウムはイミンをアミンへと還元する穏和な還元剤である。アルデヒドやケトンのようなカルボニル化合物と、1級アミンとを共存させてシアノ水素化ホウ素ナトリウムを作用させると、脱水縮合により系中で発生するイミンが還元されることで、2級アミンが得られる。アンモニアを用いると同様に1級アミンが得られる。pH 7-10 の弱塩基性条件では反応が選択的に進み、還元的アミノ化反応として利用される。
この還元反応は Borch反応として知られる[2]。
シアノ水素化ホウ素ナトリウムは水と反応して分解するが、その速度は遅いため還元反応の溶媒として水系を用いることもできる[3]。環状アセタールの水素化分解にも用いられる。
脚注
[編集]- ^ Baxter, E. W.; Reitz, A. B. Reductive Aminations of Carbonyl Compounds with Borohydride and Borane Reducing Agents in Organic Reactions, 2002, John Wiley and Sons. doi:10.1002/0471264180.or059.01
- ^ Borch, R. F.; Bernstein, M. D.; Durst, H. D. (1971). “Cyanohydridoborate Anion as a Selective Reducing Agent”. J. Am. Chem. Soc. 93 (12): 2897–2904. doi:10.1021/ja00741a013.
- ^ Beard, T. M; Turner, N. J. (2002). “Deracemisation and Stereoinversion of alpha-Amino Acids Using D-Amino Acid Oxidase and Hydride Reducing Agents”. Chem. Commun. (3): 246–247.


![{\displaystyle {\ce {[B(CN)H3]^-}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/0735d2e2353a02250b424eb56913c774d7ede533)
![{\displaystyle {\ce {[BH4]^-}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/869b819686a0036078cf1c62426a9588305e026e)
![{\displaystyle {\ce {R^1C(=O)R^2\ + R-NH2 ->\ [R^1C(=NR)R^2]}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/7bd8981b9082faa8f8adcd6b15a240a336c76b3d)
![{\displaystyle {\ce {[R^1C(=NR)R^2]\ + NaBH3CN ->\ [R^1CH(-NHR)R^2]}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/25c4c8ad12d3d1eac7b96c3c8d7eb9b90c0a43b4)