四ヨウ化ゲルマニウム
表示
| 四ヨウ化ゲルマニウム | |
|---|---|
| |
| 識別情報 | |
| CAS登録番号 | 13450-95-8 |
| PubChem | 83479 |
| ChemSpider | 75317 |
| EC番号 | 236-613-7 |
| |
| |
| 特性 | |
| 化学式 | GeI4 |
| モル質量 | 580.26 g mol−1 |
| 外観 | 赤色結晶[1] (温度によって色が変わる)[2] |
| 密度 | 4.32 g·cm−3 |
| 融点 |
146 °C (419 K)[1] |
| 溶解度 | 二硫化炭素、クロロホルム、ベンゼン等、非極性溶媒に可溶[3] |
| 危険性 | |
| GHSピクトグラム | 
|
| GHSシグナルワード | 危険(DANGER) |
| Hフレーズ | H314 |
| Pフレーズ | P260, P264, P264+265, P280, P301+330+331, P302+361+354, P304+340, P305+354+338, P316, P317, P321, P363, P405, P501 |
| 特記なき場合、データは常温 (25 °C)・常圧 (100 kPa) におけるものである。 | |
四ヨウ化ゲルマニウム(Germanium(IV) iodide)は、化学式GeI4の化合物である。
製法
[編集]ゲルマニウムとヨウ素の反応[2]か、二酸化ゲルマニウムと57%ヨウ化水素酸の反応[1]で得られる。
- GeO
2 + 4 HI → GeI
4 + 2 H
2O
化学的性質
[編集]四ヨウ化ゲルマニウムは、250℃でテトラアルキルスズと反応して、R2SnI2及びR2GeI2 (R= Et, Bu, Ph)を生成する[4]。ゲルマニウム及び硫黄と高温で反応して、赤色のGeSI2及び橙色のGe2S3I2を生成する[5]。イオン液体([BMIm]Cl/AlCl3)中、130℃でノナカルボニル二鉄と反応して、Ge12[Fe(CO)3]8I4を得る[6]。
- 12 GeI
4 + 15 Fe
2(CO)
9 → Ge
12[Fe(CO)
3]
8I
4 + 22 FeI
2 + 111 CO↑
物理的性質
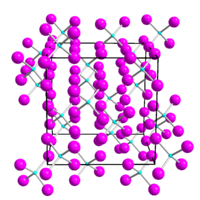
[編集]橙色から赤色の結晶性固体で、水中で加水分解する。二硫化炭素及びベンゼンに可溶であるが、四塩化炭素及びクロロホルムには難溶である[3]。融点を超えると、二ヨウ化ゲルマニウムとヨウ素に分解し始める[7]。立方晶系に結晶化し、空間群はPa3、格子定数はa = 11.89 Åである。結晶構造は、四面体状のGeI4分子から構成される。
出典
[編集]- ^ a b c A. W. Laubengayer, P. L. Brandt (Feb 1932). “The Preparation of Germanium Tetrabromide and Germanium Tetraiodide” (英語). Journal of the American Chemical Society 54 (2): 621–623. doi:10.1021/ja01341a502. ISSN 0002-7863. オリジナルの2021-10-20時点におけるアーカイブ。 2021年1月12日閲覧。.
- ^ a b L. M. Dennis, F. E. Hance (Dec 1922). “GERMANIUM. IV. GERMANIUM TETRA-IODIDE1” (英語). Journal of the American Chemical Society 44 (12): 2854–2860. doi:10.1021/ja01433a020. ISSN 0002-7863 2021年1月12日閲覧。.
- ^ a b Schenk, P.W. (1963). “12. Silicon and Germanium”. In Brauer, Georg. Handbook of preparative inorganic chemistry (Second ed.). Academic Press. p. 719. doi:10.1016/B978-0-12-395590-6.50020-X. ISBN 978-0-12-395590-6
- ^ Kocheshkov, K. A.; Fomina, N. V.; Sheverdina, N. I.; Zemlyanskii, N. N.; Chernoplekova, V. A. Reaction of tetraalkyltin with germanium tetrahalides. Izvestiya Akademii Nauk SSSR, Seriya Khimicheskaya, 1973. 3: 711. ISSN 0002-3353.
- ^ A.P. Velmuzhov, M.V. Sukhanov, A.D. Plekhovich, A.I. Suchkov, V.S. Shiryaev (Mar 2015). “Thermal decomposition study of GeSI2 and Ge2S3I2 glassy alloys” (英語). Journal of Non-Crystalline Solids 411: 40–44. Bibcode: 2015JNCS..411...40V. doi:10.1016/j.jnoncrysol.2014.09.018 2021年1月12日閲覧。.
- ^ Silke Wolf, Wim Klopper, Claus Feldmann (2018). “Ge 12 {Fe(CO) 3 } 8 (μ-I) 4 : a germanium–iron cluster with Ge 4 , Ge 2 and Ge units” (英語). Chemical Communications 54 (10): 1217–1220. doi:10.1039/C7CC08091C. ISSN 1359-7345. PMID 29336437 2021年1月12日閲覧。.
- ^ Holleman, Arnold F.; Wiberg, Egon; Wiberg, Nils (1995). Lehrbuch der anorganischen Chemie (101., verb. und stark erw. Aufl ed.). Berlin: de Gruyter. ISBN 978-3-11-012641-9
| 1 | 18 | |||||||||||||||||||||||||||||||
| 1 | HI | 2 | 13 | 14 | 15 | 16 | 17 | He | ||||||||||||||||||||||||
| 2 | LiI | BeI2 | BI3 | CI4 | NI3 | IxOy | IFx | Ne | ||||||||||||||||||||||||
| 3 | NaI | MgI2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | AlI3 | SiI4 | PI3 | SI2 | IxCly | Ar | ||||||||||||||
| 4 | KI | CaI2 | ScI3 | TiI4 | VI3 | CrIx | MnI2 | FeI2 | CoI2 | NiI2 | CuI | ZnI2 | Ga2I6 | GeIx | AsI3 | SeI2 | IBr | Kr | ||||||||||||||
| 5 | RbI | SrI2 | YI3 | ZrI4 | NbI5 | Mo | Tc | Ru | Rh | Pd | AgI | CdI2 | InI3 | SnIx | SbI3 | TeI4 | I | Xe | ||||||||||||||
| 6 | CsI | BaI2 | La | Ce | Pr | Nd | Pm | SmI2 | Eu | Gd | TbI3 | Dy | Ho | Er | Tm | Yb | Lu | HfI4 | TaI5 | W | Re | Os | Ir | Pt | AuI | HgxIy | TlI | PbI2 | Bi | Po | AtI | Rn |
| 7 | Fr | Ra | Ac | ThI4 | Pa | U | Np | Pu | Am | Cm | Bk | Cf | Es | Fm | Md | No | Lr | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og |
