鉱質コルチコイド

鉱質コルチコイド(こうしつコルチコイド、英語: Mineralocorticoid)は、副腎皮質の球状層で産生される、副腎皮質ホルモンの一つである。電解質コルチコイド、ミネラルコルチコイドなどとも言われる。塩分と水分のバランス(電解質バランスと体液バランス)に影響を与える。主な鉱質コルチコイドはアルドステロンである。
種類
[編集]生理学
[編集]
鉱質コルチコイドという名称は、これらのホルモンがミネラルの一種であるナトリウムの保持に関与しているという初期の観察結果に由来している。鉱質コルチコイドの主な内因性ホルモンはアルドステロンであるが、他の多くの内因性ホルモン(プロゲステロン[2]やデスオキシコルチコステロンなど)も鉱質コルチコイドの機能を持つ。
アルドステロンは腎臓に作用し、ナトリウムの能動的再吸収とそれに伴う水の受動的再吸収を担うと共に、皮質の集合管(結合尿細管)の主細胞におけるカリウムの能動的分泌と、集合管の間在細胞の内腔膜におけるプロトンATPアーゼを介したプロトンの能動的分泌を行う。その結果、血圧が上昇し、血液量が増加する。
アルドステロンは、副腎皮質の糸球体部で産生され、その分泌は主にアンジオテンシンIIによって媒介されるが、副腎皮質刺激ホルモン(ACTH)や局所的なカリウム濃度によっても影響を受ける。
作用機序
[編集]鉱質コルチコイドの作用は、核内受容体を介した遅いゲノム機構と、膜結合型受容体やシグナルカスケードを介した速い非ゲノム機構によって伝達される。
ゲノム機構
[編集]鉱質コルチコイドは、細胞質内の鉱質コルチコイド受容体に結合し、細胞の脂質二重層を自由に通過することができる。このタイプの受容体は、リガンドの結合によって活性化される。ホルモンが対応する受容体に結合した後、新たに形成された受容体-リガンド複合体は細胞核に移行し、DNA中の標的遺伝子のプロモーター領域にある多くのホルモン応答要素(HRE)に結合する。
その逆のメカニズムを転写抑制と呼ぶ。リガンドが結合していないホルモン受容体は、熱ショックタンパク質と相互作用し、その結果標的遺伝子の転写が阻止される。
アルドステロンとコルチゾール(糖質コルチコイド)は、鉱質コルチコイド受容体に対して同様の親和性を持つが、糖質コルチコイドは鉱質コルチコイドの約100倍の量が血中を循環している。鉱質コルチコイドの標的組織には、糖質コルチコイドによる過剰な刺激を防ぐための酵素が存在する。この酵素は、11-βヒドロキシステロイドデヒドロゲナーゼII型(タンパク質:HSD11B2)であり、糖質コルチコイドの11-デヒドロ代謝物への不活性化を触媒する。甘草はこの酵素を阻害することが知られており、慢性的に摂取すると偽性アルドステロン症と呼ばれる状態になることがある[3]。
病態生理学
[編集]高アルドステロン症(アルドステロンの上昇による症候群)は、特発性副腎過形成または副腎腺腫のいずれかによって引き起こされるのが一般的である。その結果、2つの主要な問題が生じる。
- 過剰なNa+と水の貯留による高血圧と浮腫
- カリウムイオン(K+)の排泄促進。K+の極端な減少による筋力低下は最終的に麻痺に至る。
低アルドステロン症(アルドステロンの産生不足による症候群)は、アジソン病に関連した塩分消耗状態を引き起こすが、古典的な先天性副腎過形成や他の疾患状態でもこのような状況を引き起こすことがある。急性の産生不足(出血性副腎炎)は、しばしば生命を脅かす。
医薬品
[編集]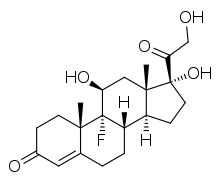
合成鉱質コルチコイドの例としては、フルドロコルチゾン(フロリネフ)がある。
重要な抗鉱質コルチコイドはスピロノラクトンとエプレレノンである。
関連項目
[編集]参考資料
[編集]- ^ Häggström, Mikael; Richfield, David (2014). “Diagram of the pathways of human steroidogenesis”. WikiJournal of Medicine 1 (1). doi:10.15347/wjm/2014.005. ISSN 2002-4436.
- ^ “Progesterone: An enigmatic ligand for the mineralocorticoid receptor”. Biochem Pharmacol 177: 113976. (July 2020). doi:10.1016/j.bcp.2020.113976. PMID 32305433.
- ^ Omar, HR; Komarova, I; El-Ghonemi, M; Fathy, A; Rashad, R; Abdelmalak, HD; Yerramadha, MR; Ali, Y et al. (2012). “Licorice abuse: Time to send a warning message”. Therapeutic Advances in Endocrinology and Metabolism 3 (4): 125–138. doi:10.1177/2042018812454322. PMC 3498851. PMID 23185686.
