利用者:Anesth Earth/作業場2
| 心臓 | |
|---|---|
 ヒトの心臓 | |
| 概要 | |
| 器官 | 循環器 |
| 動脈 | 大動脈、肺動脈幹および右左肺動脈、右冠状動脈、左冠状動脈主幹部 |
| 静脈 | 上大静脈、下大静脈、右左肺静脈、大心静脈、中心臓静脈、小心静脈、前心静脈 |
| 神経 | 心臓促進神経、迷走神経 |
| ラテン語 | cor |
| ギリシア語 | καρδία (kardía) |
| 解剖学用語 | |
心臓(しんぞう)とは、血液循環の原動力となる[1]、血液循環系の中枢器官である[2]。この臓器は血管を通して血液を送り出す[3]。本項ではヒトの心臓について概説するものとする。
概要
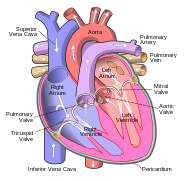
[編集]心臓は筋肉質の臓器であり、律動的な収縮によって血液の循環を行うポンプの役目を担っている[4]。心臓と血管は合わせて循環器系を構成する[5]。送り出された血液は組織に酸素と栄養素を運び、同時に二酸化炭素などの代謝廃棄物を肺へ運ぶ[6]。ヒトでは、心臓はおよそ握り拳ほどの大きさで、肺の間の胸部の中央区画、すなわち縦隔に位置している[7]。
心臓は4つの部屋(心腔)に分かれている。すなわち血流から見て上流、左右の心房と下流の左右の心室である[8][9]。一般的に、右心房と右心室を合わせて右心、左心房と左心室を合わせて左心と呼ぶ[10]。健康な心臓では、心臓弁により血液は一方向にのみ流れ、逆流を防いでいる[7]。心臓は保護袋である心膜に包まれており、その中には少量の液体(心嚢液)も含まれている。心臓の壁は3層で構成されている。すなわち、心外膜、心筋、心内膜である[11]。
心臓は洞房結節のペースメーカー細胞群によって決定されるリズムで血液を送り出す。これらの細胞は電流を生成し、心臓を収縮させ、房室結節を通って心臓の伝導系に沿って伝わる。
体内で脱酸素化された血液は、上・下大静脈から右心房に入り、右心室に流れる。ここから肺循環を通って肺へ拍出され、そこで酸素を取り込み、二酸化炭素を放出する。酸素化された血液は左心房に戻り、左心室を通過し、大動脈を通って体循環へ送り出される。そこで動脈、細動脈、毛細血管を通り、血管と細胞の間で栄養素やその他の物質が交換され、酸素を失い、二酸化炭素を得る。その後、細静脈を経て静脈を通り、心臓に戻る[12]。心臓は安静時に約72回/分の心拍数で鼓動する[13]。運動は一時的に心拍数を上げるが、長期的には低下させ、心臓の健康に良い[14]。心臓は送り出す血液のうち約5%を心臓自身で用いている。心臓を潤す血管は冠動脈(冠状動脈)といい、大動脈基部のバルサルバ洞から右心房・心室に伸び心臓の下部を回りこんで左心室の後・下壁に至る右冠動脈と、左心房・心室前方から中隔・心尖部に伸びる左冠動脈の2本に枝分かれする[15]。心筋は大きく脈動するため、心筋自体への血液の供給は主に筋肉の縮まる力が低くなった心臓拡張時に行われる[15]。心臓は交感神経と副交感神経の支配を受ける。前者は心拍数や心筋収縮力の増加および興奮伝達速度を早め、後者はこれらの減少や遅延を促す[16]。
心血管疾患は2008年時点で世界的に最も多い死因であり、全人類の死亡の30%を占めている[17][18]。これらの死亡のうち4分の3以上が冠動脈疾患と脳卒中によるものであった[17]。危険因子[要曖昧さ回避]には以下のものがある。喫煙、肥満、運動不足、高コレステロール血症、高血圧、そして適切にコントロールされていない糖尿病など[19]。心血管疾患は症状が乏しいが、胸痛や呼吸困難を引き起こすことがある。心臓病の診断は多くの場合、病歴の聴取、聴診器で心音を聴診すること、また心電図や超音波を使用する心臓超音波検査によって行われる[7]。心臓疾患の専門医は循環器内科医だが、治療には多くの医療専門分野が関わることがある[18]。
構造
[編集]

位置と形状
[編集]
ヒトの心臓は縦隔内下部のほぼ中央[21]、第5胸椎から第8胸椎の高さに位置している。心膜と呼ばれる二重膜の袋が心臓を取り囲み、縦隔に付着している[22]。心臓の後面には食道や胃があり、さらにその後方に脊椎がある。胸肋面と呼ばれる前面は胸骨と肋軟骨の後ろに位置している[4][11]。心臓の上部には、大血管(大静脈、大動脈、肺動脈)が付着している。心臓の上部は第3肋軟骨の高さに位置している[11]。
心臓の形はおおまかには、逆円錐状で、その軸は左斜め側に傾いている[11]。そのため心臓の下部は左側に傾き、肋骨の左側第5肋間から鎖骨中線の間に位置する[21][注釈 1]。心臓は、上部の太く大きな血管があり右後方に尖る[16]部分を「心底」、下部の左前方に[16]尖った部分を「心尖」と言う[21]。成人の場合、心尖は正中線(胸骨中線)から左に8〜9 cm、第4肋骨と第5肋骨(第5肋間)の肋軟骨との関節の近くにあり、ここに触れると拍動を確認できる[11][16]。成人の心臓の重さは250〜350グラムである[23]。心臓はよく拳のサイズと表現される(長さ12 cm、幅8 cm、厚さ6 cm)が[21][11]、この説明には異論もあり、心臓はわずかに大きい可能性がある[24]。よく鍛えられたアスリートは、運動の効果により、骨格筋と同様に、心筋も肥大し、かなり心臓が大きくなることがある[11]。
心臓の大部分は通常、胸の左側にわずかにずれている(左胸心)。まれな先天性障害(右胸心)では、心臓が右側にずれているが、体のすべての部分に血液を送り出すために左心がより強く大きいため、左側にあるように感じられる。左肺は右肺よりも小さく、心臓を収容するためのくぼみ(心切痕)がある[11]。
心腔
[編集]ヒトの心臓には4つの内腔、すなわち心腔がある[25]。心腔は二対の心房・心室、つまり右心房、左心房、右心室、左心室から成る[25]。それぞれの壁は、心房よりも心室が、同じ心室でも左心室の方が厚い[16]。上部の2つの心房は血液を受け取る側の心腔で、下部の2つの心室は送り出す側の心腔である。心房は房室中隔にある房室弁を通して心室に開いている。この境界は心臓の表面からも冠状溝として観察できる[26]。右心房の上部には耳のような構造があり、右心耳と呼ばれ、左心房の上部にも左心耳がある[27]。右心房と右心室を合わせて右心と呼ぶことがある。同様に、左心房と左心室を合わせて左心と呼ぶこともある[10]。心室は心室中隔によって互いに分離されており、心臓の表面からは、前室間溝と後室間溝として見ることができる[26]。
心臓骨格は密な結合組織より成る。心臓骨格は房室中隔を形成し、心房を心室から分離し、4つの心臓弁の基礎となる線維輪を形成する[28]。心臓骨格はまた、心臓の電気伝導系統において重要な境界を提供している。なぜなら、コラーゲンは電気を伝導できないからである。心房中隔は心房を分離し、心室中隔は心室を分離している[11]。
弁
[編集]
心臓には4つの弁があり、それらが心臓の各部屋を分けている。各心房と心室の間に1つの弁があり、各心室の出口に1つの弁がある[11]。つまり、弁は右心房と右心室、右心室と肺動脈、左心室と大動脈、左心房と左心室の間に存在し、それぞれ、三尖弁(右房室弁)、肺動脈弁、大動脈弁、僧帽弁(左房室弁、二尖弁)と呼ばれる[16]。
心房と心室の間にある弁は房室弁と呼ばれる。右心房と右心室の間の房室弁は三尖弁と呼ぶ。三尖弁は3つの弁尖を持ち、腱索と3つの乳頭筋(前・後・中隔乳頭筋)に接続している[29][30]。僧帽弁は左心房と左心室の間にあり、二尖弁とも呼ばれる[31]。これは2つの弁尖(前尖と後尖)を持ち、これらの弁尖も腱索を介して心室壁から突き出た2つの乳頭筋に接続している[32]。
乳頭筋は腱索という軟骨性の接続を通じて心臓の壁から弁へ伸びている[31]。これらの筋肉は弁が閉じる際に弁がひっくり返らないようにする[16][33]。心周期の弛緩期には、乳頭筋も弛緩しており、腱索の張力はわずかである。心臓の部屋が収縮すると乳頭筋も収縮し、腱索に張力を生じさせ、房室弁の弁尖が所定の位置に保持され、弁が心房側に押し戻されるのを防ぐ[11][注釈 2][30]。
さらにそれぞれ3枚の半月弁が各心室の出口に位ある[31]。肺動脈弁は肺動脈の基部に位置しており、3つの弁尖を持ち、乳頭筋には繋がっていない。心室が弛緩すると、動脈から心室に血液が逆流し、この血流がポケット状の弁を満たし、弁尖に圧力をかけて弁を閉じる。半月状の大動脈弁は大動脈の基部にあり、これも乳頭筋には接続されていない。この弁も3つの弁尖を持ち、大動脈からの逆流による圧力で閉じる[11]。
右心
[編集]右心は2つの部屋、右心房と右心室からなり、弁で分けられている。この弁は三尖弁である[11]。
右心房は、体の2つの主要な静脈である上大静脈と下大静脈からほぼ絶え間なく血液を受け取る。また、冠循環からの少量の血液は、下大静脈の開口部のすぐ上、内側にある冠状静脈洞を通じて右心房に排出される[11]。右心房の壁には、胎児期の心臓に存在していた開口部である卵円孔の名残である、卵円窩という楕円形のくぼみがある[11]。右心房の内面の大部分は滑らかで、卵円窩のくぼみは内側に位置し、前面には櫛状筋の顕著な隆起があり、これらは右心耳にも存在する[11]。
右心房は三尖弁を通じて右心室と接続されている[11]。右心室の壁には、肉柱と呼ばれる心筋の隆起があり、心内膜で覆われている。これらの筋肉の隆起に加え、中隔縁柱と呼ばれる心筋の帯が、心室中隔の下部から生じ、右心室の内部空間を横切り、下側の乳頭筋と接続している[11][34]。この帯は右心室の過膨張を防ぎ、心臓の伝導においても重要な役割を果たしている[34]。右心室は肺動脈幹に向かって先細りしており、収縮時に血液を排出する。肺動脈幹は左肺と右肺に向かって分岐し、血液をそれぞれの肺に運ぶ。肺動脈弁は右心室と肺動脈幹の間にある[11]。
左心
[編集]左心には2つの部屋があり、左心房と左心室が僧帽弁によって分けられている[11]。
左心房は4本ある肺静脈を通じて肺から酸素化された血液を受け取る。左心房には左心耳と呼ばれる小さな袋状の構造がある。右心房と同様に、左心房も櫛状筋で覆われている[35]。
左心室は右心室に比べて壁が非常に厚く、これは全身に血液を送り出すためにより大きな力が必要だからである。右心室と同様に、左心室にも肉柱があるが、中隔縁柱は存在しない。左心室は血液を大動脈弁を通じて全身に送り出す。大動脈弁の上には小さな開口部が2つあり、そこから冠状動脈を経由して血液が心筋に供給される。左側の弁尖の上には左冠状動脈があり、右側の弁尖の上には右冠状動脈がある[11]。
壁
[編集]心臓を動かす厚い筋肉[4]は心筋と呼ばれ、骨格筋と同様にアクチンとミオシンのフィラメントが滑走して動く横紋筋でありながら、多くの枝分かれ構造を持ち互いに境界膜(介在膜)で電気的に連絡し、まるで1つの大きな細胞のように同期する機能的合胞体となっている。この心筋は心臓を螺旋状に取り囲んでいる[16]。心筋は伸展の大きさに対応して強い収縮を行い、流入する血液が多くなると強く縮んで拍出量を増やす。これはスターリングの法則と呼ばれる[16]。

心臓の壁は、内側の心内膜、中間の心筋、外側の心膜の3層で構成されている。これらは二重膜で覆われた嚢である心膜に囲まれている[36]。
心臓の最も内側の層は心内膜と呼ばれ、単層扁平上皮で構成され、心腔と弁を覆っている。これは心臓の静脈や動脈の内皮と連続しており、薄い結合組織層を介して心筋と接続している[11]。心内膜はエンドセリンを分泌し、心筋の収縮を調節する役割を果たす可能性もある。[11]

心臓壁の中層は心筋で、心筋組織—横紋筋でできた不随意筋であり、コラーゲンの枠組みで囲まれている。心筋のパターンは優雅で複雑であり、筋細胞は心臓の部屋の周りを渦巻き、螺旋を描いている[11]。外側の筋肉は心房や大血管の基部を8の字の形で取り囲み、内側の筋肉は2つの心室の周りを8の字の形で包み、心尖部に向かって進んでいる[11]。この複雑な渦巻き状のパターンが、心臓が血液を効果的に送り出すのに役立っている[11]。
心筋には2種類の細胞が存在する。容易に収縮できる筋細胞と、伝導系のペースメーカー細胞である。筋細胞は心房と心室の細胞の大部分(99%)を占めている[37]。これらの収縮性細胞は、介在板によって接続されており、ペースメーカー細胞からの心臓活動電位のインパルスに迅速に反応することができる[37]。介在板は、筋細胞が合胞体として機能し、心臓全体の収縮を引き起こし、血液を心臓や大血管に送り出す収縮を可能にしている[11]。ペースメーカー細胞は心筋細胞の1%を占め、心臓の伝導系を形成している。これらは収縮性細胞よりもはるかに小さく、筋原線維が少ないため、収縮能力は限られている。その機能は多くの点でニューロンに似ている[11]。心筋組織には自動能と呼ばれる特有の機能があり、決まった速度で心臓活動電位を発生させ、それを細胞間で迅速に広げて心臓全体の収縮を引き起こす[11]。
心筋細胞には、筋収縮に関連するタンパク質が発現している[38]。これにはMYH7、ACTC1、TNNI3が含まれる[38]。これらは、アクチン、ミオシン、およびトロポニンファミリーに属する[38]。他の発現しているタンパク質にはLDB3があり、これらは骨格筋にも発現している[39]。
心膜
[編集]心膜(英: pericardium)は心臓を包む嚢(袋)である[36]。心膜の外側の硬い部分は線維性心膜と呼ばれる[36]。これは漿膜性心膜と呼ばれる内側の二重膜で裏打ちされている[36]。この漿膜性心膜は二重膜の間に心嚢液を生成して心臓の表面を潤滑にし[40]、心臓の拍動から生じる摩擦を低減する効果を持つ[21][16]。線維性心膜に付着している漿膜性心膜の部分は壁側板と呼ばれ、心臓に付着している部分は臓側板(別名: 心外膜、英語: epicardium)と呼ばれる。心膜は、胸腔内の他の構造との摩擦を減らし、心臓の位置を安定させ、感染から心臓を保護する役割を果たしている[41]。
冠循環
[編集]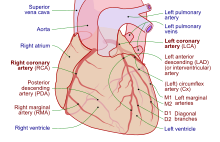
心臓組織は、体内の他の細胞と同様に、酸素や栄養素の供給を必要とし、代謝廃棄物の除去のための経路も必要である[42][43]。これを実現するのが冠循環で、冠循環には動脈、静脈、およびリンパ管が含まれる[42][43]。冠動脈を通る血流は、心筋の弛緩や収縮に応じて、流量にピークと谷がある[11]。
心臓組織は、大動脈弁のすぐ上から出る2本の動脈から血液を受け取る[43]。これらは左冠状動脈と右冠状動脈である[43]。左冠状動脈は大動脈から分岐してすぐに、左前下行枝と左回旋枝の2つに分かれる[43]。左前下行枝は左心房、左心室の大部分、および心室中隔の大部分を供給する[43]。これを行うために、左前下行枝は小さな枝(対角枝と中隔枝)に分岐する。左回旋枝は左心室の後面と下部を供給する。右冠状動脈は右心房、右心室、および左心室の後下部を供給する。また、右冠状動脈は房室結節(ヒトの約90%)および洞房結節(ヒトの約60%)に血液を供給する。右冠状動脈は心臓の後面の溝に沿って走り、左前下行枝は心臓の前面の溝に沿って走る。心臓を供給する動脈の解剖学的構造は、人によって大きな違いがある[44]。動脈はその末端でさらに小さな枝に分かれ、それぞれの動脈供給の境界で合流する[11]。
冠状静脈洞は、右心房に流れ込む大きな静脈であり、心臓のほとんどの静脈からの排出血液を受け取る。冠状静脈洞は大心静脈(左心房および両心室からの血流を受け取る)、後心静脈(左心室後部)、中心臓静脈(左心室と右心室の底部)、および小心静脈から血液を受け取る[45]。前心静脈は右心室の前部から血流を受け取り、直接右心房に合流する[11]。
心臓の3つの層の下には、リンパ管叢と呼ばれる微細なリンパ管のネットワークが存在する。これらのネットワークは左と右の主幹に集まり、心臓の表面にある心室の間の溝に沿って上行し、途中で細いリンパ管と合流する。これらのリンパ管は房室間溝に入り、横隔膜上の左心室部分から流出するリンパ管と合流する。左側のリンパ管はこのリンパ管と合流し、肺動脈と左心房に沿って進み、下気管支リンパ節で終わる。右側のリンパ管は右心房と横隔膜上の右心室部分に沿って進む。通常、これは上行大動脈の前を通過し、最終的に腕頭リンパ節で終わる[46]。
神経支配
[編集]
心臓は迷走神経および交感神経幹から分岐した神経から信号を受け取る。これらの神経は心拍数に影響を与えるが、直接制御することはない。交感神経はまた心臓の収縮力にも影響を与える[47]。これらの神経を介して伝わる信号は、延髄にある2対の心血管中枢から発生する。副交感神経系の迷走神経は心拍数を減少させ、交感神経幹からの神経は心拍数を増加させる[11]。これらの神経は心臓の上にある神経のネットワークである心臓神経叢を形成する[11][46]。
迷走神経は脳幹から出る長い神経で、胸部および腹部の多くの器官、特に心臓に副交感神経の刺激を与える[48]。交感神経幹からの神経信号はT1–T4の胸神経節を通って洞房結節および房室結節、さらには心房や心室に向かって伝わる[要出典]。心室は副交感神経繊維よりも交感神経繊維で豊富に支配されている[49]。交感神経の神経伝達物質は、ノルアドレナリン(ノルエピネフリンとも呼ばれる)である[49]。ノルアドレナリンは心臓のベータ1アドレナリン作用性受容体に結合する[11]。これにより再分極期間が短縮され、脱分極と収縮の速度が速まり、心拍数が増加する[49]。化学的またはリガンド依存性のナトリウムおよびカルシウムイオンチャネルが開き、正に帯電したイオンの流入を可能にする[11]。
発生
[編集]
ヒトでは、心臓は胚発生の約3週目に拍動を始め、血液を送り出す[50][51]。この早い段階での開始が、その後の胚発生や出生前発達にとって重要となる[52]。母体から供給された酸素や栄養が行き渡り、他の臓器が分化・成長を行えるようになる[53]。
心臓は臓側中胚葉から発生し、神経板先頭に心臓形成域を形成する[54]。ここで2つの心内膜筒が作られ、これが融合して単一の心筒を形成する[55]。3週から4週にかけて、心筒は長くなり、心膜内でS字型に折り畳まれ、心室や主要な血管が正しい位置に配置される[56]。さらに発達が進むと[56]、中隔や弁の形成、心腔の再構成が行われる。5週目の終わりまでに心房の中隔(一次中隔)が完成し、9週目には心臓の弁が完成する[11]。一次中隔が完成するまでの左右の心房の交通は一次孔と呼ばれる[56]。
一次孔はいったんは一次中隔により閉鎖されるが、第5週末以降には一次中隔が穿孔して二次孔と呼ばれる穴が出現する[56]。しかし、一次中隔に接して、二次中隔が出現し、二次孔に覆い被さる。覆い被さっていない部分は卵円孔と呼ばれる開口部となる[56]。卵円孔は胎児の心臓で、右心房から左心房へ血液を直接通し、一部の血液が肺を迂回できるようにしている[56]。出生後数秒以内に、以前は弁として機能していたと一次中隔が卵円孔を閉じ、通常の心臓循環パターンが確立される[56]。卵円孔があった部分には、右心房の表面に卵円窩と呼ばれるくぼみが残る[11]。
つまり、発生初期の心臓は初期胚の前方につくられる1本の単純な筒であるが、周囲の内・外胚葉から細胞の増殖因子や接着因子を受け、転写因子を活性化させながら屈曲してループ状になり、さらに中隔膜が形成されて2系列の並列循環構造へ成長する[53]。
心拍動は母親の心拍数に近い毎分75~80拍から始まり、その後、胚の心拍数は加速し、7週目初期に165~185 回/分のピークに達する[57][58]。9週目以降、心拍数は減速し、出生時には毎分約145(±25)拍にまで低下する。出生前の段階では、男女の心拍数に違いはない[59]。
複雑な発生過程を経る心臓は、形成に多くの遺伝子が関わる。そのために先天性心疾患は頻度が高く、100人に1人ほどの割合で生じる[60]。また心臓の心筋細胞は誕生後に細胞分裂を行なわず、大きさは生理的肥大によって成長する。そのため何らかの疾患で細胞が減少しても元に戻らないと考えられてきた[60]。しかしながら、2001年には心筋梗塞後に心筋細胞が僅かながら有糸分裂を行ったと報告される[61]など、従来の定説には疑問が呈されている[62]。しかし、筋細胞の再生が心臓の恒常性において果たす役割は無視できるほど小さいことは示唆されている[62]。そのため、末期の心臓疾病の根治には移植しか手段が無い。そのため、iPS細胞など未分化細胞による再生治療の研究が盛んに行われている[60]。
生理学
[編集]血液の流れ
[編集]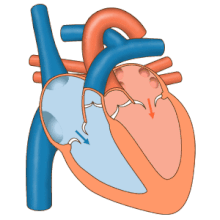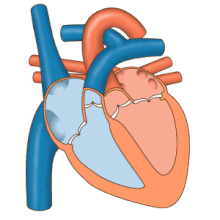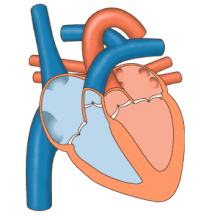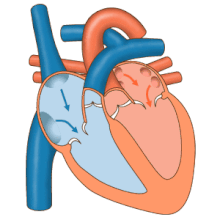
心臓は循環器系においてポンプとして機能し、全身に連続的な血液の流れを供給する[11]。この循環は、全身へ血液を送り返す体循環と、肺へ送り出して戻す肺循環で構成される[11]。肺循環では、血液が肺で呼吸の過程を通じて二酸化炭素と酸素を交換する。体循環では、酸素を全身に運び、二酸化炭素や比較的酸素の少ない血液を心臓に戻し、肺へ送る[11]。
右心は、2つの大静脈である上大静脈と下大静脈から酸素の少ない血液を集める[11]。血液は右心房と左心房に絶えず流れ込む[11]。上大静脈は横隔膜より上から血液を集め、右心房の上部後方に流れ込む[11]。下大静脈は横隔膜より下から血液を集め、上大静脈の開口部の下部にある心房の後部に流れ込む[11]。下大静脈の開口部のすぐ上で中央寄りには、薄い壁の冠状静脈洞の開口部がある[11]。冠状静脈洞は心筋から酸素の少ない血液を右心房に戻す。血液は右心房に集まり、右心房が収縮すると、血液は三尖弁を通って右心室に送られる。右心室が収縮すると三尖弁が閉じ、血液は肺動脈弁を通って肺動脈幹に送られる[11]。肺動脈幹は左右の肺動脈に分かれ、さらに小さな動脈に分岐していき、最終的に毛細血管に達する[11]。ここで、肺胞の周りを通過する際に、二酸化炭素が酸素と交換される[11]。この交換は拡散という受動的なプロセスによって行われる[63]。
左心では、酸素を豊富に含んだ血液が肺静脈を通って左心房に戻される[11]。その後、血液は僧帽弁を通って左心室に送られ、さらに大動脈弁を通って全身循環に送り出される[11]。大動脈は大きな動脈で、多くの小動脈や細動脈、最終的には毛細血管に分岐する[11]。毛細血管では、血液から体細胞に酸素や栄養が供給され、代謝のために使われると同時に、二酸化炭素や老廃物が交換される[11]。酸素が少なくなった血液は細静脈や静脈を通って上大静脈と下大静脈に集まり、右心に戻る[11]。
心周期
[編集]
心周期は、心臓が1回の拍動で収縮と弛緩を繰り返す一連の過程を指す[13]。心室が収縮し、大動脈と肺動脈幹に血液を送り出す期間を収縮期と呼び、心室が弛緩し、血液が再び心室に流れ込む期間を拡張期と呼ぶ。心房と心室は連携して働き、収縮期には心室が収縮している間に心房が弛緩し、血液を集める。拡張期には心室が弛緩している間に心房が収縮し、血液を心室に送り込む。この調整により、血液が効率的に全身に送られる[11]。
心周期はさらに以下の期に区分される[64]。収縮期の始まりは等容性収縮期といい、全ての弁が閉じた状態で心室が収縮を起こし、内圧が上昇する[64]。次の駆出期は、心室内圧が動脈の圧力を上回り動脈弁が開いて血液が流れ始めてから、内圧が充分に低下して弁が閉じるまでを指す[64]。拡張期の開始は等容性弛緩期と言い、全ての弁が閉じた状態で心室が弛緩し、内圧が低下する[64]。最後の充満期(流入期)とは、内圧低下によって房室弁が開き、動脈弁は閉じたままであるため心室内に血液が充満するまでの間を言う[65]。心拍数75回/分の場合、心周期0.8秒のうち収縮は0.3秒、弛緩は0.5秒で行われる[65]。
心拍出量
[編集]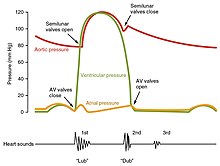
心拍出量(Cardiac Output: CO)は、1分間に各心室が送り出す血液の量(1回拍出量)を測定したもので、1回拍出量(Stroke Volume: SV)に心拍数(Heart Rate: HR)を掛けて算出される。つまり、CO = SV x HRとなる[11] 。心拍出量は体表面積で除すことで標準化され、これを心係数と呼ぶ。
平均的な1回拍出量が約70mLとされる場合、平均的な心拍出量は5.25 L/分であり、正常範囲は4.0~8.0 L/分となる[11]。1回拍出量は通常、心エコー検査を使用して測定され、心臓の大きさ、個人の身体的および精神的状態、性別、心筋収縮性、収縮の持続時間、前負荷、後負荷に影響される[11]。激しい運動時には心拍数が増加するため、心拍出量も増える[65]。
前負荷は、拡張期の終わりに心房内にかかる圧力を指し、この時点で心室は最大限に血液で満たされている。主な要因は心室が血液で満たされる時間であり、心室が頻繁に収縮すると、満たされる時間が短くなり、前負荷は少なくなる[11]。前負荷は血液量にも影響される。心筋の各収縮の力は前負荷に比例し、これはフランク・スターリングの法則として知られている。この法則によれば、筋繊維の初期の長さに比例して収縮力が増す、つまり心室が引き伸ばされるほど強く収縮する[11][66]。
後負荷は、収縮期に心臓が血液を送り出すために生成しなければならない圧力で、血管抵抗に影響される。後負荷は心臓の弁の狭窄(狭窄)や末梢血管の収縮または弛緩によっても左右される[11]。
心筋の収縮力は1回拍出量を制御し、これは変力薬と呼ばれる物質によって正または負の影響を受ける[67]。これらの物質は体内の変化によって生じることもあれば、医療処置の一環として投与されることもあり、特に集中治療室では生命維持の一環として使用されることがある。収縮力を増加させる変力薬は陽性変力薬と呼ばれ、交感神経の作動薬であるアドレナリン、ノルアドレナリン、ドーパミンが含まれる[68]。逆に、収縮力を減少させる強心剤は陰性変力薬と呼ばれ、カルシウム拮抗剤が含まれる[67]。
電気伝導
[編集]
通常のリズムで拍動する心拍、すなわち洞調律は、心臓生来のペースメーカーである洞房結節によって作り出される。ここで電気信号が発生し、心筋が収縮する。この洞房結節は、上大静脈との接合部近くにある右心房の上部に位置している[69]。洞房結節で生成された電気信号は、右心房内を放射状に伝わり、左心房にはバッハマン束を通じて伝達され、左右の心房が同時に収縮する[70][71][72]。その後、信号は房室結節に伝わる。房室結節は、右心房の下部、右心房と左心室の境界である房室中隔に位置している。この中隔は、電気信号が通過できない心臓内の心臓骨格の一部であり、信号は房室結節のみを通過するように強制される[11]。その後、信号はヒス束を通じて左右の脚枝(bundle branch)に伝わり、心室へ送られる。心室では、特殊な組織であるプルキンエ繊維によって電気信号が心筋に伝達される[73]。

心拍数
[編集]心拍数とは1分あたり心臓が拍動する回数である。通常よりも心拍数が高い状態を頻脈と言い、運動をしたり、興奮状態であったり、また発熱などによって起こる。心拍数が低い場合は徐脈と言う。なお、やや呼吸と連動し、息を吸う時には頻脈傾向になる[65]。

通常の安静時心拍数は、洞房結節(右心房の壁にあるペースメーカー細胞のグループ)によって作られ、維持される。このリズムは洞調律と呼ばれる。洞房結節の細胞は、活動電位を生成することでこの役割を果たす。この心臓活動電位は、特定の電解質がペースメーカー細胞内外に移動することで作られ、その後、周囲の細胞に伝わる[74]。
洞房結節の細胞は非興奮時、細胞膜には負の電荷がある。ナトリウムイオンが急速に流入することで膜の電荷が正になり、これが脱分極と呼ばれる。この現象は自発的に発生する[11]。細胞が十分に高い電荷を持つとナトリウムチャネルが閉じ、続いてカルシウムイオンが細胞に入り、すぐ後に細胞内からカリウムが細胞外に流出し始める。これらのイオンは、洞房結節細胞の膜にあるイオンチャネルを通じて移動する。カリウムとカルシウムは、膜の電位が十分に高くなったときにのみ動き始めるため、これらのチャネルは電位依存チャネルと呼ばれる。カルシウムチャネルが閉じ、カリウムチャネルが開くとカリウムが細胞から流出し、細胞が負の電荷を持つようになり、これを再分極と呼ぶ。膜電位が約-60 mVに達するとカリウムチャネルが閉じ、脱分極のプロセスが再び始まる[11]。
イオンは高濃度の場所から低濃度の場所へ移動するため、ナトリウムは細胞外から細胞内へ、カリウムは細胞内から細胞外へ移動する。カルシウムも重要な役割を果たし、カルシウムがゆっくりとチャネルを通ることで洞房結節細胞は正電荷を持つ「プラトー」相を維持する。この一部は絶対不応期と呼ばれる。カルシウムイオンは、トロポニンCと結びつき、トロポニン複合体を介して心筋の収縮を可能にし、分離することで弛緩を引き起こす[75]。
成人の安静時心拍数は60~100 回/分の範囲内にある。新生児の安静時心拍数は約129 回/分で、成熟するにつれて徐々に減少する[76]。アスリートの心拍数は60 回/分を下回ることもある。運動中の心拍数は150 回/分に達し、最大心拍数は200~220 回/分に達することもある[11]。
影響因子
[編集]通常の洞調律によって生じる安静時心拍数は、いくつかの要因によって影響を受ける。脳幹にある心血管中枢は、迷走神経や交感神経幹を介して心臓に及ぼされる交感神経および副交感神経の影響を制御している[77]。心血管中枢は、血管の伸展を感知する圧受容器や、血中の酸素と二酸化炭素の量、およびpHを感知する化学受容器からの情報を受け取る。これらの受容器によって、反射を介して血流の調節が行われる[11]。
圧受容器は、大動脈洞、頸動脈洞、大静脈、肺血管、右心房などに存在し、血圧、運動レベル、血液の分布などに応じて活動電位の発火率が決まる[78]。圧力と伸展が増加すると、圧受容器の発火率が上昇し、心血管中枢は交感神経刺激を減少させ、副交感神経刺激を増加させる。逆に、圧力と伸展が減少すると、発火率が低下し、交感神経刺激が増加し、副交感神経刺激が減少する[11]。また、心房への血流の変動に関連する反射として、心房反射またはベインブリッジ反射がある[79]。静脈還流が増加すると、心房の壁が伸び、ここにある特殊な圧受容器の発火率が上昇する[79]。心房の圧受容器が発火率を増加させると、心血管中枢は交感神経刺激を増加させ、副交感神経刺激を抑制して心拍数を上げる[79]。 頸動脈小体や大動脈付近にある化学受容器は、血中の酸素や二酸化炭素のレベルに反応する。酸素が少なく、二酸化炭素が多いと、受容器の発火が促進される[80]。
運動やフィットネスレベル、年齢、体温、基礎代謝率、感情状態なども心拍数に影響を与える。アドレナリン、ノルアドレナリン、甲状腺ホルモンなどのホルモンの濃度が上昇すると、心拍数は増加する。カルシウム、カリウム、ナトリウムなどの電解質のレベルも、心拍数の速さや規則性に影響を与える。低酸素血症、低血圧、脱水は心拍数を増加させる可能性がある[81]。
心拍動に使うエネルギーは、安静時には脂肪酸を用い[82]、活発に活動する場合は乳酸などを消費する[83]。乳酸をピルビン酸に酸化させる代謝であり、四肢の筋肉が用いる解糖系とは異なる[4]。
臨床的意義
[編集]疾患
[編集]心血管疾患は、心臓に関連する疾患を含み、世界中で最も多い死因となっている[84]。心血管疾患の大半は非感染性であり、生活習慣や加齢とともに増加する他の要因に関連している[84]。心臓病が主要な死因であり、2008年には全死亡の平均30%を占めている[17]。この割合は、高所得国では28%から40%と幅がある[18]。心臓や血管を専門とする内科医は循環器内科医と呼ばれる[85]。心臓疾患の治療には他にも多くの医療専門職が関与しており、心臓外科医、集中治療医、理学療法士や栄養士などの医療従事者が含まれる[86]。
虚血性心疾患
[編集]虚血性心疾患としても知られる冠動脈疾患は、動脈の内壁に脂肪物質が蓄積するアテローム性動脈硬化によって引き起こされる[87]。これらの脂肪沈着物(アテローム性プラーク)は、冠動脈を狭め、重篤な場合には心臓への血流が減少する可能性がある[87]。軽度の狭窄であれば、患者は症状を感じないことがあるが、重度の場合は胸痛が起こり、運動中、さらには安静時にも呼吸困難を引き起こす可能性がある[88]。アテローム性プラークの薄い覆いが破裂すると、内部の脂肪滴が血流にさらされ、血栓が形成されて動脈を塞ぎ、心筋への血流が制限されて心筋梗塞(心臓発作)や不安定狭心症を引き起こす[89]。最悪の場合、これが心停止を引き起こし、心臓からの血液拍出が完全に失われることがある[90]。肥満、高血圧、コントロールされていない糖尿病、喫煙、高コレステロール血症は、アテローム性動脈硬化や冠動脈疾患のリスクを高める要因となる[84][87]。
心不全
[編集]心不全は、心臓が体の要求を満たすだけの血液を送り出すことができない状態として定義される[91]。心不全の患者は、特に横になるときに呼吸困難を感じることがあり、足首のむくみ(末梢性浮腫)が見られることもある[91]。心不全は多くの心疾患が原因で発症するが、特に虚血性心疾患、心臓弁膜症、または高血圧と関連している[91]。まれに、さまざまな心筋症が原因となることもある[91]。心不全は、通常は心室の心筋が弱くなる場合(収縮不全)に見られるが、心筋が強くても、硬く、収縮の間に十分に弛緩できない場合(拡張不全)にも見られることがある[91]。この状態は、左心室に影響を与える場合(主に呼吸困難を引き起こす)、右心室に影響を与える場合(主に脚のむくみや頸静脈圧の上昇を引き起こす)、または両方の心室に影響を与える場合がある。心不全の患者は、危険な不整脈を発症するリスクが高い[91]。
心筋症
[編集]心筋症は心臓の筋肉に影響を与える疾患である。中には、心筋の異常な肥厚を引き起こすもの(肥大型心筋症)、心筋を異常に拡張させて弱くするもの(拡張型心筋症)、心筋を硬くして収縮の間に完全に弛緩できなくするもの(拘束型心筋症)、心拍リズム異常を引き起こしやすくするもの(不整脈原性心筋症)がある。これらの疾患は遺伝性のものが多く、遺伝子疾患として受け継がれることがあるが、拡張型心筋症のようにアルコールなどの毒素によって引き起こされることもある。肥大型心筋症のような心筋症の一部は、特にアスリートにおいて突然死のリスクが高まることが知られている[11]。多くの心筋症は、疾患が進行するにつれて心不全に至ることがある[91]。
弁膜性心疾患
[編集]健康な心臓の弁は血液を一方向にスムーズに流し、逆流を防ぐ役割を果たしている。しかし、病変がある弁では、開口部が狭くなり(狭窄)、血液の前方への流れを妨げたり、弁が漏れて逆流を引き起こすことがある(逆流)。弁膜性心疾患は呼吸困難、失神、胸痛を引き起こす場合があるが、無症状で、定期検診の際に異常な心音や心雑音で初めて発見されることもある。先進国では、弁膜性心疾患の主な原因は加齢による変性だが、心内膜炎などの感染症によって引き起こされることもある。一部の地域では、リウマチ性心疾患が弁膜性心疾患の主要な原因であり、通常は僧帽弁や大動脈弁の狭窄を引き起こし、A群溶血性レンサ球菌感染症に対する免疫反応によって引き起こされる[92][93]。
心不整脈
[編集]健康な心臓では、電気的インパルスが洞房結節から発生し、心房全体、房室結節、最終的には心室に伝わり、規則的な収縮を維持している[94][95]。この電気経路に異常が起こると、異常な心拍リズム、つまり不整脈が発生する[96]。心不整脈は無症状であることもあれば、動悸、失神、呼吸困難を引き起こすこともある[97]。心房細動などの一部の不整脈は、長期的に脳卒中のリスクを高める[98]。
一部の不整脈では心臓が異常に遅く拍動し、これを徐脈または徐脈性不整脈と呼ぶ。これは、洞不全症候群や、心臓の伝導系の障害(心ブロック)によって引き起こされる[99]。他の不整脈では、心臓が異常に速く拍動し、これを頻脈または頻脈性不整脈と呼ぶ。これらの不整脈には多くの種類があり、心臓のさまざまな部位から発生する。例えば、心房から発生するもの(例:心房粗動)、房室結節から発生するもの(例:房室結節回帰性頻拍)、心室から発生するもの(例:心室頻拍)がある。頻脈性不整脈の一部は心臓内の瘢痕によって引き起こされ(例:一部の心室頻拍)、他のものは興奮焦点(例:局所心房頻拍)によって引き起こされる。生まれつき存在する異常な伝導組織が原因となるもの(例:ウォルフ・パーキンソン・ホワイト症候群)もある。最も危険な心拍の異常は心室細動で、心室が痙攣して収縮できなくなり、未治療では急速に致命的となる[100]。
心膜疾患
[編集]心臓を包む膜である心膜が炎症を起こす病態は、心膜炎と呼ばれる。この病気は通常、背中に広がる胸痛を引き起こし、しばしばウイルス感染(伝染性単核球症、サイトメガロウイルス、またはコクサッキーウイルス)が原因となることが多い。心膜腔に液体(心嚢液)が蓄積することがあり、これを心嚢液貯留と呼ぶ。心嚢液貯留は心膜炎、腎不全、腫瘍に続発して発生することが多く、通常は症状を引き起こさない。しかし、大量の液体が蓄積したり、急速に液体が蓄積した場合、心臓を圧迫して心タンポナーデと呼ばれる状態を引き起こし、呼吸困難や致命的な低血圧をもたらす。診断や心タンポナーデの緩和のために、針を使用して心膜腔から液体を除去する処置を心嚢穿刺と呼ぶ[101]。
先天性心疾患
[編集]一部の人々は、生まれつき心臓に異常を持っており、これを先天性心疾患と呼ぶ。これらの異常は比較的軽微なもの(例:卵円孔開存、正常の変異と見なされることもある)から、生命を脅かす重篤なもの(例:左心低形成症候群)までさまざまである。一般的な異常には、心臓の左右を分ける筋肉に影響を与えるもの(例:心室中隔欠損、「心臓に穴が開いている」状態)や、心臓の弁(例:先天性大動脈弁狭窄)、心臓から出る主要な血管(例:大動脈縮窄)に影響を与えるものがある。より複雑な症候群もあり、心臓の複数の部分に影響を与えるものも見られる(例:ファロー四徴症)。
一部の先天性心疾患では、通常は肺に戻される酸素含量の少ない血が、代わりに全身に送り出されることがある。これらはチアノーゼ性心疾患として知られ、しばしば重篤である。主な先天性心疾患は、出生直後や出生前に検出され、呼吸困難や成長の遅れを引き起こすことが多い(例:大血管転位)。比較的軽度の先天性心疾患は、成人期まで検出されず、後になって症状が現れることがある(例:心房中隔欠損)[102][103]。
チャネロパチー
[編集]チャネロパチーは、影響を与える臓器系に基づいて分類できる。心血管系では、各心拍に必要な電気インパルスが、心臓の各細胞の電気化学的勾配によって提供される。心拍はイオンが膜を越えて正しく移動することに依存しているため、心臓のイオンチャネルの異常(心臓チャネロパチー)は、心疾患の主要なグループを形成している[104][105]。心臓のイオンチャネル異常で、突然死症候群や不整脈突然死症候群の一部の原因を説明できることがある[106]。最も一般的な心臓チャネロパチーは、QT延長症候群である。
- QT延長症候群(LQTS) – 主に遺伝性。心電図ではQT間隔(QTc)が延長していることが確認される。特徴として失神、突然死の危険がある生命を脅かすリズム障害、トルサード・ド・ポワント型の心室頻拍や心室細動がある[107]。
- QT短縮症候群
- カテコールアミン誘発性多形性心室頻拍(CPVT)[108]
- 進行性心臓伝導障害(PCCD)[109]
- 早期再分極症候群(BER) – 主に若年層や活動的な人、特に男性に見られる。これは、テストステロンが多くなることでカリウム電流が増加し、心電図上でJ点が上昇することによる。極めてまれに、心室細動や死に至ることがある[110]。
- ブルガダ症候群 – 遺伝性疾患であり、この症候群に特徴的な異常な心電図所見を有し、若い男性における突然死の最も多い原因の1つである[111]。
診断
[編集]心疾患は、病歴聴取、心臓検査、および血液検査、心エコー検査、心電図、画像診断などの追加検査によって診断される。その他、心臓カテーテル検査などの侵襲的手技も有用である[112]。
検査
[編集]心臓検査は、視診、触診(触診)、聴診器を使用した聴診が含まれる[113]。手や関節などに現れる症状や徴候を評価する。通常は橈骨動脈(手首の近く)で脈拍が測定され、リズムや強さが確認される。血圧は、手動または自動の血圧計を使用して測定される。より侵襲的だが、動脈にカテーテルを留置して直接圧力を測定することも可能である(動脈ライン)。頸静脈圧の上昇有無も確認する。胸部は、心臓から伝わる振動があるかを触診し、聴診器で音を聞く。
心音
[編集]
心臓の弁の閉鎖によって心音が生じる。
通常、健康な心臓では、2つの心音(S1とS2)のみが聞こえる。I音(S1)は、心室収縮時に房室弁が閉じる音で、英語では"lub"と表現される[114]。II音(S2)は、心室拡張時に半月弁が閉じる音で、英語では"tup"と表現される[114][11]。それぞれの音は2つの成分からなり、2つの弁が閉じる際のわずかな時間差を反映している[115]。S2は、吸気やさまざまな弁や心臓の問題によって分裂することがある[115]。追加の心音が存在する場合もあり、これにより心音は三拍子となり、心拍数が増加すると馬の速い歩調に似てくるので奔馬調律と呼ばれる[114]。III音(S3)は通常、心室内の血液量の増加を示す[114]。III音は非常に小さく、II音の後に心房から心室へ血液が流れることで発生する音である[65]。IV音(S4)は心房音とも呼ばれ、拡張期の終わり近くで心房壁が収縮するとき心室壁が伸展されて生じる音である[116]。S4は正常人では極めて弱く、聴取不能であるが、聴取されればほぼ病的である[116]。S3とS4が両方存在する場合、4拍子の奔馬調律が聞かれる[11]。
心雑音は、異常な心音だが、必ずしも病的ではなく、いくつかの種類がある[117]。通常は2つの心音(S1とS2)があり、異常な心音は追加の心音(S3やS4)や、心音の間に生じる血液の流れに関連する「雑音」として現れる。心雑音は、音量で1(最も静か)から6(最も大きい)まで評価され[118](Levineの分類)、心音との関連、心周期内での位置、音の放散、姿勢の変化、聴診器の面によって聞こえる音の周波数、および最もよく聞こえる場所などでも評価される[117]。心雑音は、心臓弁の損傷や心室中隔欠損などの先天性心疾患が原因で発生することもあれば、正常な心臓でも聞かれることがある[119]。別の種類の音として、心膜摩擦音があり、これは心膜炎の場合に炎症を起こした心外膜が互いに擦れ合う音である[120]。
血液検査
[編集]血液検査は、多くの心血管疾患の診断と治療において重要な役割を果たす。
トロポニンは、血液供給が不十分な心臓の感度の高いバイオマーカーである。損傷後4~6時間で放出され、通常12~24時間でピークに達する[68]。トロポニンの検査は、発症時と3~6時間以内に行われることが多く[121]。検査値の高値または有意な上昇が診断に重要である。脳性ナトリウム利尿ペプチド(BNP)検査は心不全の評価に使用され、左心室に負荷がかかると上昇する。これらの検査は心疾患に対して特異的なため、と見なされる[122]。CP-MB(クレアチンキナーゼMB型)検査も心臓の血液供給に関する情報を提供するが、特異度や感度が低いため、使用頻度は少なくなってきている[123]。
その他の血液検査も、患者の一般的な健康状態や心臓病のリスク要因を理解するためにしばしば行われる。これには、全血球計算(貧血の調査)や、基礎代謝パネル(電解質異常などを明らかにするための検査)が含まれることが多い。適切な抗凝固療法を行うために凝固検査も必要とされることがある。また、コレステロールの評価のための空腹時脂質検査や、糖尿病の評価のための空腹時血糖(またはHbA1c検査)もよく行われる[124]。
心電図
[編集]
身体に表面電極を装着することで、心臓の電気活動を記録することができる。この電気信号の記録を心電図(ECGまたはEKG)という。心電図はベッドサイド検査であり、身体に10個のリードを装着する。この方法で「12誘導」心電図が得られるが、3つの追加リードは数学的に計算され、1つのリードは接地されている[125]。
心電図には5つの主な特徴があり、P波(心房脱分極)、Q波、R波、S波(心室脱分極)[注釈 3]、およびT波(心室再分極)がある[11]。心臓の細胞が収縮すると、電流が心臓を通過する。心電図上での下向きの変動は、細胞がそのリードの方向に向かってより正に帯電する(「脱分極する」)ことを示し、上向きの変動は細胞がそのリードの方向に向かってより負に帯電する(「再分極する」)ことを示す。これはリードの位置に依存するため、脱分極の波が左から右に移動すると、左側のリードでは負の変動が、右側のリードでは正の変動が見られる。心電図は、リズム障害や心臓への血液供給の不足を検出するための有用なツールである[125]。心臓の異常が疑われるが、心電図上にすぐに現れない場合もある。その場合、運動を行いながらの運動負荷試験があえて異常を引き起こすために使用されることがある。また、評価時にリズム異常が検出されない場合は、24時間のホルター心電図を装着することもある[125]。
画像診断
[編集]心臓の解剖学や機能を評価するために、さまざまな画像診断法が使用される。これには、超音波検査(心エコー)、血管造影、CT、MRI、およびPETスキャンが含まれる。心エコーは、心臓の機能を測定し、弁膜疾患を評価し、異常の有無を確認するために使用される心臓の超音波検査である。心エコーは胸部にプローブを当てて行うこともあれば(経胸壁)、食道内にプローブを挿入して行うこともある(経食道心エコー)。典型的な心エコーの報告書には、弁の狭窄の有無、血液の逆流(逆流)の有無、および収縮期と拡張期の血液量に関する情報が含まれる。収縮期に左心室および右心室から排出される血液量を示す駆出率も計算される。駆出率は、心臓から排出される血液量(1回拍出量)を心臓が血液で満たされた量(拡張末期容量)で割ることによって得られる[126]。心エコーは、身体にストレスがかかる状況で行われることもあり、血液供給の不足を示す兆候を調べるために使用される。これが心臓負荷試験の一つであり、運動を行うか、運動ができない場合はドブタミンなどの薬を注射して行う[113]。
CTスキャンや胸部X線などの画像診断法は、心臓の大きさを評価し、肺水腫の兆候を確認したり、心臓周囲の心嚢液貯留の有無を調べるのに役立つ。また、心臓から出る主要な血管である大動脈の評価にも有用である[113]。
治療
[編集]心臓に影響を及ぼす病気は、ライフスタイルの改善、薬物治療、手術など、さまざまな方法で治療される。
虚血性心疾患
[編集]冠状動脈の狭窄(虚血性心疾患)は、部分的に狭窄した動脈による胸痛(狭心症)の緩和、完全に閉塞した動脈(心筋梗塞)による心筋損傷の最小化、または心筋梗塞の予防を目的として治療される。狭心症の症状を改善する薬には、ニトログリセリン、β遮断薬、カルシウム拮抗薬がある。予防的治療には、抗血小板薬(アスピリンなど)やスタチン、禁煙や減量などの生活習慣の改善、さらに高血圧や糖尿病のリスク因子の管理が含まれる[127]。
薬物治療に加えて、狭窄した冠動脈は、血流を広げる方法や血流を再配置して閉塞を回避する方法で治療されることがある。これには、経皮的冠動脈形成術が含まれ、小さなバルーン付きのワイヤーを冠動脈に通し、バルーンを膨らませて狭窄を広げ、時には金属製のステントを残して動脈を開いた状態に保つ方法がある[25]。
冠動脈の狭窄が経皮的冠動脈形成術では治療に適さない場合、開胸手術が必要となることがある。この場合、別の部位の血管(例えば、大伏在静脈、橈骨動脈、または内胸動脈)を使用して、狭窄前の部分(通常は大動脈)から狭窄後の部分に血管を吻合する冠動脈バイパス術が行われる[25][128]。
弁膜性心疾患
[編集]異常に狭くなったり、逆流が生じるようになったりした心臓の弁は、手術が必要になることがある。この手術は、通常、損傷した心臓の弁をウシやブタの組織、または金属製の人工心臓弁に置き換える開胸手術として行われることが一般的である。ただし、状況によっては、三尖弁や僧帽弁を修復することで、弁置換手術を回避できる場合もある。また、心臓弁は、経皮的冠動脈形成術と類似した技術を使用して、経皮的に治療することもある。たとえば、経カテーテル的大動脈弁置換術は、開胸による弁置換が高リスクと判断された患者に対して、行われることが増えている[92]。
心不整脈
[編集]異常な心臓のリズム(不整脈)は、抗不整脈薬を使用して治療できる。これらの薬は、カルシウム拮抗薬、ナトリウムチャネル遮断薬、アミオダロン、ジゴキシンなど、電解質の細胞膜を横切る流れを調整するか、または心臓に対する自律神経系の影響を変更する(β遮断薬やアトロピン)。一部の不整脈、たとえば心房細動のような脳梗塞リスクを高めるものは、ワルファリンや直接経口抗凝固薬などの抗凝固薬を使用して、このリスクを低減できる[98]。
薬物で不整脈が制御できない場合、別の治療法としてカテーテルアブレーションがある。この手技では、足の静脈や大腿動脈から心臓に向かってワイヤーを通し、不整脈の原因となっている異常な組織を特定する。その後、その異常な組織を加熱または凍結アブレーションすることで、心臓のリズムの乱れを防ぐ。多くの不整脈は、このような最小限の侵襲的カテーテル技術で治療できるが、特に心房細動は、他の心臓手術の際や単独の手術として、開胸手術や胸腔鏡手術で治療することも可能である。また、電気ショックで異常なリズムを停止させるカルディオバージョンが使用されることもある。
ペースメーカーや除細動器などの心臓デバイスも不整脈の治療に用いられることがある。ペースメーカーは、皮膚下に小さなバッテリーで動く発電機(ジェネレーター)を埋め込み、1本以上のリードが心臓に伸びる装置であり、通常は徐脈(異常に遅い心拍)を治療するために使用される[99]。植込み型除細動器は、命にかかわる速い心拍リズムを治療するために使用される。これらのデバイスは心臓を監視し、危険な心拍数の上昇が検出された場合、自動的に電気ショックを与え、正常なリズムに戻す。埋め込み型除細動器は、心不全や心筋症、または遺伝性不整脈症候群を持つ患者に最もよく使用される。
心不全
[編集]心不全患者の治療は、通常、その原因(虚血性心疾患や高血圧など)を取り除くことから始まり、主に薬物療法が中心となる。これには、患者が生成する尿の量を増やし、肺に液体が溜まるのを防ぐ利尿薬や、心臓のポンプ機能を維持することを目的としたβ遮断薬、アンジオテンシン変換酵素阻害薬、鉱質コルチコイド受容体拮抗薬が含まれる[91]。
心不全患者に対しては、心臓再同期療法(Cardiac resynchronization therapy: CRT)と呼ばれる特殊なペースメーカーを使用して心臓のポンプ効率を向上させることができることもある[99]。これらのデバイスは、除細動器と組み合わせて使用されることが多い。非常に重度の心不全の場合、補助人工心臓と呼ばれる小型ポンプを移植し、心臓のポンプ機能を補助することがある。最も重度のケースでは、心臓移植が検討される場合もある[91]。
関連画像
[編集]脚注
[編集]注釈
[編集]出典
[編集]- ^ “心臓”. コトバンク デジタル大辞泉、精選版日本国語大辞典. 2020年2月20日閲覧。
- ^ 広辞苑 第五版 p.1386【心臓】
- ^ Moran, Michael E. (2013-08-26), “Gray's Anatomy of Stones: Henry Vandyke Carter”, Urolithiasis (New York, NY: Springer New York): pp. 131–144, ISBN 978-1-4614-8195-9 2024年10月5日閲覧。
- ^ a b c d 生化学辞典第2版、p.674 【心臓】
- ^ Taber, Clarence Wilbur; Venes, Donald (2009). Taber's cyclopedic medical dictionary. F.A. Davis Co.. pp. 1018–1023. ISBN 978-0-8036-1559-5
- ^ Guyton & Hall 2011, p. 157.
- ^ a b c Moore, Keith L.; Dalley, Arthur F.; Agur, Anne M.R. (2009). “1”. Clinically Oriented Anatomy. Wolters Kluwel Health/Lippincott Williams & Wilkins. pp. 127–173. ISBN 978-1-60547-652-0
- ^ Starr, Cecie; Evers, Christine; Starr, Lisa (2009). Biology: Today and Tomorrow With Physiology. Cengage Learning. p. 422. ISBN 978-0-495-56157-6. オリジナルの2 May 2016時点におけるアーカイブ。
- ^ Reed, C. Roebuck; Brainerd, Lee Wherry; Lee, Rodney; Kaplan, Inc. (2008). CSET : California Subject Examinations for Teachers (3rd ed.). New York: Kaplan Pub.. p. 154. ISBN 978-1-4195-5281-6. オリジナルの4 May 2016時点におけるアーカイブ。
- ^ a b Gray's Anatomy 2008, p. 960.
- ^ a b c d e f g h i j k l m n o p q r s t u v w x y z aa ab ac ad ae af ag ah ai aj ak al am an ao ap aq ar as at au av aw ax ay az ba bb bc bd be bf bg bh bi bj bk bl bm bn bo bp bq br bs bt bu bv bw bx Betts, J. Gordon (2013). Anatomy & physiology. OpenStax College, Rice University. pp. 787–846. ISBN 978-1-938168-13-0. オリジナルの27 February 2021時点におけるアーカイブ。 11 August 2014閲覧。
- ^ Guyton & Hall 2011, pp. 101, 157–158, 180.
- ^ a b Guyton & Hall 2011, pp. 105–107.
- ^ Guyton & Hall 2011, pp. 1039–1041.
- ^ a b 小室(2004)、p.2-7、I.循環器を深く知るための基本講義、A.構造と機能を学ぶ、心臓の構造
- ^ a b c d e f g h i j 佐藤・佐伯(2009)、p.44-47、第3章 循環、2.心臓heart、1)心臓の構造と機能
- ^ a b c “Cardiovascular diseases (CVDs) Fact sheet N°317 March 2013”. WHO. World Health Organization. 19 September 2014時点のオリジナルよりアーカイブ。20 September 2014閲覧。
- ^ a b c Longo, Dan; Fauci, Anthony; Kasper, Dennis; Hauser, Stephen; Jameson, J.; Loscalzo, Joseph (2011). Harrison's Principles of Internal Medicine (18th ed.). McGraw-Hill Professional. p. 1811. ISBN 978-0-07-174889-6
- ^ Graham, I; Atar, D; Borch-Johnsen, K; Boysen, G; Burell, G; Cifkova, R; Dallongeville, J; De Backer, G et al. (Oct 2007). “European guidelines on cardiovascular disease prevention in clinical practice: executive summary: Fourth Joint Task Force of the European Society of Cardiology and Other Societies on Cardiovascular Disease Prevention in Clinical Practice (Constituted by representatives of nine societies and by invited experts)”. European Heart Journal 28 (19): 2375–2414. doi:10.1093/eurheartj/ehm316. PMID 17726041. オリジナルの27 April 2019時点におけるアーカイブ。 21 October 2019閲覧。.
- ^ “Gray's Anatomy of the Human Body – 6. Surface Markings of the Thorax”. Bartleby.com. 20 November 2010時点のオリジナルよりアーカイブ。2010年10月18日閲覧。
- ^ a b c d e 解剖学第2版、p40-44、循環器系 2.心臓
- ^ Dorland's (2012). Dorland's Illustrated Medical Dictionary (32nd ed.). Elsevier. p. 1461. ISBN 978-1-4160-6257-8
- ^ “How Your Heart Works”. HowStuffWorks (April 2000). 29 July 2016時点のオリジナルよりアーカイブ。14 August 2016閲覧。
- ^ Ampanozi, Garyfalia; Krinke, Eileen; Laberke, Patrick; Schweitzer, Wolf; Thali, Michael J.; Ebert, Lars C. (7 May 2018). “Comparing fist size to heart size is not a viable technique to assess cardiomegaly”. Cardiovascular Pathology 36: 1–5. doi:10.1016/j.carpath.2018.04.009. ISSN 1879-1336. PMID 29859507.
- ^ a b c d Kolh, Philippe; Windecker, Stephan; Alfonso, Fernando; Collet, Jean-Philippe; Cremer, Jochen; Falk, Volkmar; Filippatos, Gerasimos; Hamm, Christian et al. (October 2014). “2014 ESC/EACTS Guidelines on myocardial revascularization: the Task Force on Myocardial Revascularization of the European Society of Cardiology (ESC) and the European Association for Cardio-Thoracic Surgery (EACTS). Developed with the special contribution of the European Association of Percutaneous Cardiovascular Interventions (EAPCI)”. European Journal of Cardio-Thoracic Surgery 46 (4): 517–592. doi:10.1093/ejcts/ezu366. ISSN 1873-734X. PMID 25173601.
- ^ a b Gray's Anatomy 2008, pp. 960–962.
- ^ Gray's Anatomy 2008, pp. 964–967.
- ^ Pocock, Gillian (2006). Human Physiology. Oxford University Press. p. 264. ISBN 978-0-19-856878-0
- ^ Netter 2007, p. 220.
- ^ a b Gray's Anatomy 2008, pp. 966–967.
- ^ a b c 伊藤隆 1983, pp. 283–284.
- ^ Gray's Anatomy 2008, p. 970.
- ^ “Papillary Muscles”. Atlas of Human Cardiac Anatomy. 17 March 2016時点のオリジナルよりアーカイブ。7 March 2016閲覧。
- ^ a b 下髙原理恵、小林幸恵 、島田和幸、島田達生「ヒト心臓における中隔縁柱の分枝」(pdf)『心臓』第41巻第9号、2009年、999-1002頁。
- ^ “pectinate muscle”. The Free Dictionary. 23 August 2018時点のオリジナルよりアーカイブ。2016年7月31日閲覧。
- ^ a b c d 伊藤隆 1983, pp. 300–301.
- ^ a b “Cardiac Muscle and Electrical Activity | BIO103: Human Biology”. courses.lumenlearning.com. 2025年1月1日閲覧。
- ^ a b c “The human proteome in heart”. www.proteinatlas.org. 9 November 2018時点のオリジナルよりアーカイブ。2017年9月29日閲覧。
- ^ Lindskog, Cecilia; Linné, Jerker; Fagerberg, Linn; Hallström, Björn M.; Sundberg, Carl Johan; Lindholm, Malene; Huss, Mikael; Kampf, Caroline et al. (2015-06-25). “The human cardiac and skeletal muscle proteomes defined by transcriptomics and antibody-based profiling”. BMC Genomics 16 (1): 475. doi:10.1186/s12864-015-1686-y. ISSN 1471-2164. PMC 4479346. PMID 26109061.
- ^ Gray's Anatomy 2008, p. 959.
- ^ J., Tortora, Gerard (2009). Principles of human anatomy. Nielsen, Mark T. (Mark Thomas) (11th ed.). Hoboken, NJ: J. Wiley. ISBN 978-0-471-78931-4. OCLC 213300667
- ^ a b “Physiology Tutorial - Coronary Circulation”. www.vhlab.umn.edu. 2025年1月1日閲覧。
- ^ a b c d e f “Blood supply of the heart” (英語). Kenhub. 2025年1月1日閲覧。
- ^ Davidson's 2010, p. 525.
- ^ Gray's Anatomy 2008, p. 981.
- ^ a b Gray's Anatomy 2008, p. 982.
- ^ Davidson's 2010, p. 526.
- ^ Gray's Anatomy 2008, p. 945.
- ^ a b c Miller 2007, p. 576.
- ^ Terry J. DuBose Sex, Heart Rate and Age Archived 2012年6月15日, at the Wayback Machine.
- ^ Moore 1990, p. 338.
- ^ Moore 1990, p. 294.
- ^ a b 小室(2004)、p.5、I.循環器を深く知るための基本講義、A.構造と機能を学ぶ、心臓の発生
- ^ Moore 1990, pp. 294, 295.
- ^ “Main Frame Heart Development”. Meddean.luc.edu. 16 November 2001時点のオリジナルよりアーカイブ。2010年10月17日閲覧。
- ^ a b c d e f g Moore 1990, pp. 300–314.
- ^ DuBose, T.J.; Cunyus, J.A.; Johnson, L. (1990). “Embryonic Heart Rate and Age”. J Diagn Med Sonography 6 (3): 151–157. doi:10.1177/875647939000600306.
- ^ DuBose, T.J. (1996) Fetal Sonography, pp. 263–274; Philadelphia: WB Saunders ISBN 0-7216-5432-0
- ^ DuBose, Terry J. (26 July 2011) Sex, Heart Rate and Age Archived 2 May 2014 at the Wayback Machine.. obgyn.net
- ^ a b c 小室(2004)、p.3、I.循環器を深く知るための基本講義、A.構造と機能を学ぶ、心臓発生研究と疾患治療
- ^ Beltrami, Antonio P.; Urbanek, Konrad; Kajstura, Jan; Yan, Shao-Min; Finato, Nicoletta; Bussani, Rossana; Nadal-Ginard, Bernardo; Silvestri, Furio et al. (2001-06-07). “Evidence That Human Cardiac Myocytes Divide after Myocardial Infarction” (英語). New England Journal of Medicine 344 (23): 1750–1757. doi:10.1056/NEJM200106073442303. ISSN 0028-4793.
- ^ a b Leri, Annarosa (2009-12-22). “Human Cardiac Stem Cells: The Heart of a Truth” (英語). Circulation 120 (25): 2515–2518. doi:10.1161/CIRCULATIONAHA.109.911107. ISSN 0009-7322.
- ^ Petersson, Johan; Glenny, Robb W. (2023-10). “Gas Exchange in the Lung”. Seminars in Respiratory and Critical Care Medicine 44 (5): 555–568. doi:10.1055/s-0043-1770060. ISSN 1098-9048. PMID 37816345.
- ^ a b c d “循環器用語ハンドブック(WEB版) 心周期 | 医療関係者向け情報 トーアエイヨー”. med.toaeiyo.co.jp. 2024年11月3日閲覧。
- ^ a b c d e 佐藤・佐伯(2009)、p.48-52、第3章 循環、2.心臓heart、2)心臓の活動と検査
- ^ Guyton & Hall 2011, pp. 110–113.
- ^ a b Berry, William; McKenzie, Catherine (1 January 2010). “Use of inotropes in critical care”. Clinical Pharmacist 2: 395. オリジナルの28 November 2016時点におけるアーカイブ。.
- ^ a b Bersten, Andrew (2013). Oh's Intensive Care Manual (7th ed.). London: Elsevier Health Sciences. pp. 912–922. ISBN 978-0-7020-4762-6
- ^ Pocock, Gillian (2006). Human Physiology (Third ed.). Oxford University Press. p. 266. ISBN 978-0-19-856878-0
- ^ Antz, Matthias (1998). “Electrical Conduction Between the Right Atrium and the Left Atrium via the Musculature of the Coronary Sinus”. Circulation 98 (17): 1790–1795. doi:10.1161/01.CIR.98.17.1790. PMID 9788835.
- ^ De Ponti, Roberto (2002). “Electroanatomic Analysis of Sinus Impulse Propagation in Normal Human Atria”. Journal of Cardiovascular Electrophysiology 13 (1): 1–10. doi:10.1046/j.1540-8167.2002.00001.x. PMID 11843475.
- ^ “Definition of SA node”. MedicineNet.com (27 April 2011). 1 August 2012時点のオリジナルよりアーカイブ。7 June 2012閲覧。
- ^ 宮内, 靖史 (2010). "プルキンエ線維と不整脈" (pdf). 心臓. 42 (9): 1148–1152.
- ^ Guyton & Hall 2011, pp. 115–120.
- ^ Davis, J.P.; Tikunova, S.B. (2008). “Ca2+ exchange with troponin C and cardiac muscle dynamics”. Cardiovascular Research 77 (4): 619–626. doi:10.1093/cvr/cvm098. PMID 18079104.
- ^ Ostchega, Y; Porter, K.S.; Hughes, J; Dillon, C.F.; Nwankwo, T (2011). “Resting pulse rate reference data for children, adolescents and adults, United States 1999–2008”. National Health Statistics Reports (41): 1–16. PMID 21905522. オリジナルの23 June 2017時点におけるアーカイブ。.
- ^ Guyton, Arthur C.; Hall, John E. (2005). Textbook of medical physiology (11th ed.). Philadelphia: W.B. Saunders. pp. 116–122. ISBN 978-0-7216-0240-0
- ^ Guyton & Hall 2011, p. 208.
- ^ a b c “ベインブリッジ反射 | 医学書院_医療情報サービス”. imis.igaku-shoin.co.jp. 2024年10月26日閲覧。
- ^ Guyton & Hall 2011, p. 212.
- ^ “Tachycardia” (英語). Kenhub. 2024年10月26日閲覧。
- ^ Miller, Hi; Yum, Ky; Durham, Bc (1971-03-01). “Myocardial free fatty acid in unanesthetized dogs at rest and during exercise” (英語). American Journal of Physiology-Legacy Content 220 (3): 589–596. doi:10.1152/ajplegacy.1971.220.3.589. ISSN 0002-9513.
- ^ Kaijser, L.; Berglund, B. (1992-01). “Myocardial lactate extraction and release at rest and during heavy exercise in healthy men” (英語). Acta Physiologica Scandinavica 144 (1): 39–45. doi:10.1111/j.1748-1716.1992.tb09265.x. ISSN 0001-6772.
- ^ a b c “Cardiovascular diseases (CVDs)” (英語). World Health Organization. 10 March 2016時点のオリジナルよりアーカイブ。2016年3月9日閲覧。
- ^ “循環器内科とは? どんな症状がある人が受診すべきなの?|スマートドック | 健康コラム” (2021年12月1日). 2024年12月30日閲覧。
- ^ “Your Heart Failure Healthcare Team”. www.heart.org. 10 March 2016時点のオリジナルよりアーカイブ。2016年3月9日閲覧。
- ^ a b c “Different heart diseases”. World Heart Federation. 12 March 2016時点のオリジナルよりアーカイブ。2016年3月9日閲覧。
- ^ “狭心症 - 04. 心血管疾患”. MSDマニュアル プロフェッショナル版. 2024年12月30日閲覧。
- ^ Harrison's 2011, p. 1501.
- ^ Davidson's 2010, p. 554.
- ^ a b c d e f g h i Ponikowski, Piotr; Voors, Adriaan A.; Anker, Stefan D.; Bueno, Héctor; Cleland, John G.F.; Coats, Andrew J.S.; Falk, Volkmar; González-Juanatey, José Ramón et al. (August 2016). [https://web.archive.org/web/20200614214934/https://orbi.uliege.be/bitstream/2268/205777/1/2016%20ESC%20Guidelines%20for%20the%20diagnosis%20and%20treatment%20of%20acute%20and%20chronic%20heart%20failure.pdf “2016 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure: The Task Force for the diagnosis and treatment of acute and chronic heart failure of the European Society of Cardiology (ESC). Developed with the special contribution of the Heart Failure Association (HFA) of the ESC”]. European Journal of Heart Failure 18 (8): 891–975. doi:10.1002/ejhf.592. hdl:2434/427148. ISSN 1879-0844. PMID 27207191. オリジナルの14 June 2020時点におけるアーカイブ。 24 September 2019閲覧。.
- ^ a b Vahanian, Alec; Alfieri, Ottavio; Andreotti, Felicita; Antunes, Manuel J.; Barón-Esquivias, Gonzalo; Baumgartner, Helmut; Borger, Michael Andrew; Carrel, Thierry P. et al. (October 2012). “Guidelines on the management of valvular heart disease (version 2012): the Joint Task Force on the Management of Valvular Heart Disease of the European Society of Cardiology (ESC) and the European Association for Cardio-Thoracic Surgery (EACTS)”. European Journal of Cardio-Thoracic Surgery 42 (4): S1–44. doi:10.1093/ejcts/ezs455. ISSN 1873-734X. PMID 22922698.
- ^ Davidson's 2010, pp. 612–613.
- ^ Hall 2018, p. 114.
- ^ Barrett 2022, p. 607.
- ^ Hall 2018, p. 140.
- ^ “Heart arrhythmia - Symptoms and causes” (英語). Mayo Clinic. 2024年12月30日閲覧。
- ^ a b Kirchhof, Paulus; Benussi, Stefano; Kotecha, Dipak; Ahlsson, Anders; Atar, Dan; Casadei, Barbara; Castella, Manuel; Diener, Hans-Christoph et al. (November 2016). “2016 ESC Guidelines for the management of atrial fibrillation developed in collaboration with EACTS”. Europace 18 (11): 1609–1678. doi:10.1093/europace/euw295. ISSN 1532-2092. PMID 27567465.
- ^ a b c European Society of Cardiology (ESC); European Heart Rhythm Association (EHRA); Brignole, Michele; Auricchio, Angelo; Baron-Esquivias, Gonzalo; Bordachar, Pierre; Boriani, Giuseppe; Breithardt, Ole-A. et al. (August 2013). “2013 ESC guidelines on cardiac pacing and cardiac resynchronization therapy: the task force on cardiac pacing and resynchronization therapy of the European Society of Cardiology (ESC). Developed in collaboration with the European Heart Rhythm Association (EHRA)”. Europace 15 (8): 1070–1118. doi:10.1093/europace/eut206. ISSN 1532-2092. PMID 23801827.
- ^ Blomström-Lundqvist, Carina; Scheinman, Melvin M.; Aliot, Etienne M.; Alpert, Joseph S.; Calkins, Hugh; Camm, A. John; Campbell, W. Barton; Haines, David E. et al. (2003-10-14). “ACC/AHA/ESC guidelines for the management of patients with supraventricular arrhythmias – executive summary: a report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines and the European Society of Cardiology Committee for Practice Guidelines (Writing Committee to Develop Guidelines for the Management of Patients With Supraventricular Arrhythmias)”. Circulation 108 (15): 1871–1909. doi:10.1161/01.CIR.0000091380.04100.84. ISSN 1524-4539. PMID 14557344.
- ^ Davidson's 2010, pp. 638–639.
- ^ Baumgartner, Helmut; Bonhoeffer, Philipp; De Groot, Natasja M.S.; de Haan, Fokko; Deanfield, John Erik; Galie, Nazzareno; Gatzoulis, Michael A.; Gohlke-Baerwolf, Christa et al. (December 2010). “ESC Guidelines for the management of grown-up congenital heart disease (new version 2010)”. European Heart Journal 31 (23): 2915–2957. doi:10.1093/eurheartj/ehq249. ISSN 1522-9645. PMID 20801927.
- ^ Harrison's 2011, p. 1458–65.
- ^ Marbán, Eduardo (2002-01-10). “Cardiac channelopathies”. Nature 415 (6868): 213–218. Bibcode: 2002Natur.415..213M. doi:10.1038/415213a. ISSN 0028-0836. PMID 11805845.
- ^ Marban, Eduardo (2003-07-01). “Cardiac Channelopathies” (英語). Heart Views 4 (3): 4. ISSN 1995-705X.
- ^ “Channelopathies That Lead to Sudden Cardiac Death: Clinical and Genetic Aspects”. Heart Lung Circ 28 (1): 22–30. (January 2019). doi:10.1016/j.hlc.2018.09.007. PMID 30389366.
- ^ “Long QT Syndrome” (英語). NORD (National Organization for Rare Disorders). 2022年11月19日閲覧。
- ^ “Catecholaminergic polymorphic ventricular tachycardia: MedlinePlus Genetics” (英語). medlineplus.gov. 2022年11月19日閲覧。
- ^ “Progressive familial heart block: MedlinePlus Genetics” (英語). medlineplus.gov. 2022年11月19日閲覧。
- ^ Bourier, Felix; Denis, Arnaud; Cheniti, Ghassen; Lam, Anna; Vlachos, Konstantinos; Takigawa, Masateru; Kitamura, Takeshi; Frontera, Antonio et al. (2018-11-27). “Early Repolarization Syndrome: Diagnostic and Therapeutic Approach”. Frontiers in Cardiovascular Medicine 5: 169. doi:10.3389/fcvm.2018.00169. ISSN 2297-055X. PMC 6278243. PMID 30542653.
- ^ “Brugada syndrome: MedlinePlus Genetics” (英語). medlineplus.gov. 2022年11月19日閲覧。
- ^ Davidson's 2010, pp. 527–534.
- ^ a b c Davidson's 2010, pp. 522–536.
- ^ a b c d 武内重五郎 1997, p. 216.
- ^ a b Talley, Nicholas J.; O'Connor, Simon (2013). Clinical Examination. Churchill Livingstone. pp. 76–82. ISBN 978-0-7295-4198-5
- ^ a b 武内重五郎 1997, p. 217.
- ^ a b Davidson's 2010, pp. 556–559.
- ^ 武内重五郎 1997, p. 221.
- ^ 武内重五郎 1997, pp. 219–229.
- ^ 武内重五郎 1997, p. 230.
- ^ “Acute Coronary Syndrome Workup”. Medscape. 6 August 2016時点のオリジナルよりアーカイブ。14 August 2016閲覧。
- ^ Davidson's 2010, pp. 531.
- ^ Harrison's 2011, p. 1534.
- ^ Davidson's 2010, pp. 521–640.
- ^ a b c d Davidson's 2010, pp. 528–530.
- ^ Armstrong, William F.; Ryan, Thomas; Feigenbaum, Harvey (2010). Feigenbaum's Echocardiography. Lippincott Williams & Wilkins. ISBN 978-0-7817-9557-9. オリジナルの23 April 2016時点におけるアーカイブ。
- ^ Authors/Task Force Members; Piepoli, Massimo F.; Hoes, Arno W.; Agewall, Stefan; Albus, Christian; Brotons, Carlos; Catapano, Alberico L.; Cooney, Marie-Therese et al. (September 2016). “2016 European Guidelines on cardiovascular disease prevention in clinical practice: The Sixth Joint Task Force of the European Society of Cardiology and Other Societies on Cardiovascular Disease Prevention in Clinical Practice (constituted by representatives of 10 societies and by invited experts) Developed with the special contribution of the European Association for Cardiovascular Prevention & Rehabilitation (EACPR)”. Atherosclerosis 252: 207–274. doi:10.1016/j.atherosclerosis.2016.05.037. ISSN 1879-1484. PMID 27664503. オリジナルの28 August 2021時点におけるアーカイブ。 11 September 2018閲覧。.
- ^ Davidson's 2010, pp. 585–588, 614–623.
参考文献
[編集]- Hall, John (2011). Guyton and Hall Textbook of Medical Physiology (12th ed.). Philadelphia: Saunders/Elsevier. ISBN 978-1-4160-4574-8
- Longo, Dan; Fauci, Anthony; Kasper, Dennis; Hauser, Stephen; Jameson, J.; Loscalzo, Joseph (2011). Harrison's Principles of Internal Medicine (18th ed.). McGraw-Hill Professional. ISBN 978-0-07-174889-6
- Susan Standring; Neil R. Borley, eds (2008). Gray's anatomy : the anatomical basis of clinical practice (40th ed.). London: Churchill Livingstone. ISBN 978-0-8089-2371-8
- Nicki R. Colledge; Brian R. Walker; Stuart H. Ralston, eds (2010). Davidson's principles and practice of medicine (21st ed.). Edinburgh: Churchill Livingstone/Elsevier. ISBN 978-0-7020-3085-7
- Netter, Frank H. 著、相磯貞和 訳『ネッター解剖学アトラス (原書第4版)』南江堂、2007年。ISBN 9784524250325。
- 伊藤隆『解剖学講義』南山堂、1983年10月1日。ISBN 978-4-525-10051-3。
- Miller, Ronald 著、武田純三 訳『ミラー麻酔科学』メディカルサイエンスインターナショナル、2007年4月1日。ISBN 9784895924658。
- 武内重五郎『内科診断学』(改訂第15版)南江堂、1997年5月1日。ISBN 4-524-20237-4。
- Moore, Keith L. 著、星野一正 訳『MOORE人体発生学』(第4版)医歯薬出版、1990年3月1日。ISBN 4263202252。
- 『生化学辞典第2版』(第2版第6刷)東京化学同人、1995年。ISBN 4-8079-0340-3。
- 河野邦雄、伊藤隆造、坂本裕和、前島徹、樋口桂 著、財団法人 東洋療法学校協会 編『解剖学第2版』(第2版第1刷)医歯薬出版、2006年。ISBN 4-263-24207-6。
- 佐々木猛智『貝類学』(第1刷)東京大学出版会、2010年。ISBN 978-4-13-060190-0。
- 監修:佐藤昭夫、佐伯由香『人体の構造と機能 第2版』(第2版第6刷)医歯薬出版、2009年。ISBN 978-4-263-23434-1。
- 編集:小室一成、編集協力:川名正敏 萩原誠久 中村文隆 吉田勝哉『講義録 循環器学』(第1版第2刷)メディカルビュー社、2006年。ISBN 4-7583-0056-9。
- Hall, Jhon E. 著、石川義弘 訳『ガイトン生理学』(13版)エルゼビア・ジャパン、2018年3月20日。ISBN 9784860347741。
- Barrett, Kim E. 著、佐久間康夫、岡村康司 訳、岡田泰伸 編『ギャノング生理学』(原書26版)丸善出版、2022年2月25日。ISBN 9784621307083。
関連項目
[編集]外部リンク
[編集]- 心臓の構造と機能(ビジュアル生理学 内の項目)
- 『Anesth Earth/作業場2』 - コトバンク
- "循環器学用語集". 日本循環器学会. 2024年10月21日閲覧。
- "In Brief - Your Guide to a Healthy Heart Fact Sheet" [一般向けに心臓を健康に維持する方法を記した小冊子]. アメリカ国立心肺血液研究所 (英語). 2024年10月21日閲覧。
- "Atlas of Human Cardiac Anatomy" [ヒトの心臓解剖アトラス]. ミネソタ大学 (英語). 2024年10月21日閲覧。
- Dissection review of the anatomy of the Human Heart including vessels, internal and external features
- McNulty, John A. (14 April 1996). "Heart Development" [心臓の発生]. Loyola University Medical Center (英語). 2024年11月3日閲覧。
- The Heart, BBC Radio 4 interdisciplinary discussion with David Wootton, Fay Bound Alberti & Jonathan Sawday (In Our Time, 1 June 2006)
- . Encyclopædia Britannica (英語). Vol. 13 (11th ed.). 1911. pp. 129–134.